Molekulární mechanismy regulace renálních progenitorů: Kolik dílků v hádance?
Feb 24, 2022
Abstraktní: Ledvinymyší, krys a lidí mají progenitory, které udržují každodenní homeostázu a účastní se endogenních regeneračních procesů po poranění, díky své schopnosti proliferovat a diferencovat. V glomerulárních a tubulárních kompartmentech nefronu konzistentní studie prokázaly, že dobře charakterizované, odlišné populace progenitorových buněk, lokalizované v parietálním epitelu Bowmanova pouzdra a rozptýlené v proximálních a distálních tubulech, mohou za fyziologických podmínek vytvářet segmentově specifické buňky. a po poranění tkáně. Avšak defektní nebo abnormální regenerační reakce těchto progenitorů mohou přispívat k patologickým stavům. Molekulární charakteristikyledvinovéprogenitory byly rozsáhle studovány, což ukazuje, že četné klasické a evolučně konzervované dráhy, jako je Notch nebo Wnt/-catenin, hrají hlavní roli v buněčné regulaci. Další, jako je kyselina retinová, renin-angiotensin-aldosteronový systém, TLR2 (Toll-like receptor 2) a leptin, jsou také důležité v tomto procesu. V tomto přehledu shrnujeme nepřeberné množství řízení molekulárních mechanismůledvinovéprogenitorové reakce během homeostázy a po níporanění ledvin.Nakonec prozkoumáme, jak by jednobuněčné sekvenování RNA mohlo přinést charakterizaciledvinovéprogenitory na další úroveň, přičemž znalost jejich molekulárního podpisu získává na klinice význam.
klíčová slova:renální progenitory; molekulární mechanismy; poškození ledvin; sekvenování jednobuněčné RNA; molekulární podpis

CISTANCHE ZLEPŠÍ ONEMOCNĚNÍ LEDVIN/RENÁL
Úvod Pro několik orgánů savců byly navrženy mechanismy endogenní regenerace a opravy [1]. Klasické regenerační orgány, jako je gastrointestinální trakt a kůže, byly v průběhu let rozsáhle studovány a odhalily hlavní roli endogenních progenitorů [2]. Ve střevě udržují střevní kmenové buňky každodenní homeostázu, zatímco odlišné kmenové/progenitorové buňky mají na starosti rychlé opravné procesy po poranění [2]. Podobně epidermální kmenové buňky tvoří heterogenní zásobu kmenových buněk, které se po poranění účastní epidermální homeostázy a také opravy tkáně [3]. Dospělýledvinaje orgán s nízkým buněčným obratem a obdařený progenitory schopnými proliferace a diferenciace [4,5]. Tato cenná vlastnost umožňuje výzkumníkům a lékařům uvažovat o nových terapeutických cestách k obnověfunkce ledvinpo zranění. Zde navrhujeme přehled molekulárních mechanismů probíhajících v glomerulárních a tubulárníchledvinovéprogenitory ve fyziologických a patologických stavech (obrázek 1) a o tom, jak by dysregulace těchto drah mohla být původemnemoc ledvin. Budeme také zkoumat, jakledvinovéprogenitory by mohly být dále charakterizovány pomocí technologie sekvenování jednobuněčné RNA (scRNAseq) a klinický význam molekulárního podpisu těchto buněk.


Renální progenitory
Renální progenitory objevili Sagrinati et al. u člověkaledvinyna základě exprese markerů kmenových buněk CD133 a CD24, při absenci nebo nízké expresi diferenciačních markerů [6,7]. Buňky CD133 plus CD24 plus jsou lokalizovány na močovém pólu Bowmanova pouzdra a také rozptýleny podél tubulárního kompartmentu nefronu mezi diferencovanými tubulárními buňkami [6]. Nějakýledvinovéprogenitory, včetně těch, které jsou lokalizovány v Bowmanově pouzdru a podskupina těch, které se nacházejí sc podél tubulu, také exprimují CD106 (také nazývaný vaskulární buněčná adhezní molekula 1, VCAM1), zatímco většina progenitorů lokalizovaných podél tubulu nikoli [6, 8]. Tyto fenotypické dCfferences odrážejí různorodou funkční kapacitu; CD133 plus CD24 plus CD106- buňky rozptýlené podél tubulů skutečně vykazují funkční rysy tubulárních progenitorů, zatímco CD133 plus CD24 plus CD106 plus parietální epiteliální úhoře (PEC) jsou multipotentní [6]. Navíc podskupina CD1 33 plus CD24 plus CD1 06 plus progenitorů lokalizovaných blízko distálního pólu Bowmanova pouzdra a exprimujících podokalyxin je schopna generovat pouze podocyty [6]. Celkově tato pozorování konfigurují hierarchickou liniiledvinovépředchůdci uvnitřledvinakterý připomíná hemopoetický systém [9]. PEC s podobnými progenitorovými rysy a anatomickou lokalizací byly také identifikovány u myší a potkanůledviny[4,10,11]. Genetické značení PEC v transgenní indukovatelné myší linii prokázalo, že PEC migrují do glomerulárních chomáčů a diferencují se na podocyty u dospělých myší [11]. V poslední době byl Pax2 identifikován jako marker pro myšledvinovéprogenitorů a vytvoření indukovatelného myšího modolu pro sledování linie buněčné populace Pax2 plus umožnilo demonstrovat diferenciaciledvinovéprogenitory lokalizované mezi PEC do podocytů během postnatálního glomerulárního růstu [4]. Další studie prokázaly, že juxtamedulární a kortikolové glomeruly mají různý počet Pax2 plus progenitorů, přičemž kortikální mají dvojnásobný počet Pax2 plus progenitorů, kteří čůrají počet glomerulárních podocytů ve zdravých podmínkách [12]. U dospělých potkanůledvinyMezi epiteliálními buňkami vystýlajícími krysí Bowmanovo pouzdro byly popsány nezralé buňky exprimující neurální buněčnou adhezní molekulu (NCAM) a marker progenitorových buněk CD24 [10].
Genetické značení Pax2 plus progenitorů Bowmanova pouzdra myší umožnilo prokázat, že tyto progenitory se diferencují na podocyty v modelech fokální segmentální glomerulosklerózy (FSGS) a jejich reakce na poranění určuje výsledek glomerulárních poruch, což dále potvrzuje jejich roli jako podocytů. progenitory [4,12]. Kaverina a kolegové nedávno s použitím modelu transgenních myší, ve kterém byly podocyty značeny GFP (zelený fluorescenční protein) a PEC současně značeny tdTomato, poskytli silný důkaz, že PEC slouží jako zdroj nových podocytů u dospělých myší po poranění. Tyto buňky koexprimovaly dvě fluorescenční značky, získaly podocytové markery a vykazovaly primární, sekundární a terciární výběžky nohy [13]. Abnormální progenitorová odpověď na poranění může také přispět k glomerulárním poruchám [4,10,14,15]. Bylo skutečně prokázáno, že za určitých podmínek, u lidí, myší a potkanů, chaotická migrace a proliferace progenitorových buněk Bowmanova pouzdra přispívá k tvorbě srpku a glomerulárním jizvám [4,10,14]. Studie na člověkuledvinovébiopsie jsou v souladu s představou, že proliferující progenitory generují hyperplastické léze u srpkovité a kolabující glomerulopatie [14] a podobné výsledky byly získány u potkanů [10]. Sledování linie PEC u myší prokázalo, že jejich proliferace vede k výraznému zvýšení počtu buněk v srpcích myší nefrotoxické sérové nefritidy a kolapsující glomerulopatie [16] a tvorbě sklerotických lézí a ukládání extracelulární matrix u FSGS [15]. V nedávné době specifické genetické sledování progenitorů mezi PEC prokázalo jejich zapojení do tvorby hyperplastických glomerulárních lézí, které lze považovat za selhání regenerace podocytů po poranění [4]. Ze všech těchto studií je nyní jasné, želedvinovéprogenitory lokalizované mezi PEC reagují na poškození podocytů a spouštějí regenerační program, ale neefektivní nebo nadměrná reakce může vést k tomu, že se funkční tkáň stane jizvou podobnou tkání složenou z buněk a dezorganizované extracelulární matrix. Proto znalost mechanismů, které řídí správnou proliferativní a diferenciační odpověďledvinovéprogenitorů během homeostázy a po zranění má zásadní význam a může umožnit identifikaci domnělých modulátorů pro posílení regeneračního potenciáluledvinovépředchůdci.
Regulátory glomerulární progenitorové fyziologie: Když orchestr ladí melodii
Které signální dráhy regulují klid glomerulárních progenitorů, proliferaci a diferenciaci směrem k podocytům u zdravýchledviny? Studie nefrogeneze prokázaly, že aktivace signalizace -catenin/Wnt představuje klíčový krok vedoucí k diferenciaci PEC na podocyty během vývoje [17,18]. Delece Ctnnb1 (-catenin 1) v PEC u myší s podmíněným knockoutem v pozdním stadiu těla ve tvaru písmene S vyvolala glomerulární anomálie a nahrazení PEC v Bowmanových pouzdrech dobře diferencovanými podocyty. Sledování nefrogeneze u embryonálních podmíněně knockoutovaných myší s kateninem odhalilo, že tyto "parietální podocyty" pocházejí z prekurzorových buněk v parietální vrstvě těla ve tvaru písmene S přímým přepnutím linie. Tato zjištění ukazují, že pro správnou diferenciaci a zrání PEC na podocyty je nutná signalizace -catenin/Wnt [17]. WT1, hlavní regulátor tohoto procesu [19], je také silným inhibitorem signální dráhy -catenin/Wnt [18]. Studie provedené v klidových PEC prokázaly, že exprese WT1 je potlačena vysokými hladinami Pax2 a expresí vysokých hladin mikroRNA-193a (miR-193a) [20]. Když PEC snižují expresi miR-193a, umožňuje to upregulaci WT1, která potlačuje signalizaci -catenin/Wnt a indukuje diferenciaci PEC na podocyty. Nedávné výsledky in vitro ukázaly, že apolipoprotein L1 (APOL1) také reguluje molekulární fenotyp PEC prostřednictvím modulace exprese miR193a a že APOL1 a miR193a sdílejí vzájemný vztah zpětné vazby [21]. V kultivačním systému byla diferenciace PEC na podocyty skutečně doprovázena poklesem exprese miR-193a. Podobně potlačení miR-193a zvýšilo expresi APOL1 [21]. Budoucí práce by se měly zabývat tím, zda tato osa APOL1–miR-193a funguje podobným způsobem in vivo jako in vitro u relevantních transgenních myších modelů a u lidíledviny. Je zajímavé, že APOL1 je gen náchylnosti s genetickými variantami, které zvyšují pravděpodobnost rozvoje podocytopatií [22].
Řízení rozhodování o buněčném osudu a buněčné proliferace v mnoha různých systémech je provozováno prostřednictvím integrované signalizace signálních drah Wnt a Notch [23]. Lasagni a kol. oznámil, že vledvinovéprogenitorů lokalizovaných v Bowmanově pouzdru, aktivace Notch podporuje vstup do S-fáze buněčného cyklu a následnou mitózu, dokud nejsou v nediferencovaném stavu [24]. Nicméně narušená downregulace dráhy Notch běhemledvinovéprogenitorová diferenciace indukovala tvorbu podocytů s abnormálním obsahem DNA a jejich následnou smrt mitotickou katastrofou [24,25]. Nedávné výsledky naznačují, že CXCL12 odvozený z podocytů (chemokinový ligand 12 motiv CXC) inhibuje signalizaci Notch, čímž udržuje klidový stav progenitorů podocytů [12]. Notch downregulace souvisí s upregulací inhibitorů buněčného cyklu p21, p27 a p57 a downregulací cyklinu D1 [24], což podocytu propůjčuje charakteristiky postmitotické, neproliferativní buňky. Mechanismus zpětné vazby podocyt-renální progenitor zprostředkovaný CXCL12- také omezuje regeneraci podocytů po glomerulárním poškození [12]. Ve skutečnosti pomocí sledování linie Pax2 plusledvinovéprogenitorů u myší s nefropatií vyvolanou Adriamycinem vědci ukázali, že blokáda CXCL12 podporuje tvorbu podocytů de novo a zmírňuje glomerulosklerózu [12].

CISTANCHE ZLEPŠÍ FUNKCI LEDVIN/RENÁL
Jako vylepšeníledvinovédiferenciace progenitorů na podocyty může představovat atraktivní terapeutickou strategii k podpoře remise glomerulárních poruch, bylo provedeno několik studií k identifikaci diferenciačních sloučenin. Retinové kyseliny (RA) jsou deriváty vitaminu A se zavedenými výhodami při léčbě různých druhů rakoviny [26]. Bylo také prokázáno, že RA chrání předpoškození ledvinv několika experimentálních modelechnemoc ledvin,včetně onemocnění s minimálními změnami, membranózní nefropatie, FSGS, nefropatie asociované s virem lidské imunodeficience (HIV) (HIVAN) a lupusové nefritidy [27]. Četné studie zdůraznily roli RA v diferenciaci podocytů in vitro [28,29] a my jsme použili RA v kultivačním médiu pro podporuledvinovédiferenciace progenitorů směrem k podocytární linii [7]. Je zajímavé, že expozice albuminu, který váže RA s vysokou afinitou, během in vitro kultur by mohla inhibovatledvinovédiferenciace progenitorů směrem k podocytům sekvestrací RA. In vivo jsme uvedli, že RA se uvolnila v Bowmanově prostoru po glomerulárním poškození a zastavení endogenní syntézy RA v modelu fokální segmentální glomerulosklerózy zhoršilo albuminurii, glomerulární poškození a mortalitu [30]. Exogenní podávání RA, neutralizující sekvestrační aktivitu albuminu, umožnilo regenerační odpověďledvinovéprogenitorů, což vede ke zvýšení počtu podocytů a zlepšenífunkce ledvin[30]. Nedávné výsledky Lasagni et al. [4] potvrdili hypotézu, že farmakologické přístupy, které zvyšují citlivost podocytů na signalizaci RA, by zmírnily progresi experimentálníhopoškození ledvin. Opravdu, léčba in vitroledvinovéprogenitory s RA v přítomnosti 6-bromo-indirubin-30 -oximu (BIO), inhibitoru glykogensyntázy kinázy 3 (GSK3), vyvolaly silnou diferenciaciledvinovéprogenitorů směrem k podocytům prostřednictvím aktivace transkripční aktivity RA-responsive elements (RARE), tj. zvýšení citlivosti renálních progenitorů na diferenciační účinky endogenní RA. Zlepšení diferenciace renálních progenitorů na podocyty pomocí BIO v myším modelu FSGS vedlo k důležitému účinku na onemocnění, zvýšení remise onemocnění u léčených myší. V progresivním stadiu myšího modelu diabetu 2. typu souvisejícího s obezitou, BIO jako doplněk k inhibici duálního renin-angiotenzinového systému (RAS)/transportéru sodíku a glukózy (SGLT)-2 metforminem, ramiprilem a empagliflflozinem zmírnil pokles rychlosti glomerulární fifiltrace (GFR) dalším snížením glomerulosklerózy, zvýšením počtu podocytů díky udržení specializace, stejně jako indukcí de novo diferenciace od progenitorů podocytů a zlepšením hustoty fifiltračních štěrbin [31].
Endlich a kol. prokázali roli Dach1 (jezevčík homolog 1) při určování buněčného osudu PEC do podocytů a pro správnou funkci podocytů. Podocyty exprimují vysoké hladiny Dach1 in vivo a in vitro, zatímco PEC exprimují velmi nízké hladiny Dach1. Autoři zjistili, že indukce exprese Dach1 v PEC významně upreguluje podocytově specifické proteiny synaptopodin a WT1. Zajímavé je, že Dach1 je součástí regulační sítě Eya-Six-Hox-Pax a regulace exprese synaptopodinu byla doprovázena současnou downregulací exprese Pax2 [32].
Guhr a kol. analyzovány jakými mechanismyledvinovéprogenitory si udržují potenciál exprimovat podocytové proteiny za patofyziologických podmínek a prokázaly, že obsahují aktivovaný ubikvitin-proteazomový systém (UPS), který vede k rychlé degradaci nově syntetizovaných proteinů specifických pro podocyty [33]. Na druhé straně UPS udržuje identitu podocytů regulací hladin proteinů specifických pro podocyty, jako jsou proteiny vázající aktin – aktinin 4 (ACTN4) a synaptopodin (SYNPO), transkripční faktor Wilms tumor 1 (WT1), člen rodiny stomatinů podocin, protein štěrbinové diafragmy nefrin, adaptorový protein NCK1 a aktivovaná proteinkináza Cλ (PKCλ) [33]. Aktivita UPS je proto důležitým determinantem fenotypů glomerulárních buněk a stavu diferenciace.Je dobře známo, že vledvina,mechanické prostředí je v zavedených modelech glomerulárních onemocnění podrobeno modifikacím a může ovlivnit diferencovaný stav řady buněčných typů, včetně podocytů [34]. Nedávno jsme analyzovali vliv tuhosti substrátu naledvinovéprogenitorové chování, což prokazuje, že alespoň in vitro je fenotyp člověkaledvinovéprogenitorů je vysoce závislá na Youngově modulu substrátu, což je míra tuhosti materiálu definovaná jako poměr napětí k napětí, přičemž tužší substráty podporují proliferaci a migraci renálních progenitorů. Tuhost substrátu moduluje také kapacituledvinovéprogenitory k diferenciaci směrem k podocytům, přičemž Youngův modul 12 kPa je optimální mezi analyzovanými. Pomocí chemických a genetických inhibitorů jsme prokázali, že aktivita Rho kinázy (ROCK) je nutná ke zprostředkování účinků tuhosti naledvinovéproliferace, migrace a diferenciace progenitorů [35]. Snížená glomerulární tuhost je společným rysem mnoha forem glomerulárního poškození, včetně FSGS [34,36], což naznačuje důležitou roli ROCK také vnemoc ledvin.
Inhibitory renin angiotensin aldosteronového systému (RAAS-I) jsou léky účinné při zpomalení progresenemoc ledvinprostřednictvím různých akcí. Mechanismy odpovědné za terapeutické účinky těchto léků, stejně jako jejichledvinovébuněčné cíle, byly z velké části studovány na několika zvířecích modelech člověkanemoc ledvin. Nedávné údaje ukázaly, že mohou také uplatnit své příznivé účinky propagacíledvinovéprogenitorová diferenciace na podocyty. V krysím modelu glomerulárního poškození léčba ACE-I skutečně vyvolala snížení proliferace progenitorů, snížení tvorby srpku a zabránilo progresi směrem ke glomeruloskleróze [10]. Zmírnění aktivace progenitorových buněk léky tedy obnovilo normální glomerulární architekturu [10]. Je zajímavé, že exprese receptoru angiotenzinu (Ang) II, AT1, byla omezena na vzácné CD24 plus PEC u normálních lidí.ledvinyale byl upregulován v hyperplastických lézích [37], což naznačuje příspěvek dráhy receptoru Ang II/AT1 k podpoře abnormálníchledvinovémigrace a proliferace progenitorů u proliferativních onemocnění [37]. V souladu s tím, u pacienta postiženého CGN (crescentic glomerulonefritis), ACE-I terapie spojená s regresí hyperplastických lézí a normalizovala expresi AT1 receptoru naledvinovépředchůdci. Tyto výsledky poskytují další vysvětlení pro příznivé účinky pozorované po léčbě blokátorem receptoru angiotenzinu II (ARB). Podobně léčba ARB zlepšila výsledek u potkaního modelu mesangiální proliferativní glomerulonefritidy, což vyvolalo zvýšení počtu PEC exprimujících markery kmenových buněk [38].
Poranění podocytů jsou považována za důležitý přispěvatel k diabetunemoc ledvinprogrese do konečné fázenemoc ledvin[39–41]. Suganami a kol. hlášeny prevence a zvrácenípoškození ledvinpodáváním leptinu na zvířecích modelech diabetické nefropatie [39]. Nedávno Pichaiwong et al. prokázali, že nahrazení leptinu by mohlo zvrátit strukturální a funkční parametry pokročilé diabetické nefropatie u BTBR ob/ob myši s deficitem leptinu [41]. Zejména léčba leptinem, ale ne RAAS-I, vedla k významnému zvýšení hustoty a počtu podocytů a ke zvýšení WT1-pozitivní proliferující PEC. Mechanismy, které jsou základem tohoto procesu, byly dále popsány v následné práci, kde ukázaly, že duální léčba ob/ob myší s deficitem leptinu se selektivním antagonistou receptoru endotelin-1 typu A (ETAR) v kombinaci s inhibicí RAAS vedly ke zlepšenému fenotypu [40], charakterizovanému aktivací PEC a zvýšeným počtem podocytů. Tyto výsledky poskytují nepřímý důkaz, že PEC mohou být potenciálním rezervoárem pro obnovu ztracených podocytů a že diferenciační kapacita PEC může být klíčovým prvkem pro regresi diabetické nefropatie, která může být farmakologicky modulována.
Regulátory glomerulárních progenitorů v patologii: Když je orchestr rozladěnýZatímcoledvinovéprogenitory mohou řídit regeneraci podocytů po poranění [4], mohou také vytvářet extrakapilární proliferativní léze nebo srpky, které jsou charakteristickým znakem jak zánětlivých, tak nezánětlivých glomerulárních onemocnění [42]. Důkazy v experimentálních modelech [15] a v lidských biopsiích skutečně naznačují, že srpky se skládají zledvinovéprogenitory [14], které abnormálně posouvají své reakce z reparativních na poškozující. Není zcela pochopeno, které faktory jsou zodpovědné za naklánění váhy. CGN je nejlépe charakterizované onemocnění, u kteréholedvinovéhlavními viníky jsou předci. Buněčný půlměsíc je typická morfologická změna pozorovaná u CGN. Je definována jako vícevrstvé nahromaděníledvinovéprogenitory a další typy buněk v Bowmanově prostoru. V důsledku toho uzavírá vývod moči a proudění primární moči a později je postižený nefron narušen. Prasknutí glomerulárních kapilár při srpkovité chorobě vede k expozicirenal progenitory k vysoké koncentraci plazmy, která dramaticky zvyšuje proliferaci člověkaledvinovéprogenitory v kultuře [43]. Za tvorbu srpku může odpovídat několik složek plazmy, ale v současné době existují konzistentní údaje pouze pro aktivaci fifibrinogenu, který je členem aktivované koagulační kaskády při poranění cév. Nedostatek fifibrinogenu nebo fifibrinolýza brání tvorbě srpku u několika modelů hlodavců [43,44].

Pocházejí také kolapsová nefropatie a pseudoměsíčkyledvinovéprogenitory [14]. Na rozdíl od srpků bylo navrženo, že pseudoměsíčky pocházejí zledvinovéprogenitory jako dysregulovaná odpověď na masivní a rychlé odloučení podocytů, ke kterému dochází za určitých podmínek přímého poškození podocytů (jako je expozice určitým lékům, imunitně zprostředkované poruchy nebo infekce, které přímo cílí na podocyt), ke kterému dochází v nepřítomnosti zánětlivých složek a vede k kolaps kapilár [22,45]. Tyto léze jsou také často pozorovány u virových glomerulopatií, jako je HIV- a parvovirová nefropatie [22]. U těchto virových glomerulopatií interferon (IFN-)- a IFN- nejenže spouští lokální zánět uvnitř glomerulu, ale také působí na PEC a podocyty, přičemž IFN- inhibuje migraci PEC a oba potlačujeledvinovédiferenciace progenitorů na podocyty in vitro [46]. In vivo na modelu adriamycinové nefropatie injekce buď IFN- nebo IFN- zhoršovala proteinurii a glomerulosklerózu [46]. Nedávno byl popsán kolabující FSGS u pacientů nedávného afrického původu s vysoce rizikovým genotypem APOL1 a infikovaných koronavirem těžkého akutního respiračního syndromu 2 (SARS-CoV-2) [47,48]. Bylo navrženo, že SARS-CoV-2 by mohl přímo infikovat podocyt [49] a/nebo spustit zánětlivou kaskádu, která zahrnuje aktivaci interferon-chemokinové dráhy, která naopak interaguje s variantním genem APOL1 [ 50]. Jak je uvedeno výše,ledvinovédiferenciace progenitorů na podocyty je spojena s expresí APOL1, a proto by se mohla podílet na nefropatii spojené s onemocněním koronaviru 2019 (COVID-19).
Několik nedávných studií zdůraznilo kritickou roli pro de novo expresi CD9 a následně CD44 jako patogenního přepnutí PEC z klidového na aktivovaný fenotyp u CGN a u FSGS [16,51,52], což potvrzuje patogenní roli PEC u těchto onemocnění a nabízí nové molekulární cíle pro terapii glomerulárních onemocnění. Na podporu této myšlenky Kaverina et al. ukázali, že PEC ztrácejí expresi CD44 při diferenciaci na podocyty v poraněných glomerulech starých myší, což naznačuje, že zvýšení PEC CD44 nepředstavuje regenerační, ale patologický přechod [53]. Ve FSGS se ukázalo, že CD44 hraje důležitou roli v migraci buněk směrem k poraněné fifiltrační bariéře, kde poraněné podocyty upregulují migrační inhibiční faktor (MIF) a faktor 1 odvozený ze stromálních buněk (SDF1), které stimulují expresi CD44 a CD{{12} }zprostředkovaná migrace [54]. Kromě toho PEC produkovaly izoformy proteinů extracelulární matrix jak odvozené od PEC, tak specifické pro podocyty způsobem závislým na CD 44- [55]. Nakonec studie sledování linií PEC naznačila, že se CD44 neúčastnilledvinaregeneraci prostřednictvím diferenciace na podocyty a účastnily se pouze profifibrotické dráhy [56].
Trubkové progenitory
Renálníprogenitory z parietální epiteliální vrstvy Bowmanova pouzdra mohou potenciálně regenerovat proximální tubulární epiteliální buňky v glomerulotubulární junkci [57]. Nicméně tubulární progenitory rozptýlené v proximálních a distálních tubulech existují také u lidí [6,58–60] a u myší [5,61–63] a zvyšují se po tubulárním poranění u pacientů postižených akutním nebo chronickým tubulárním poškozením [6 ]. Kumar a kol. provedli liniové sledování vzácných buněk exprimujících Sox9-v proximálním tubulu a identifikovali je jako domnělou tubulární progenitorovou populaci účastnící se postakutníchporanění ledvin(AKI) zotavení [64]. Sox9 je transkripční faktor, který vledvinavývoj, řídí větvení epitelu a je exprimován v prekurzorech nefronů [64,65]. Je zajímavé, že když byl Sox9 vyřazen ze segmentů S1 a S2, došlo k pomalejší obnově fyziologickýchrenální funkce, zvýšené tubulární poranění, stejně jako zvýšenéledvinovédošlo k fibróze [64]. Po parciální nefrektomii buňky Sox9 plus proliferují a vytvářejí epiteliální buňky proximálního tubulu, Henleovy kličky, distálního tubulu, sběrného kanálku a parietální vrstvy glomerulu [66]. Nedávno Lazzeri et al. poskytl důkaz, že tubulární progenitory podléhají mitóze a nahrazují přibližně polovinu nevratně ztracených tubulárních buněk během AKI [5]. Provedením sledování linie buněk Pax2 plus na myším modelu tubulárního poškození identifikovali tubulární progenitory jako odlišnou tubulární buněčnou subpopulaci, která byla odolná vůči smrti a vykazovala vysokou klonogenní aktivitu, což vedlo ke generaci segmentů dlouhých tubulů [5].
Regulátoři tubulární progenitorové fyziologie: Polyfonní sbor
Člověkledvinovéprogenitory exprimují B lymfom Mo-MLV (Moloney virus myší leukémie) inzerční oblast 1 (Bmi-1) [57]. Bmi-1 je členem rodiny transkripčních represorů polycomb. Podílí se na regulaci buněčného cyklu a stárnutí kmenových buněk endogenních pro různé orgány, jako je prostata, tenké střevo a plíce [67–70]. Vledviny, hladiny BMI-1 rychle vzrostly po zranění na myším modelu AKI [71]. Tato zjištění ukazují na zapojení Bmi-1 exprimovaného v tubulárních progenitorechledvinovéregenerace. Opravdu, Lv a kol. ukázali, že akutní tubulární nekróza vedla ke zvýšení Bmi-1 a následné mobilizaci tubulárních progenitorů u myší divokého typu, zatímco tubulární progenitory nebyly mobilizovány u Bmi-1 knockout myší [72]. Bmi-1 knockout myši vykazovaly silnéledvinovéfenotyp, včetně intersticiální fibrózy, tubulární atrofie a závažnéledvinovédysfunkce se sníženou buněčnou proliferací, zvýšenou buněčnou apoptózou a senescencí a zánětlivou buněčnou infifiltrací [72,73]. V nedávné studii Zhou et al. dále objasnil roli Bmi-1 vledvinovéprogenitorů, což ukazuje, že Bmi-1 si zachovalo sebeobnovu a kmenledvinovéprogenitory udržováním redoxní rovnováhy a prevencí zástavy buněčného cyklu prostřednictvím inhibice reaktivních forem kyslíku (ROS), p16 a p53 [74].
Další důležitou molekulou zapojenou do regulace tubulárního progenitoru je Toll-like receptor 2 (TLR2), neboli CD282, evolučně konzervovaný membránový protein, který hraje důležitou roli při rozpoznávání patogenů a aktivaci přirozené imunity. TLR2 působí jako senzor poškození tkáně prostřednictvím detekce molekul molekulových vzorů spojených s poškozením (DAMP) uvolňovaných poškozenými tkáněmi. Aktivace TLR2 vede k aktivaci downstream transkripčních faktorů, které regulují expresi genů pro přežití nebo prozánětlivých cytokinů a chemokinů [75–77]. Sallustio a kol. ukázali, že tubulární progenitory exprimují TLR2, jehož stimulace agonisty napodobujícími zánětlivé mediátory nebo DAMP indukuje masivní sekreci monocytárního chemoatraktantního proteinu-1 (MCP-1), interleukinu 6 (IL-6), interleukin 8 (IL-8) a komplementová složka C3 prostřednictvím aktivace NF-κB (nukleární faktor kappa-light-chain-enhancer aktivovaných B buněk) [59]. Kromě toho stimulace TLR2 modulovala rychlost proliferace a diferenciační kapacitu tubulárních progenitorů, což naznačuje důležitou roli vledvinovéoprava [59]. Následné studie stejné skupiny identifikovaly odlišné sady miRNA specificky exprimovaných v tubulárních progenitorech [78]. Mezi nimi miR-1915 a miR{4}}p regulovaly expresi CD133 a PAX2 a také TLR2. Sallustio a kol. poté rozebral mechanismy obnovy po AKI a našel zásadní roli pro TLR2 vledvinovéregenerace [79]. Zjistili, že po poranění vede snímání poškození TLR2 k sekreci inhibinu-A a dekorinu tubulárními progenitory, které naopak podporují tubulární regeneraci prostřednictvím buněčné proliferace [79]. Tyto dva cytokiny patří k signální dráze TGF- (transforming growth factor-) a podílejí se na regulaci buněčného cyklu, zvýšení buněčné proliferace a inhibici apoptózy [80–84].
Exprese molekul z dráhy Wnt byla popsána u dospělýchledvinovéprogenitory u myší [85] a lidí [86]. Pomocí myšího modelu sledování linie, Rinkevich et al. ukázaly, že jak během homeostázy, tak po poranění dospělí savciledvinyprocházejí segmentově specifickou klonální expanzí z buněk odvozených z WNT responzivních prekurzorů [63]. Navrhli, že schopnost reagovat na signály WNT vybírá buňky, které nakonec provedou robustní klonální expanzi. Studie v SIX2 plus z močiledvinovéprogenitory naznačily, že aktivace dráhy WNT inhibicí GSK3 indukuje diferenciaciledvinovépředchůdci do ledvinovéepiteliální proximální tubulární buňky [87]. Kromě toho Wnt3 vykazoval proregenerační účinky a byl upregulován v CD133 plusledvinovéprogenitory v in vitro modelu poškození cisplatinou [88]. V této studii autoři odhalili funkční roli samotného CD133 v renální tubulární reparaci prostřednictvím udržování proliferativní odpovědi a kontroly stárnutí tím, že působí jako permisivní faktor pro -catenin signalizaci, bránící jeho degradaci v cytoplazmě [88]. V zebrafifishledviny,poškozené tubuly byly nahrazeny novými nefrony zledvinovéprogenitory exprimující Wnt receptor frizzled9b a transkripční faktor lefl. Po poranění byla u zraněných indukována exprese Wnt ligandů Wnt9a a Wnt9bledvinyv místech, kde progenitorové buňky tvoří nové nefrony [89]. Tyto výsledky naznačují, že zásadní role signální dráhy Wnt/frizzled vledvinaregenerace je mezi druhy vysoce konzervovaná.

CISTANCHE ZLEPŠÍ ONEMOCNĚNÍ LEDVIN/RENÁL
Jak již bylo zmíněno, signalizace Notch je evoluční konzervovaná dráha, která má kritickou roliporanění ledvina opravy [24,90–93], zejména během AKI [94,95]. Kang a kol. ukázal, že Sox9 plusledvinovéprogenitory exprimovaly vysoké hladiny Notch a nadměrná exprese intracelulární domény Notch1 (NICD1) v populaci Sox9 plus zlepšilaledvinovéhistologie v modelu AKI indukovaném kyselinou listovou [62]. Ma a kol. uvedli, že aktivace Sox9 plus renálních progenitorů, jejichž role je zásadní vledvinaoprava, byla zprostředkována cestou Notch, což potvrzuje předchozí zprávu, že hladiny exprese Notch1-3, Jagged1/2, Dll4 a Sox9 se zvyšují po ischemicko-reperfuzním poškození (IRI) [66]. V jiných orgánech, jako je pankreas, aktivace Sox9 moduluje dráhu Notch regulací Hes1, aby se udržela zásoba progenitorových buněk [96]
U několika léků bylo prokázáno, že se zlepšilyledvinaregenerace a mezi nimi mohou být slibnou terapeutickou možností pro léčbu AKI inhibitory histondeacetylázy (HDAC) (HDACis) [97–102]. HDAC tvoří skupinu enzymů zapojených do mnoha buněčných procesů odstraněním acetylové skupiny z histonových nebo nehistonových proteinů [103]. Marumo a kol. zaznamenali snížení aktivity HDAC5, zvýšenou acetylaci histonů a reaktivaci kostního morfogenetického proteinu 7 (BMP-7) v proximálních tubulárních buňkách během fáze zotavení poledvinovéIRI [104]. Tato pozorování naznačují, že HDAC mohou uplatňovat své příznivé účinky naledvinovézotavení díky zvýšené expresi BMP-7, proteinu, který udržuje zásobu renálních progenitorů v nediferencovaném stavu běhemledvinavývoj [105]. Zajímavé je, že léčba HDACis rozšířilaledvinovépopulace progenitorových buněk u zebrafifish [106]. V modelu nefrotoxické sérové nefritidyglomerulonefritida u myší, aktivovaná léčba trichostatinem A (TSA).ledvinavedlejší populace (SD) buňky [107]. SD buňky tvoří podskupinu buněk s multilineárním potenciálem a známými renoprotektivními vlastnostmi, které oslabují chronickénemoc ledvin(CKD) prostřednictvím zvýšení exprese BMP-7 [107]. Pomocí výše popsaného přístupu sledování linie Lazzeri et al. prokázali, že léčba dvěma široce používanými HDAC, TSA a 4-fenylbutyrátem (4-PBA), vedla k proliferaci Pax2 plus progenitoru, čímž se zabránilo rozvoji tkáňové fibrózy a CKD [5]. Vývoj selektivních HDAC se zvýšenou účinností a nižší toxicitou by se zlepšilledvinazotavení prostřednictvím tubulární proliferace progenitorů. Je třeba poznamenat, že HDAC prokázaly příznivé terapeutické účinky v mnoha experimentálních modelechonemocnění ledvinkromě AKI, včetně glomerulosklerózy, tubulointersticiální fibrózy, glomerulárního a tubulointersticiálního zánětu, lupusové nefritidy, polycystickýchnemoc ledvinaledvinovébuněčný karcinom (RCC), jak je uvedeno v [108]. Několik HDAC je v současné době ve fázi 1 nebo 2 studií pro léčbu RCC a renálního poškození (clinicaltrial.org).
Regulátory tubulárních progenitorů v patologii: A Cacophonus Choir
Biologické a molekulární vlastnostiledvinarakovina tomu nasvědčujeledvinovéprogenitory by mohly být na počátku vývoje různýchledvinatypy nádorů. V nedávné studii Peired et al. ukázal toho člověkaledvinovéprogenitory nadměrně exprimující NICD1 měly zvýšenou proliferační kapacitu a tvoří aberantní mitózu ve 2D kulturách a mohly generovat nádorovou hmotu ve 3D kulturách [8]. Podobně Pax2 plusledvinovéprogenitory nadměrně exprimující NICD1 po indukci transgenu u dospělých myší nebo po IRI byly původem papilárních adenomů a RCC [8]. V potvrzení tohoto zjištění vedla léčba blokující endogenní aktivaci NOTCH1 indukovanou AKI k rozvoji menšího počtu nádorů [8]. Nedávno dvě studie naznačily, že angiomyolipomy pocházejí z multipotentníchledvinaepiteliální buňky lokalizované v tubulu a podstupující klonální expanzi v reakci na deleci genu komplexu tuberózní sklerózy (TSC) [109,110]. Obě studie navrhovaly, aby tyto buňky mohly býtledvinovéprogenitory s víceliniovou diferenciační kapacitou [109,110]. Zajímavé je, že Cho a kol. odhalila, že aktivace dříve nehlášené regulační smyčky Rheb-Notch-Rheb, ve které je klíčovou událostí cyklická vazba Notch1 na prvky reagující na Notch (NRE) na promotoru Rheb, byla hlavním mechanismem za generováním více linií přítomných u angiomyolipomu [109]. Celkově vzato tyto výsledky naznačují, že deregulace dráhy Notch vledvinovéprogenitory mohou vést kledvinovépatologií.
Wan a kol. pozorovali, že exprese SOX9 byla upregulována u pacientů s RCC a korelovala s pokročilým patologickým stupněm [111]. Pacienti s RCC s vysokými hladinami SOX9 měli také kratší přežití [111]. Tato data potvrdila předchozí studii, která spojovala expresi SOX9 s RCC Fuhrmanovým gradingem, a ukázala, že pacienti se SOX9 ( ) měli mnohem lepší terapeutickou odpověď na inhibitory tyrozinkinázy než pacienti se SOX9 ( plus ) [112]. Proto bychom mohli předpokládat, že zvýšení exprese SOX9 v SOX9 plusledvinovéprogenitory by mohly přispět k rozvoji RCC. Podobný mechanismus byl popsán u bazálního karcinomu prsu, kde exprese SOX9 v luminálních kmenových/progenitorových buňkách mohla řídit plasticitu linie pro rakovinu prostřednictvím aktivace signalizace NF-κB [113].
Výhled do budoucnosti renálních progenitorů
Sekvenování jednobuněčné RNA: Nechte nás sladit se s dobouRychlý vývoj scRNAseq otevírá nové perspektivy pro rozbor molekulárních procesů, které jsou součástíledvinovéprogenitorová regulace ve fyziologických a patologických stavech. ScRNAseq spočívá v získání profilování genové exprese v rozlišení jedné buňky, což dokazuje různé buněčné stavy a molekulární dynamiku dokonce i vzácnějších subpopulací. Tato nová technologie byla úspěšně použita v několika orgánech – například ke studiu Promininu 1 plus jaterních progenitorů [114], Dach1-downregulovaných lymfoidních progenitorů [115] a KTR5 plus plicních progenitorů u pacientů s COVID-19 [116]. Během několika posledních let stále větší počet výzkumných skupin aplikoval tuto strategii k definování buněčných populacíledvinyu myší a lidí [117–120]. Ve velmi nedávné studii Rudman-Melnick et al. identifikovali transkripční podpis všech buněčných populací v experimentálním modelu AKI, přičemž zdůraznili přítomnost dříve nepopsaných molekul souvisejících se zraněním [119]. Takový přístup by mohl potenciálně odhalit nové mechanismy aktivované vledvinovéprogenitory po AKI, což vede k identifikaci potenciálních molekulárních cílů. Ve své základní práci Young et al. byli schopni přiřadit jasné buňky a papilární RCC buňky k podtypu proximálních stočených tubulárních buněk definovaných expresí SLC17A3 a VCAM1 [117]. Jak již bylo zmíněno dříve, exprese VCAM1 nebo CD106 charakterizuje spolu s CD133 vzácnou populaciledvinovéprogenitory rozptýlené většinou v proximálním tubulu [6]. Analýza dat scRNAseq odhalila, že transkriptom lidského renálního progenitoru vykazuje podobnosti s PT1, domnělou buňkou původu lidského papilárního RCC [8]. Tato pozorování potvrzují naši hypotézu, že papilární RCC pochází z Notch zprostředkované transformace a proliferace populace proximálních tubulů renálních progenitorů [8].
Klinické aplikace: Klinika volá Tune
Renální progenitorové terapie představují slibnou novou hranici v léčběonemocnění ledvin, jak několik studií naznačuje, že se zlepšujífunkce ledvinpo zranění [121]. Nicméně injekceledvinovéprogenitorů přímo do zvířecích modelůporanění ledvinindukce regenerace tkáně představuje důležitá omezení, která byla odhalena jinde [121]. Tyto výhrady bylo možné obejít díky nově využívaným vlastnostemledvinovéprogenitory, což je jejich schopnost vylučovat trofické faktory, cytokiny nebo chemokiny, které účinně zprostředkovávajíledvinaopravit parakrinním nebo autokrinním způsobem (obrázek 2). Kenji a kol. uvedli, že intraperitoneální injekce kultivačního supernatantu získaného od dospělých potkanůledvinaprogenitory významně potlačily apoptózu tubulárních buněk reziduálníchledvinovébuňky, zmírnily zánět a podpořily proliferaci nezralých buněk v experimentálním modelu IRI prostřednictvím uvolňování HGF (hepatocytový růstový faktor), EGF (epidermální růstový faktor), TGF- a Epo (erytropoetin) [122]. Uvádí se, že terapeutické použití mnoha růstových faktorů se skutečně zlepšiloporanění ledvin, jako jsou HGF, BMP7, EGF, TGF- a VEGF (vaskulární endoteliální růstový faktor) [123–127]. Sallustio a kol. oznámil, že člověkledvinovéprogenitory nejenže významně opravují poškozené tubulární buňky, ale také vykazují antififibrotické účinky prostřednictvím sekrece CXCL6 (chemokinový ligand 6 motiv CXC), SAA2 (sérový amyloid A2), SAA4 (sérový amyloid A4) a BPIFA2 (BPI (baktericidní permeabilita -vzrůstající) člen rodiny A obsahující 2) prostřednictvím parakrinního mechanismu [128]. Aggarwal a kol. oznámil, želedvinovéprogenitorová sekrece limitů Epoledvinovéfifibróza po tubulárním poranění [129]. Kromě rozpustných faktorů vylučují renální progenitory extracelulární vezikuly (EV), částice ohraničené lipidovou dvojvrstvou o velikosti nanometrů nesoucí bioaktivní lipidy, proteiny a RNA, které umožňují komunikaci mezi buňkami prostřednictvím parakrinních akcí. Nejmenším a nejlépe popsaným typem EV jsou exozomy, které byly nedávno zkoumány pro své ochranné účinky proti AKI vyvolané IRI [130,131]. Li a kol. prokázali, že exozomy odvozené z renálního progenitoru by mohly obnovit renální struktury a funkce prostřednictvím svých imunomodulačních, antiapoptotických a proliferačních stimulačních schopností v modelech AKI. MikroRNA (miRNA) byly nejhojnějšími složkami exozomů a mezi nimi byla miR-146a identifikována jako klíčový hráč ve zprostředkování cytoprotektivních účinků downregulací IRAK1 (kináza 1 spojená s receptorem interleukinu 1)/NF-kB signalizace [130]. V modelu diabetické nefropatie bylo zjištěno, že exozomy vylučované močovým progenitorem snižují apoptózu podocytů potlačením kaspázy-3 a podporou vaskulární regenerace, což může souviset s cytokiny VEGF, TGF- 1, angiogeninem a BMP -7 obsažené v exozomech odvozených z močového progenitoru [132]. Inhibice apoptózy podocytů také souvisela s nadměrnou expresí miR-16-5p v exozomech sekretovaných močovým progenitorem supresí VEGF-A [133].
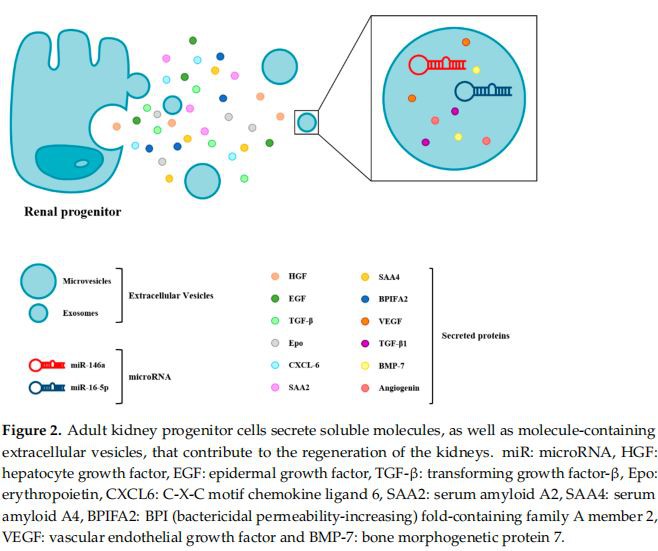
Molekuly a exozomy vylučovanéledvinovéprogenitory podporují zotavení znemoc ledvindíky jejich schopnosti uplatňovat řadu renoprotektivních a regeneračních účinků díky jejich snížené imunitě a nižšímu riziku maldiferenciace a tumorogeneze ve srovnání s buněčnými terapiemi. Tyto pozoruhodné vlastnosti je činí přitažlivými pro klinické aplikace. Další výzvou v klinickém přístupu knemoc ledvinje objev nových nástrojů pro diagnostiku a monitorovánínemoc ledvinkteré by byly snadno dostupné neinvazivními postupy. V tomto kontextu představuje moč cennou biotekutinu díky své dostupnosti, rychlému a snadnému odběru vzorků a široké rozmanitosti proteinů, metabolitů, buněk a buněčného obsahu uvolňovaného z urogenitálního traktu [134]. Přítomnost buněk v moči, které vykazují vlastnosti kmenových buněk, byla poprvé popsána Zhangem et al. v roce 2008 [135]. V následujících letech několik skupin vyvinulo techniky k izolaci a charakterizaci progenitorů pocházejících z moči od zdravých dárců a pacientů sledvinaporuchy [136]. Dosud nebylo dosaženo žádného formálního konsenzu o tom, jaké markery lze použít k definování progenitorů pocházejících z moči. Většina studií ukázala, že exprimují markery mezenchymálních kmenových buněk (CD44, CD73 a VIM) a markery kmenových buněk (jako POU5F1, SSEA4 a TRA-1-81, stejně jako CD117), ale žádné markery odvozené z krvetvorby nebo urotelu buněčné linie a nízké hladiny tubulárních nebo podocytově specifických markerů [136]. Pokud jde o jejich původ, Bharadwaj et al. ukázal, že pochází z močiledvinovéprogenitory nesly chromozom Y mezi muži a ženamitransplantace ledvinpříjemce s uvedením, že pocházejí zledviny[137]. Tyto buňky mají schopnost diferencovat se na podocyty [138] a exprimovat proteinové markery specifické pro podocyty a PEC [137,139], což naznačuje, že pocházejí z PEC. Srovnávací transkriptomová analýza z močiledvinovépředchůdci aledvinapocházející z biopsieledvinovéepiteliální proximální buňky potvrdily identitu renálních progenitorů progenitorů pocházejících z moči [87], což naznačuje, že mohou také pocházet z rozptýlených tubulárních progenitorů. Tyto buňky lze přeprogramovat na indukované pluripotentní kmenové buňky (iPSC) a použít je pro regenerativní medicínu, modelování onemocnění nebo farmakologické testování [140,141].
Nedávno bylo navrženo, aby výrazledvinovéprogenitorový marker CD133 v urinárních EV představuje dobrý marker pro hodnocení funkčního stavu renálního tubulárního kompartmentu a přítomnosti buněk s proliferativní a reparační aktivitou v tubulech po poranění. Dvě studie skutečně uvedly, že hladiny CD133 plus EV v moči, zvýšené u zdravých subjektů, nejen klesají u pacientů s akutním tubulárním poškozením [142], ale také u akutních a chronických glomerulárních onemocnění [143]. Kromě toho přítomnost samotných renálních progenitorů v moči může odrážet patofyziologický stavledvinovétkáň. Zejména Manonelles et al. poskytl důkaz, že izolace CD133 plus CD24 plus renálních progenitorů z moči stabilních příjemců aloštěpu po šesti měsících by mohla předpovědět špatný dlouhodobý výsledek transplantace po dvou letech [144]. Proliferace a migrace renálních progenitorů z Bowmanova pouzdra do glomerulárního chomáču přes močový prostor za účelem nahrazení odloučených podocytů by mohla vysvětlit vylučování renálních progenitorů, a pokud se udrží v průběhu času, může selhat při zachování funkce aloštěpu, což má za následek pokles GFR, albuminurie a vývoj chronické glomerulární histologické léze [144].
Pocházející z močiledvinabuňky by také mohly být mocným personalizovaným nástrojem pro funkční studie na kandidátních variantách v dědičnostinemoc ledvin. Jak popsal Lazzeri et al., pocházející z močiledvinovéprogenitory získané od pacientů nesoucích patogenní mutace v genech kódujících proteiny podocytů expandují v kultuře, ale po diferenciaci podocytů se u nich vyvinou anomálie v expresi nebo lokalizaci proteinů podocytů [138]. V souladu s tímto důkazem byla stejná technika použita k prokázání patogenity varianty genu NPHS1 neznámého významu u pacienta s refrakterní lupusovou nefritidou [145]. Další studie zdůraznila možnost použít renální epiteliální buňky získané z moči k provedení RNA a funkčních studií naledvina-specifické geny, ověřující patogenitu synonymní varianty v PKHD1 (polycystickýledvinaa onemocnění jater 1) a potvrzení genetické diagnózy ARPKD (Autosomal Recessive PolycysticNemoc ledvin) u pacienta s CKD spojeným s atypickou polycystouledviny [146].
Závěry
Obrovské množství literatury popisuje četné mechanismy regulaceledvinovéprogenitorů v glomerulárních a tubulárních kompartmentech, což nám umožňuje mít globální představu o složitosti molekulárních procesů probíhajících za fyziologických a patologických podmínek. Znát molekulární podpisledvinovéprogenitorů otevírá dveře k identifikaci nových cílů, které mají drogy udržetledvinaregeneraci nebo biomarkery ke sledováníledvinazdraví.
