Diagnostický biomarker pro diabetické onemocnění ledvin: Exprese mikroRNA
Mar 26, 2022
Kontakt:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
ČÁST I.: Profilování exprese mikroRNA u diabetického onemocnění ledvin
HIROKIISHII, SHOHEI KANEKO, KATSUNORI YANAl, AKINORI AOMATSU, KEIJ HIRAl, SUSUMU OOKAWARA A YOSHIYUKI MORISHITA
ÚVOD
Prevalence diabetického onemocnění ledvin (DKD) celosvětově rychle roste a souvisí se značnou ekonomickou a sociální zátěží, protože je hlavní příčinou konečného stadia onemocnění ledvin a je spojena s rozvojem různých vaskulárních komplikací1. Zlepšit prognózu DKD(diabetické onemocnění ledvin), je nutná jeho včasná diagnóza a specifické léčebné látky. Obojí však nebylo stanoveno.
Definitivní diagnóza DKD (diabetické onemocnění ledvin) vyžaduje histologickou analýzu renálních biopsií. Renální biopsie je však invazivní, je obtížné získat diagnostické vzorky a není vhodné pro opakované postupy. Proto bylo několik molekul séra nebo moči, jako je kolagen IV, COOH-terminální propeptid kolagenu VI a receptor faktoru nekrózy nádorů 1 ze 2, hodnoceno pro použití jako diagnostické markery DKD(diabetické onemocnění ledvin),2-4ale žádný z nich se dosud nestal zavedeným pro klinické použití.5-7
Pokud jde o léčbu DKD(diabetické onemocnění ledvin)bylo prokázáno, že několik léků, jako jsou blokátory systému renin-angiotensin, inhibitor kotransportéru sodíku a glukózy 2 a analogy peptidu-1 podobného glukagonu, mají ochranné účinky v DKD(diabetické onemocnění ledvin),8-10ale žádné nejsou ideální. Existuje tedy naléhavá potřeba identifikace diagnostických biomarkerů a terapeutických činidel pro DKD(diabetické onemocnění ledvin).
MikroRNA(miRNA)přitahují pozornost jako biomarkery specifické pro onemocnění a terapeutické cíle pro různá onemocnění, jako je rakovina a několik zánětlivých onemocnění.11,12miRNA(MikroRNA) jsou malé, nekódující RNA o délce přibližně 22 nukleotidů, které působí jako posttransskripční regulátory cílových genů a jejich odvozených proteinů indukcí degradace messenger RNAmiR a/nebo translační represe.13,14Předpokládá se, že NUS jsou zodpovědné za regulaci >60% všech úrovní exprese proteinů, čímž hrají klíčovou a různorodou roli v patofyziologických procesech u různých onemocnění.15.
Předchozí studie ukázaly, že několik miRNA(MikroRNA)se podílejí na patogenezi DKD(diabetické onemocnění ledvin), a v důsledku toho mohou představovat užitečné biomarkery nebo terapeutické cíle pro DKD(diabetické onemocnění ledvin).16.17Další studie zkoumající regulační úlohu miRNA(MikroRNA)v DKD(diabetické onemocnění ledvin)jsou nezbytné a tyto miRNA(MikroRNA)mohou být vyvinuty jako diagnostické biomarkery a terapeutická činidla pro DKD(diabetické onemocnění ledvin). Proto jsme v této studii zkoumali miRNA(MikroRNA)zapojený do DKD(diabetické onemocnění ledvin)a určil jejich potenciál jako specifických biomarkerů nebo terapeutických činidel pro DKD(diabetické onemocnění ledvin).
cistanche kmenové výhody
MATERIÁL A METODY
Zvířecí model.Myši byly umístěny v místnosti s řízenou teplotou a vlhkostí za antivirových podmínek a mikroizozolátorů bez protilátek. Samci db/db myší (C57BLKS/J lar -+Leprdb/+Leprdb) a jejich normální vrh m/m myší (C57BLKS/J Iar-m+/m+) byly zakoupeny od Institutu pro reprodukci zvířat (Ibaraki, Japonsko). Samci myší AKITA (myši C57BL/6-Ins2Akita/J) a jejich normální sourozenci (C57BL/6J) byli získáni od společnosti Japan SLC, Inc. (Tokio, Japonsko).
Renální ischemie a reperfuze byly provedeny tak, jak bylo popsáno výše.18Stručně řečeno, samci myší C57BL/6J (Tokyo Laboratory Animals Science, Tokio, Japonsko) byli anestetizováni isofluranem a byl identifikován pravý renální pedikulován, ligován a provedena pravá nefrektomie. Levý renální pedikul byl poté identifikován a upnut netraumatickým mikrovaskulárním klipem po dobu 45 minut. Svorky byly odstraněny po skončení období ischemie a úspěšná reperfuze byla vizuálně potvrzena. Falešně operované myši podstoupily stejný chirurgický zákrok bez upnutí renálního pedikulu. Zvířata byla obětována 24 hodin po reperfuzi.
Jednostranná ureterická obstrukce byla provedena, jak bylo dříve hlášeno.19Stručně řečeno, samci myší C57BL / 6J (Tokyo Laboratory Animals Science) byli anestetizováni pomocí isofluranu a pak byl levý močovod vystaven břišnímu řezu střední čáry, zcela ligován 4-0 hedvábím ve dvou bodech a rozdělen mezi ně. Falešně operovaná skupina nepodstoupila ligaci. Myši byly obětovány a jejich ledviny byly odebrány 7 dní po operaci.
Samci myší akcelerovaných senescencí (SAMP1/YitFcsJ) a kontrolních myší (SAMR/YitFcsJ) byli zakoupeni od SLC Japan.20Tyto myši byly obětovány ve věku 48 týdnů. Samci myší HIGA (HIGA/NscSlc) a balb/cCrSlc myší, které byly vybrány jako kontrolní kmen kvůli jejich nízkým sérovým koncentracím IgA, byly získány z Japonska SLC.
Byly odebrány ledviny a krev, získáno sérum a většina tkání byla skladována při teplotě -80 °C. Levé ledviny byly použity pro histologickou analýzu a pravé ledviny pro mRNA a miRNA(MikroRNA)kvantifikace. Pro biochemické analýzy byly myši převezeny do jednotlivých metabolických klecí pro sběr 24hodinových vzorků moči. Koncentrace albuminu a kreatininu v moči byly měřeny pomocí LBIS Mouse Urinary Albumin Assay Kit (typ S) (Fujifilm Wako, Shibayagi, Gunma, Japonsko) a Lab-Assay Creatinine Kit (Fujifilm Wako, Osaka, Japonsko).
Pacienti a zdraví jedinci.Přijali jsme pacienty s chronickým onemocněním ledvin, kteří podstoupili renální biopsii na Saitama Jichi Medical University mezi květnem 2016 a květnem 2019. Do DKD bylo přijato dvacet pět pacientů(diabetické onemocnění ledvin)a byli srovnáváni s pacienty, kteří měli jiné onemocnění ledvin než DKD (n = 50 pacientů; IgA nefropatie 17, membránová nefropatie 9, minimální změna nefrotického syndromu 6, nefroskleróza 4, intersticiální nefritida 3,nefropatie spojená s IgG4 3, lupus nefritida 2 a další onemocnění ledvin 6) a byly porovnány pro jejich výchozí charakteristiky. Každý případ byl přezkoumán několika zkušenými patology, aby se zajistilo, že vzorky biopsie vykazovaly patologické změny odpovídající kategorii onemocnění a nevykazovaly významné změny charakteristické pro jiné nemoci. Moderátor(diabetické onemocnění ledvin)byla diagnostikována pomocí charakteristických nálezů zvýšení mesangiální matrice, nodulární glomerulosklerózy, difúzního glomerulárního zahuštění bazální membrány a souběžné hyalinózy aferentních a eferentních arteriol.21Diabetes mellitus byl diagnostikován pomocí American Diabetes Association criteeGFR byl odhadnut pomocí diety v renální ria.22Metoda nemocí (MDRD), modifikovaná pro Japonce (ml/min/následující: populace, eGFR,as;1x sérový kreatinin1,73m²)=0,881×186,3×age-0,203× (×0,742 pro ženy).23,24
Analýza mikropolí.Analýza miRNA(MikroRNA)výraz byl proveden Hokkaido System Science (Hokkaido, Japonsko). Podrobnosti o mikropolu analy-sis byly popsány jinde.25Stručně řečeno, RNA byla defosforylace a poté ligována na Cy3-pCp pomocí miRNA(MikroRNA)Kompletní sada etiketovacích činidel a Hyb Kit (Agilent Technologies, CA, USA) a miRNA(MikroRNA)Spike-in Kit (Agilent Technologies). MiRNA(MikroRNA)Kompletní etiketovací činidlo a Hyb Kit byly použity k hybridizaci cRNA.Po hybridizaci byly mikroarové paprsky omyty pomocí Gene Expression Wash Pack (Agilent Technologies) a skenovány skenerem Agilent Microarray. Intenzity signálu byly hodnoceny pomocí Agilent Feature Extraction ver.12.0.3.1.mRNA expresní analýzy byla také provedena Hokkaido System Science. RNA byla označena Cy3 pomocí Low-Input Quick-Amp Labeling Kit, One-Color (Agilent Technologies). Označené vzorky cRNA byly hybridizovány s myší miRNA(MikroRNA)Microarray 8×60K rel.21.0 (Agilent Technologies) při 65 °C po dobu 17 hodin pomocí sady hybridizace genové exprese (Agilent Technologies). Po hybridizaci byla mikropole omyta součástmi Gene Expression Wash Buffers Pack (Agilent Technologies) a naskenována skenerem Agilent Microarray. Intenzity signálu byly vyhodnoceny pomocí Agilent Feature Extraction ver.12.0.3.1.Normalizace byla dosažena pomocí metody posunu 90. percentilu, což je běžně používaná metoda pro mikropole, jak bylo popsáno dříve.26Výsledky byly analyzovány pomocí softwaru GeneSpring v12.1 (Agilent Technologies). Statistická analýza byla provedena pomocí jednosměrné ANOVA s post hoc Tukeyho upřímně významným rozdílovým testem. Sklopné změny s mezní hodnotou>4 a hodnotou P<0.05 were="" considered="" to="" indicate="" statistically="" significant="" differences.="" the="" genespring="" single="" experiment="" analysis="" (sea)bioinformatics="" tool="" was="" used="" for="" computational="" analysis="" to="" identify="" potential="" curated="" canonical="" pathways="" that="" were="" enriched="" in="" the="" transcript="" list="" showing="" a="" significant="" gene="" expression="" difference="" between="" the="" control="" mice,db/db="" mice,db/db="">(MikroRNA)-181b-5p-mimic-PEI-NPs a db/db myši+control-miRNA(MikroRNA)-PEI-NPs skupiny používající databázi WikiPathways Predicted target. FmRNA miRNA byly prohledávány pomocí softwaru Target Scan.
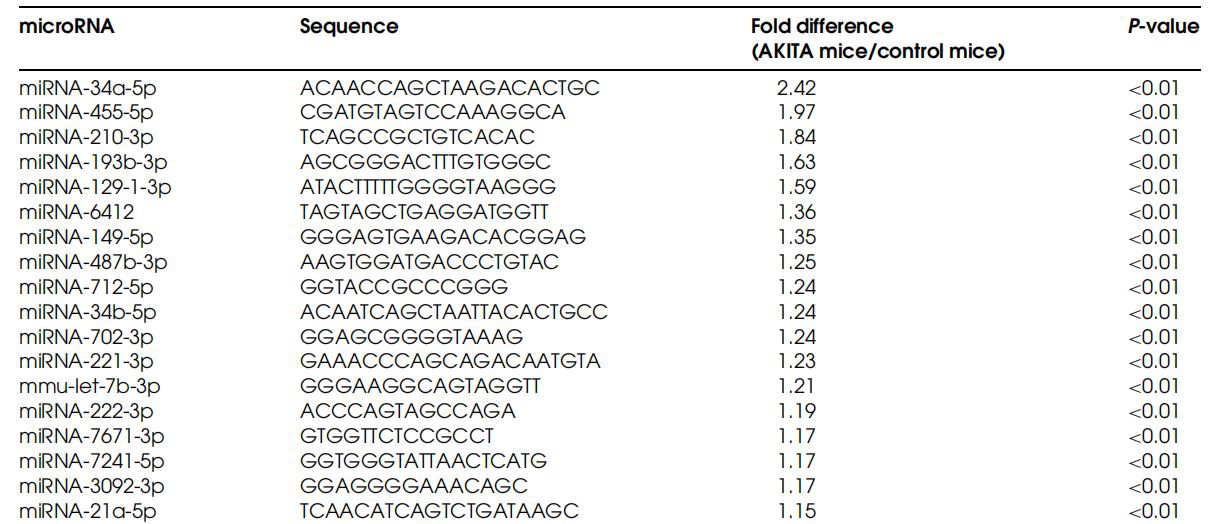
Tabulka I.Seznam miRNA(MikroRNA)diferencovaně exprimované v ledvinách myší AKITA analýzou mikropole
Kvantitativní reverzní transkripce v reálném čase -PCR.Podrobnosti o kvantitativních testech reverzní transkrip-tion-PCR(qRT-PCR) v reálném čase pro měření mRNA a miRNA(MikroRNA)výraz v ledvinách myší byl popsán dříve.27Měření miRNA(MikroRNA)byly vzorky ledvin homogenizovány pomocí skleněného homogenizátoru a drtiče filtrační kolony (kolona drtiče QIA; Qiagen, Hilden, Německo), pak byla RNA extrahována pomocí miRNeasy Mini Kit (Qiagen). Jeden mikrogram každého vzorku RNA byl zpětně přepsán do cDNA pomocí miRScript PCR System (Qiagen). qRT-PCR byl poté proveden pomocí miScript SYBR Green PCR Kit a specifických primerů pro miRNA-20a-5p, miRNA-34a-5p,miRNA-125b-5p,miRNA-129-1-3p, miRNA-129b-5p,miRNA-142a-3p,miRNA-142a-5p, miRNA-181b-5p, miRNA-223-3p,miRNA-146a-5p, rmiRNA-455-5p,miRNA-652-3p,miRNA-342-3p,rmiRNA-6401,a miRNA-6980-5p(miScript Primer Assays; Qiagen), podle pokynů výrobce. Úrovně exprese byly normalizovány na úroveň U6-snuRNA a byly vypočteny jako rozdíly v záhybech (2-△ACT) od normálních úrovní kontrolní exprese. Úrovně exprese U6 se statisticky nelišily mezi všemi skupinami v této studii.
Měření miRNA(MikroRNA)v lidském a myším séru, RNA byla připravena z 300 μl vzorků séra pomocí plazmatické kolony NucleoSpin miRNA (Macherey-Nagel, Duren, Německo) a miRNeasy Serum/Plasma Kit (Qiagen). Poté byla izolovaná RNA zpětně přepsána pomocí miScript I RT Kit (Qiagen).qRT-PCR byl proveden pomocí miScript SYBR Green PCR Kit (Qiagen). Primery pro miRNA-20a-5p,miRNA-34a-5p,miRNA-125b-5p,miRNA-129-1-3p,
Mirna(MikroRNA)-142a-3p,miRNA-1129b-5p,miRNA-142a-5p,miRNA-146a-5p,miRNA-181b-5p,miRNA-455-5p,miRNA-342-3p,n miRNA-223-3p, miRNA-652-3p,miRNA-6401 a miRNA-6980-5p byly zakoupeny od společnosti Qiagen. Hladiny každé miRNA byly normalizovány na hladiny miRNA-16 jako endogenní kontrola. Hladiny sérové exprese miRNA-16a-5p se statisticky nelišily mezi všemi skupinami v této studii.
Pro měření exprese mRNA byly vzorky ledvin homogenizovány pomocí skleněného homogenizátoru a filtračního col-umn drtiče (QIA drtiče; Qiagen). RNA byla izolována pomocí soupravy RNeasy Total RNA Isolation Kit (Qiagen) a 1 μg každého vzorku RNA bylo reverzně přepsáno pomocí systému SuperscriptII First Strand synthe-sis (Life Technologies, MA, USA).qRT-PCR byl proveden pomocí SYBR GreenER qPCR SuperMix (Life Technologies). Primery pro myší kolagen typu I Alpha 1 Chain, kolagen Typu IV Alpha 1 Chain byly zakoupeny od Takara Bio (Shiga, Japonsko). Exprese každé cílové mRNA byla normalizována na expresi beta-aktinu jako referenčního genu.

Obr. 1.Tepelná mapa diferenciálně vyjádřených miRNA(MikroRNA)v ledvinách myší AKITA. Tepelná mapa ukazuje hierarchické shlukování a systémové variace v expresi miRNA(MikroRNA)v ledvinách myší z každé skupiny (n = 4 na skupinu). miRNA zobrazené červeně vykazovaly vysokou expresi a ty, které byly zobrazeny zeleně, vykazovaly relativně nízkou expresi. (Barevná verze fifigure je k dispozici online.)
Příprava miRNA(MikroRNA)-181b-5p napodobuje.Mirna(MikroRNA)-181b-5p a zakódovaná malá RNA (control-miRNA) byly syntetizovány společností Ajinomoto Bio-Pharma Services (Osaka, Japonsko). Sekvence miRNA-181b-5p mimic byla 5'-AACAUUUUGUCGGUGG-GUU-3' a sekvence control-miRNA(MikroRNA)byl 5'-GGUUCGUACGUACACUGUUCA-3'.
Dodávka miRNA(MikroRNA)-181b-5p-PEI-NP do ledvin.Zkoumat účinky miRNA(MikroRNA)-181b-5p mimické ošetření, lineární NP založené na PEI (in vivo jet PEI; Polyplus-transfection,llkirch-graffenstaden, Francie) byly použity, jak bylo popsáno výše.27Stručně řečeno, miRNA(MikroRNA)-PEI-NPs (miRNA∶ 50μg, poměr dusíku (N) v polymeru k fosfátu (P)v nukleových kyselinách = 6) byly rozpuštěny ve 200 μL 5% roztoku glukózy a injikovány do db/db myší ocasní žílou podle protokolu výrobce. Následující skupiny sloužily jako kontroly:(1)normální littermates(m/m),(2) neléčené db/db myši a(3)db/db myši injekčně s control-miRNA(MikroRNA)-PEI-NP používající stejný protokol. Posoudit terapeutický potenciál miRNA-181b-5p pro DKD(diabetické onemocnění ledvin), injekčně jsme injekčně aplikovali miRNA-181b-5p-PEI-NPs nebo control-miRNA-PEI-NPs do 10týdenních db/db myší týdně po dobu 10 týdnů.

Obr. 2.Tepelná mapa diferenciálně vyjádřených miRNA(MikroRNA)v ledvinách db/db myší. Tepelná mapa ukazuje hierarchické shlukování a systémové variace v expresi miRNA v ledvinách každé skupiny (n = 4 na skupinu). Červená, vyšší výraz; modrá, nižší výraz. (Barevná verze fifigure je k dispozici online.)
HistologieFluorescence a jámmunohistochemie.Po disekci ledvin byla reprezentativní část každé ledviny okamžitě fixována v PBS pufrovaném 4% paraformaldehydu a vložena do parafínu. Sekce (5 μm) byly použity pro imunobarvení a periodické kyselé Schiffovo (PAS) barvení. Mesangiální expanze byla hodnocena v PAS obarvených řezech výpočtem mezangiálního indexu (M) podle protokolu Animal Model of Diabetic Com-plications (AMDCC): plocha (počet pixelů) barvení PAS / celková plocha (počet pixelů) glomerulů. INDIKÁTOR chybné funkce byl vypočítán pro nejméně 20 glo-meruli na skupinu (3-4 glomeruly na myš a šest myší s dvojitými vlákny e na skupinu). Cy3-značené oligonukleotidy (Cy3-miRNA(MikroRNA); Takara Bio) byly použity k vyhodnocení renální distribuce intravenózně podané miRNA(MikroRNA)-PEI-NP, jak bylo popsáno výše.27Brifly,Cy3-miRNA(MikroRNA)byl komplexován s PEI-NP a intravenózně injikován do db/db myší, poté byly ledviny odstraněny o 1 hodinu později. Sekce (tloušťka 5 μm) byly inkubovány po dobu 2 hodin při pokojové teplotě fluoresceinem značeným lektinem Lotus tetragonolobus (Vector Laboratories, CA, USA) a DAPI byl použit jako coun-terstain. Úroveň fluorescence byla poté hodnocena fluorescenční mikroskopií (BZ-X710; Keyence, Osaka, Japonsko) a BZ-X_Analyzer software (Keyence). Pro imunochemickou studii byly použity myší mAbs proti kolagenu I (NB600-408, Novus Biologicals, CO, USA) a IV (NB120-6586, Novus Biologicals) a kozí polyklonální sekundární protilátky proti HRP myší a králíků (PI-1000, Vector Laboratories). Vzorky tkáně byly vloženy do Tissue-Tek OCT Compound (Sakura Finetek Japonsko, Tokio, Japonsko) a zmrazeny v tekutém dusíku. Sekce kryostatu (tloušťka 5 μm) byla namontována na skleněná sklíčka potažená silanem (Matsunami Glass Ind, Osaka, Japonsko).
Hybridizace in situ.ISH pro miRNA(MikroRNA)-125b-5p a miRNA-181b-5p byly provedeny pomocí dvojitých digoxigeninem značených miRCURY LNA detekčních sond (Qiagen). Zakódovaná sonda sloužila jako negativní kontrola a U6 sloužila jako pozitivní kontrola. Postup byl proveden podle protokolu výrobce.28Brifly, parafinem vložené části myší ledviny (5-μm) byly deparafinizovány, promyty v PBS a ošetřeny proteinázou K po dobu 10 minut při 37 ° CC. Preparáty pak byly inkubovány lNA-digoxigeninem značenou sondou (40 nM) ve vlhké komoře přes noc při teplotě 60 °C. Po promytí byly řezy přes noc inkubovány antidigoxigeninovou protilátkou konjugovanou s alkalickou fosfatázou při teplotě 4 °C. Poté byly preparáty vyvinuty s použitím nitroblue tetrazoliumchloridu/5-brom-4-chlor-3'-indolyfosfatázy ptoluidinové soli (Life Tech-nologies) přes noc ve tmě při pokojové teplotě. Fotomikrografy byly poté získány pod světelným mikroskopem (BZ-X710; Klíč).
Tabulka II.Seznam miRNA(MikroRNA)diferenciálně exprimované v ledvinách db/db myší analýzou microarray

Schválení studie.Studie byla provedena v souladu se zásadami Helsinské deklarace a byla schválena Etickým výborem Jichi Medical University (schvalovací číslo 17-023, 11. října 2017). Od všech účastníků byl získán písemný informovaný souhlas. Pokusy na zvířatech byly schváleny Etickou komisí pro zvířata Jichi Medical University a byly provedeny v souladu s pokyny pro použití a péči o experimentální zvířata z Příručky Jichi Medical University pro laboratorní zvířata.
Statistika.Data byla analyzována pomocí softwaru JMP (verze 13.0.0; SAS Institute Inc, Cary, NC, USA). Výsledky jsou vyjádřeny jako prostředky ± SD. Průměry byly porovnány pomocí jednosměrné analýzy rozptylu, a pokud existovaly statisticky významné rozdíly, Tukeyho test byl proveden post hoc, aby se porovnaly průměry dvou různých skupin. Pro kategorické proměnné byly rozdíly analyzovány pomocí testu chí-kvadrát. Byla provedena logistická regrese a byly vypočteny AUC. P<0.05 was="" considered="" to="" represent="" statistical="">
KLIKNĚTE ZDE NA ČÁST II. & III.
Zkratky:BMI = index tělesné hmotnosti; DAPI = 4,6-diamidino-2-fenylindol; FITC = fluorescein isothiokyanát; DKD=diabetické onemocnění ledvin; eGFR = odhadovaná rychlost glomerulární fltrace; HDL lipoprotein s vysokou hustotou; HIGA = vysoký imunoglobulin A; IRI = ischemie-reperfuzní poranění; LDL = lipoprotein s nízkou hustotou; ns = nevýznamné; PEI-NPs = polyethyleniminové nanočástice; RNU6 = U6 Malá jaderná 1; SAMP = myš akcelerovaná senescencí; SAMR = ovládací prvek pro myš akcelerovanou senescence; UACR = poměr albuminu ke kreatininu v moči; UUO = jednostranná ureterální obstrukce
cistanche rostlina
Poznámka: Tradiční čínská léčivá bylina cistanche (také známá jako "dračí bylina" a "pouštní ženšen"),roste pouze ve vyprahlých a teplých pouštích. Jako jedna z devíti nesmrtelných bylin, Cistanche (cistanche tubulosa / cistanche deserticola / desertliving cistanche / cistanche salsa) obsah s bohatými účinnými složkami, jako je echinakosid, akteosid, celkové fenylethanoidní glykosidy, flavonoidy, polysacharidy atd. Tyto účinné složky učinily cistanche vzácnou výživnou bylinou a potravinovým materiálem pro imunitu lidí, vnitřní orgány a mozkové buňky a neurony atd. Moderní farmakologické studie potvrdily následující účinky cistanche(přínosy cistanche): zlepšení imunity; zlepšit sexuální funkci a funkci ledvin; proti únavě; proti stárnutí; zlepšit paměť; anti-Parkinsonova nemoc; proti Alzheimerově chorobě; antioxidace; snadnost-zácpa; protizánětlivé; podporuje růst kostí, bělení kůže; chrání játra; atd.

co je to cistanche



