Pohlavní rozdíly u obezity, metabolismu lipidů a zánětů: Role pohlavních chromozomů?
Mar 24, 2022
Kontakt: Audrey Hu Whatsapp/hp: 0086 13880143964 E-mail:audrey.hu@wecistanche.com
Temeka Zore, Maria Palafox, Karen Reue
ABSTRAKTNÍ
Pozadí: Sexrozdíly v obezitě a příbuzných chorobách jsou dobře známé. Gonadální hormony jsou hlavní determinantou těchtosexrozdíly. Pohlavní rozdíly ve velikosti a složení těla jsou však evidentní před expozicí gonadálním hormonům, což poskytuje důkaz pro příspěvky nezávislé na gonadách, které lze připsat komplementu pohlavních chromozomů XX nebo XY. Velké genetické studie odhalily rozdíly mezi muži a ženami v genetické architektuře množství tukové tkáně a anatomické distribuci. Tyto studie však typicky opomíjely chromozomy X a Y.
Rozsah recenze: Zde diskutujeme o tom, jaksexkomplement chromozomů může ovlivnit obezitu, hladiny lipidů a zánět. Anomálie lidského pohlavního chromozomu, jako je Klinefelterův syndrom (XXY), stejně jako myší modely s upravenými změnamisexkomplementu chromozomů, podporují důležitou roli pohlavních chromozomů při obezitě a metabolismu. Zejména modifikace myší Four Core Genotypes sestávající z myší XX buď s vaječníky nebo varlaty a myší XY s vaječníky nebo testovanými, odhalila účinek dávkování chromozomu X na adipozitu, hyperlipidémii a záněty bez ohledu na mužské nebo ženské pohlavní žlázy. . Mechanismy mohou zahrnovat zvýšenou expresi genů, které unikají inaktivaci chromozomu X.
Hlavní závěry: Ačkoli jsou méně prozkoumány než účinky gonadálních hormonů,sexchromozomy mají nezávislé a interaktivní účinky na adipozitu, metabolismus lipidů a záněty. Zejména přítomnost dvou X chromozomů byla spojena se zvýšenou adipozitou a dyslipidémií u myších modelů a u mužů XXY. Může přispět zvýšená exprese genů, které unikají inaktivaci chromozomu X, ale je zapotřebí více práce.
Klíčová slovaGenetika; Gonadální hormony; Tuková tkáň;Sexchromozomové anomálie; inaktivace chromozomu X; Modely myší
k čemu se cistanche používá: zlepšit sexualitu
1. SEXUÁLNÍ DIMORFISMUS PŘI NEMOCI
Studiumsexrozdíly ve fyziologii se prosadily, protože se týkají pochopení rozdílů mezi muži a ženami v náchylnosti k onemocnění. Ženy častěji než muži trpí autoimunitními chorobami (např. systémový lupus erythematodes, sklerodermie, Sjogrenův syndrom), dále osteoporózou, Alzheimerovou chorobou a klinickou depresí [1e6]. Autismus se vyskytuje častěji u chlapců než u dívek a rozdíly mezi pohlavími jsou pozorovány také u neurologických onemocnění, jako je Parkinsonova choroba a schizofrenie, abychom jmenovali alespoň některé [7e9]. U kardiovaskulárních onemocnění a cévní mozkové příhody existují rozdíly mezi pohlavími ve věku nástupu, patologii onemocnění a mortalitě [10].
Nějakýsexrozdíly v lidských onemocněních přímo souvisí s odlišnýmisexkomplementu chromozomů u žen (XX) a mužů (XY). Muži jsou častěji postiženi X-vázanými chorobami, jako je barvoslepost, Duchennova svalová dystrofie a hemofilie. Ženy mohou být chráněny před těmito recesivními poruchami (nebo mohou zažít jejich oslabenou závažnost), protože mají dva chromozomy X [11]. Náhodná inaktivace jednoho chromozomu X v ženských buňkách během raného vývoje umlčí chromozom X nesoucí mutantní gen v přibližně polovině ženských buněk, což umožňuje exkluzivní expresi genu divokého typu v těchto buňkách. Extrémní příklad vlivu genotypu XX versus XY na závažnost onemocnění u Rettova syndromu, který je důsledkem mutace genu MECP2 na chromozomu X. Ženy postižené Rettovými mutacemi pociťují progresivní neurovývojové nedostatky vedoucí k poruchám učení, komunikace, koordinace a dalších mozkových funkcí. Naproti tomu muži s mutacemi MECP2 obvykle umírají in utero nebo v dětství [12].
Zde budeme diskutovat o tom, jaksexkomplement chromozomů může ovlivňovat faktory, které jsou základem metabolických poruch, jako je obezita, dyslipidémie a záněty. Je dobře známo, že gonadální hormony mají silné účinky na ukládání tuku a náchylnost k souvisejícím onemocněním, jako jsou kardiovaskulární onemocnění a diabetes 2. typu [13]. Vzhledem k tomu, že ženské gonády se typicky nacházejí společně s chromozomy XX a mužské gonády s chromozomy XY, nezávislé role gonadálních hormonů asexchromozomy nebyly oceněny. Avšak anomálie lidských pohlavních chromozomů, jako je Klinefelterův syndrom (XXY) a Turnerův syndrom (XO), stejně jako myší modely s upravenými změnami komplementu pohlavních chromozomů, podporují důležitou roli pohlavních chromozomů při obezitě a metabolismu.
2. POHLAVÍ ROZDÍLY V LIDSKÉ ADIPOSitě A OBEZitě
Tuková tkáň slouží jako efektivní zásobárna energie. Má také aktivní roli při příjmu mastných kyselin z cirkulujících lipoproteinů produkovaných v reakci na jídlo a při regulovaném uvolňování mastných kyselin pro použití jinými tkáněmi mezi jídly nebo během fyzické aktivity. Mezi muži a ženami jsou klíčové rozdíly v distribuci tukové tkáně, přičemž muži akumulují větší množství viscerální tukové tkáně a ženy mají typicky větší akumulaci tuku v subkutánních (glutealfemorálních) zásobnících [14,15]. Pohlavně specifická distribuce tuku je ovlivněna několika faktory, včetně stravy a hormonálního stavu [16]. Jeden přispěvatel dosexzkreslení distribuce tukové tkáně může být rychlost přímého příjmu mastných kyselin tkáněmi, což je proces, který probíhá nezávisle na lipoproteinové lipáze (enzymu odpovědném za uvolňování mastných kyselin z lipoproteinů). Přímé vychytávání mastných kyselin je vyšší v gluteálním femorálním depu u žen a v abdominálním depu u mužů [17].
Celková tuková hmota i hromadění viscerálního tuku jsou silně spojeny s rozvojem kardiovaskulárních onemocnění, mrtvice, hypertenze a inzulinové rezistence [15,18,19]. Standardní měření pro akumulaci tuku u lidí zahrnují index tělesné hmotnosti (hmotnost jako funkci výšky), který odráží adipozitu celého těla, a poměr pasu a boků, který poskytuje indikaci rozložení tuku, přičemž měření v pase jako proxy pro viscerální tuk a měření kyčle pro gluteální tuk [19]. Seminářové studie provedené v 80. letech 20. století prokázaly, že celková adipozita, stejně jako hmota podkožního tuku, mají dědičnost přibližně 30 procent [20]. Tento odhad byl potvrzen studií z roku 1990 u kavkazských mužských dvojčat, která prokázala 31procentní dědičnost poměru pasu k bokům, zatímco novější populační studie odhadovala dědičnost stejného znaku na 39 procent [21,22]. Některé odhady naznačují, že dědičnost distribuce tuku je větší u žen než u mužů [19]. Distribuce tuku a dědičnost se také liší mezi etnickými skupinami [23,24]. Jeden přístup k identifikaci genů, které přispívajísexrozdíly v akumulaci a distribuci tukové tkáně jsou celogenomové asociační studie (GWAS) ve velkých lidských kohortách. Tento přístup typuje genetické varianty napříč genomem a koreluje jejich výskyt se znakem k identifikaci lokusů, které jsou asociovány. GWAS prováděné u stovek tisíc lidí identifikovalo více než 100 genetických lokusů, které obsahují běžné genetické varianty ovlivňující adipozitu [25e27]. Důležité je, že nejméně 17 lokusů, které jsou spojeny s indexem tělesné hmotnosti, bylo také identifikováno v GWAS pro diabetes 2. typu [25].
Analýza nashromážděných dat GWAS odhalila odlišnou genetickou architekturu pro lokusy ovlivňující adipozitu u mužů a žen. Například metaanalýza více než 50 studií GWAS s poměrem pasu k bokům (upraveným pro celkový tuk) u více než 200000 jedinců identifikovala 49 lokusů, z nichž 20 ukázalosex-specifické účinky, přičemž 19 z nich má silnější účinky u žen [28]. Tyto lokusy představují bohatý zdroj pro identifikaci genetických faktorů ovlivňujících pohlaví pro složení těla a distribuci tuku, i když v současnosti tyto lokusy dohromady tvoří pouze několik procent genetické variability v adipozitě. Zbývá vykonat mnoho práce, včetně identifikace kauzálních variant v každém lokusu a jejich mechanismu působení na ovlivnění adipozity. Je třeba poznamenat, že tyto analýzy nezohlednily lokusy na chromozomech X nebo Y, což zanechalo mezeru v našich znalostech o tom, jak mohou genetické variace na X a Y přispět k pozorovanýmsexrozdíly v adipozite. Následující části popisují studie mimo GWAS, které informovaly o úloze chromozomů X a Y při adipozitě a metabolických onemocněních.

extrakt z cistanche tubolosa
3. ROZDÍLY POHLAVÍ V EXPANZI TUKOVÉ TKÁNĚ
Bylo navrženo, že adipocyty v gluteálních femorálních depotech (a dalších subkutánních depotech) propůjčují lepší metabolické zdraví díky schopnosti expandovat a ukládat více tuku náborem nových adipocytů [16,29,30]. Dříve se předpokládalo, že samci myší vykazují větší expanzi tukové hmoty vyvolanou stravou (ve viscerálních i subkutánních zásobnících) než samice, a to je částečně způsobeno účinkysexhormony [31e33]. Nedávná studie však ukazuje, že u myší C57BL/6Jsexrozdíly v přírůstku hmotnosti vyvolaném dietou silně závisí na věku myší, které jsou krmeny stravou s vysokým obsahem tuku. U juvenilních myší (ve věku 6 týdnů) vedlo podávání stravy s vysokým obsahem tuku po dobu 3 měsíců k většímu procentuálnímu přírůstku hmotnosti u samců než u samic. U dospělých myší (ve věku 31 týdnů) se však trend obrátil a samice přibraly podstatně vyšší procento tělesné hmotnosti jako odpověď na dietu s vysokým obsahem tuku [34].
Jeden potenciální přispěvatel dosexrozdíly v expanzi tukové tkáně je počet prekurzorových buněk adipocytů (pluripotentní kmenové buňky, které se mohou diferencovat na adipocyty, chondrocyty nebo osteoblasty) v depotech myších gonád nebo podkožního tuku. Samice myší C57BL/6J na dietě s nízkým obsahem tuku mají více prekurzorových buněk adipocytů než samci v gonadálních (viscerálních) a inguinálních (subkutánních) tukových polštářcích [35e 37]. Když byly krmeny stravou s vysokým obsahem tuků (45 procent kalorií jako tuk), samice myší vykazovaly zvýšené prekurzorové buňky adipocytů a zralé adipocyty v gonadálním tuku, ale samci nezvyšovali počet zralých tukových buněk v tukovém polštáři gonád [36]. Jiné studie, které využívaly pulsní značení nebo sledování linií ke sledování osudu proliferujících progenitorových buněk adipocytů, odvodily, že mužský gonadální tuk vykazuje hyperplazii v reakci na dietu s vysokým obsahem tuku, zatímco ženy vykazují hyperplazii adipocytů v gonadálních i podkožních tukových zásobách [ 38,39]. Thesex- specifické vzorce byly zvráceny ovariektomií u samic myší nebo podáváním estrogenu u myších samců, což naznačuje roli gonadálních hormonů [37]. Tyto studie se ukázaly jako cenné, ale jsou zapotřebí další studie náboru a obratu adipocytů v tukových zásobách obou pohlaví, aby se objasnily nesrovnalosti mezi studiemi, které používaly odlišné metodiky, a aby byly poskytnuty další podrobnosti.
4. GONADÁLNÍ A CHROMOZOMÁLNÍ VLIVY NA ADIPOSTU
Gonadální hormony mají zásadní vliv na ukládání tuku a související onemocnění, jak dokazují srovnání žen před menopauzou a po menopauze. Po menopauze a snížení hladin estrogenu a dalších gonadálních hormonů ženy typicky pociťují zvýšené ukládání tuku v abdominálních depotech a zvýšený výskyt kardiovaskulárních onemocnění, hyperlipidemie, inzulínové rezistence a hypertenze [14,40e43]. Krátkodobé snížení hladiny estrogenu (4 týdny) však nevedlo ke změněnému ukládání tuku, i když ovlivnilo postprandiální hladiny cirkulujících triglyceridů [44]. Naproti tomu krátkodobá (4 týdny) suprese hladin testosteronu u mužů vedla ke zvýšenému ukládání mastných kyselin pocházejících z jídla v hýžďovém femorálním depotu tuku [45]. Účinky gonadálních hormonů na vývoj tukových zásob a metabolismus jsou pravděpodobně ovlivněny řadou proměnných, včetně hladin hormonů a hladin estrogenních a androgenních receptorů [46].
Kromě dobře zavedených rolí gonadálních hormonů, hromadící se důkazy podporují klíčovou rolisexchromozomů při určování pohlavních rozdílů v adipozitě. Přítomnost chromozomů XX u žen a chromozomů XY u mužů určuje vývoj vaječníků, respektive varlat [47]. Konkrétně gen SRY (sex-determining region Y) přítomný na chromozomu Y kóduje transkripční faktor, který u embryí XY iniciuje vývoj varlat a následnou tvorbu testikulárních hormonů. Nedostatek genu SRY v embryu (v důsledku XX chromozomů nebo delece genu SRY) vede k rozvoji vaječníků a produkci ovariálních hormonů.Sexrozdíly ve složení těla jsou zřejmé před expozicí gonadálním hormonům. Například během embryonálního vývoje člověka a myši vykazují samčí plody větší velikost než samičí plody ještě před gonadální diferenciací [48,49]. Děti nadále vykazují rozdíly mezi pohlavími v tělesné hmotnosti při narození, přičemž děti mužského pohlaví obvykle váží více než děti ženského pohlaví, částečně kvůli větší délce těla a většímu obvodu hlavy [50]. Rozdíly mezi muži a ženami ve výšce, hmotnosti, svalové hmotě a celkové hmotě tělesného tuku přetrvávají v dětství, před pubertou [51].
Jeden přístup ke studiu účinkůsexkomplementu chromozomů je hodnocení adipozity a souvisejících vlastností u jedinců s Klinefelterovým syndromem (XXY) nebo Turnerovým syndromem (XO). Klinefelterův syndrom je nejčastějšísexchromozomová porucha, která se vyskytuje přibližně u 1 z 660 porodů a je častou příčinou neplodnosti a hypogonadismu u mužů [52]. Tito muži mají typicky eunuchoidní tělesný habitus, malá varlata, hypogonadotropní hypogonadismus a neplodnost [53]. U jedinců s Klinefelterem bylo prokázáno, že mají téměř pětkrát vyšší výskyt rozvoje metabolického syndromu [54], který je definován jako výskyt alespoň tří z následujících: abdominální obezita, zvýšená hladina glukózy nalačno, zvýšená hladina triglyceridů, snížená vysoká hustota lipoproteinů a hypertenze [55]. Muži XXY mají také zvýšené riziko inzulinové rezistence a diabetu 2. typu [56,57]. Je možné, že zvýšené riziko metabolického syndromu a inzulinové rezistence u jedinců XXY je sekundární ke zvýšené abdominální obezitě, která zase může pramenit z hypogonadismu a nízkých hladin testosteronu u mužů XXY [54,56,58]. Důležité je, že studie prepubertálních chlapců XXY (průměrný věk < 11)="" identifikovaly="" zvýšenou="" hmotu="" tělesného="" tuku="" a/nebo="" obvod="" pasu="" před="" vlivem="" změněných="" hladin="" gonadálních="" hormonů="" v="" pubertě="" [59,60].="" to="" naznačuje,="" že="" samotný="" komplement="" pohlavního="" chromozomu="" xxy="" může="" ovlivnit="" adipozitu="" a="" související="" metabolické="">
Turnerův syndrom (TS) je nejčastější abnormalitou pohlavních chromozomů postihující ženy s incidencí 1 z 2500 až 3000 živě narozených dětí (8). Ženy s TS se vyznačují nízkým vzrůstem, krkem s plovací blaninou a sexuálním infantilismem s gonadální dysgenezí [61,62]. Ženy s TS mají také vrozené srdeční vady, které je mohou predisponovat k srdečnímu onemocnění, které se vyvíjí nezávisle na metabolických faktorech [63]. V souvislosti s metabolickým onemocněním mají XO ženy dramaticky snížené hladiny gonadálních hormonů [64]. Vzhledem k tomu, že estrogeny a progestiny u normálních premenopauzálních žen poskytují ochranu před abdominální obezitou a inzulinovou rezistencí a podporují ukládání tuku v gluteálních femorálních tukových polštářcích [40], nízké hladiny těchto hormonů mohou zastírat jakékoli přímé účinky komplementu XO chromozomu na metabolismus. V souladu s nízkými hladinami gonadálních hormonů mají TS ženy čtyřnásobné zvýšení rizika diabetu 2. typu a trojnásobné zvýšení celkové mortality [65]. Předpokládá se, že potenciální role časného programování plodu přispívá k metabolickým abnormalitám u žen s TS, což je v souladu s nízkou porodní hmotností a vysokou tělesnou hmotností v dospělosti [66]. Další údaje ukazují roli počtu pohlavních chromozomů, jak je popsáno níže.
Kvůli matoucímu účinku aberantních hladin gonadálních hormonů u žen XO je obtížné dospět k závěrům o vlivu komplementu pohlavních chromozomů na metabolickou homeostázu u těchto jedinců. Z experimentálního hlediska by bylo cenné porovnat účinky jediného chromozomu X u TS žen s jedinci se dvěma chromozomy X na pozadí podobně nízkých gonadálních hormonů. Posledně jmenovaný stav je přibližně u XX žen s primární ovariální insuficiencí (POI) a odpovídajícími nízkými hladinami gonadálních hormonů. Srovnání lipidových profilů u žen s TS a POI (věku a tělesné hmotnosti) dva týdny po ukončení estrogenní substituční terapie ukázalo, že ženy s TS měly více aterogenní lipidový profil [67]. Vzhledem k tomu, že ženy s TS i POI měly snížené příspěvky gonadálních hormonů ve srovnání s normálními ženami a odpovídaly životnímu stylu a složení těla, výzkumníci předpokládali, že některé metabolické účinky u žen s TS lze přičíst změněnému dávkování chromozomu X [57,67]. Je však důležité si uvědomit, že srovnání mezi ženami s TS a POI zůstává matoucí skutečností, že jedinci s TS mají aberantní vývoj a zhoršenou sekreci ovariálních hormonů po celý život, zatímco ženy s POI jsou během vývoje normální a jsou postiženy až později v životě. .
Další anomálie pohlavních chromozomů vyskytující se u lidí zahrnují Swyerův syndrom a Triple X syndrom. Swyerův syndrom, také známý jako XY gonadální dysgeneze, je vzácná porucha sexuálního vývoje, kdy 46 XY jedinců má narušený vývoj gonadální tkáně [68]. Tito jedinci se navenek prezentují jako ženy, ale nevyvinou se jim funkční vaječníky a neprocházejí pubertou, pokud nejsou léčeni hormonální terapií. Tento stav může být způsoben mutacemi genu SRY (předpokládá se, že je základem 10 až 20 procent případů) nebo mutacemi v jiných genech [68]. Syndrom Triple X (47, XXX) je charakterizován proměnlivou prezentací fenotypů, jako je vysoká postava, kognitivní poruchy a poruchy chování a problémy se zuby [69]. V současné době nebyly hlášeny žádné studie s adekvátní velikostí vzorků syndromu Swyer nebo XXX, které by analyzovaly účinky těchto stavů na adipozitu nebo související metabolické vlastnosti. Je třeba poznamenat, že v buňkách XO, XX a XXX inaktivace chromozomu X umlčí většinu genů na všech chromozomech X kromě jediného. Výskyt abnormalit u Turnerova (XO) i XXX syndromu proto podporuje názor, že dávkování chromozomů X je důležité, navzdory procesu inaktivace všech X kromě jednoho. Možné důvody důležitosti mít právě dva chromozomy X je diskutováno v částech 5 a 8.

přínos extraktu z cistanche tubolosa: léčba onemocnění ledvin
5. ÚLOHA DÁVKOVÁNÍ XX CHROMOZOMŮ V ROZDÍLECH POHLAVÍ V ADIPOSTĚ
Průkazné studie metabolických změn u XXY mužů a XO žen byly brzděny nedostatkem vhodných kontrolních skupin s podobnými hladinami gonadálních hormonů, omezenou statistickou silou kvůli malým kohortám a heterogenitou mezi jednotlivci v genetických a environmentálních faktorech, které obezitu ovlivňují. . Použití myších modelů umožňuje překonat některá z těchto omezení a vyhodnotit relativní přínosysexchromozomů a gonadálních hormonů na rozdíly mezi pohlavími.
Tradiční přístup používaný v myších modelech k identifikaci příčinysexrozdíly je posoudit působení gonadálních hormonů po pubertě [70]. Dospělým samicím a samcům myší se provede gonadektomie a vyšetří se, aby se zjistilo, zda je původní rozdíl mezi pohlavími odstraněn. Pokud ano, provede se náhrada hormonů implantovanou pumpou nebo denní injekcí a myši se pozorují, aby se zjistilo, zda je původní rozdíl mezi pohlavími obnoven. Následné studie mohou zahrnovat identifikaci hormonálního receptoru, který zprostředkovává účinek, což lze provést chemickou nebo genetickou inhibicí funkce hormonálního receptoru. U pohlavních rozdílů, ke kterým dochází před pubertou nebo které nejsou změněny gonadektomií, lze studovat roli nárůstů testosteronu, ke kterým dochází pre- nebo postnatálně. Pro smysluplné provedení a interpretaci studií, které manipulují s gonadálními hormony, je třeba vzít v úvahu mnoho faktorů, které jsou přezkoumány jinde [70]. Pokud rozdíly gonadálních hormonů nemohou plně vysvětlit rozdíl mezi pohlavími, je třeba zvážit potenciální účinek komplementu pohlavních chromozomů.
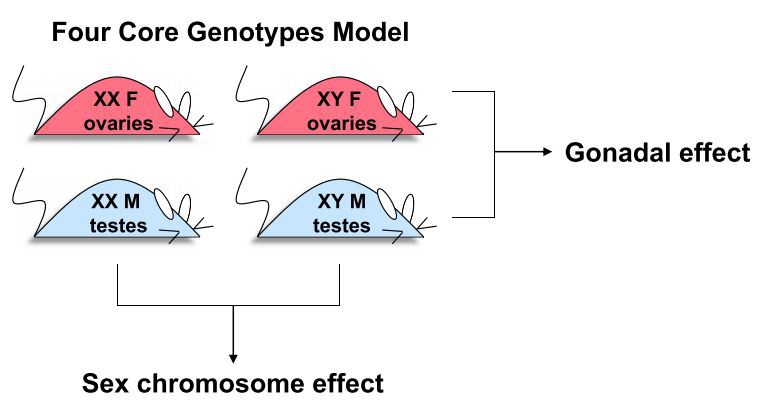
Myší model, který byl speciálně navržen tak, aby analyzoval účinky gonadálních hormonů, stejně jakosexchromozomy, je myš se čtyřmi jádrovými genotypy (FCG). Model zahrnuje přemístění genu Sry, který podporuje vývoj varlat, z chromozomu Y na autozom tak, aby se gonadální pohlaví mohlo segregovat nezávisle na komplementu pohlavního chromozomu [70,71]. Pozice genu Sry na autozomu nemění prenatální ani dospělé hladiny androgenů [72]. Studie provedené na myších FGC zahrnují srovnání čtyř genotypů, které zaměňují chromozomální a gonadální složky pohlaví za vzniku XX myší s vaječníky nebo varlaty a XY myší s vaječníky nebo varlaty (označované jako XX F, XX M, XY F a XY M). Porovnání těchto čtyř genotypů 2x2 umožňuje identifikaci účinků, které jsou diktovány buď gonadálním typem nebosextyp chromozomu (obrázek 1). Aby se eliminoval příspěvek cirkulujících gonadálních hormonů, jsou FCG myši často studovány po gonadektomii v dospělosti.
Pomocí FCG modelu, účinkysexByl identifikován komplement chromozomů na několika metabolických vlastnostech, včetně obezity, profilu plazmatických lipidů, příjmu potravy a hypertenze [73e77]. U myší C57BL/6 FCG, kterým byla v dospělosti provedena gonadektomie, aby se odstranily akutní účinky gonadálních hormonů, myši s chromozomy XX versus XY (bez ohledu na původně přítomné mužské nebo ženské pohlavní žlázy) rychleji přibíraly na váze při jídle nebo stravě s vysokým obsahem tuků a akumulovaly větší tělesnou hmotnost. tuku, zejména v inguinálním podkožním depu (obrázek 2) [73]. Zvýšený přírůstek hmotnosti u XX ve srovnání s XY myšmi byl podpořen, alespoň částečně, zvýšeným příjmem potravy u XX myší, konkrétně během lehké fáze cirkadiánního cyklu [74]. Jako noční zvířata spotřebují myši přibližně 70 procent svých kalorií během fáze tmy a během fáze světla odpočívají a svačí (30 procent celkových kalorií). Zvýšený příjem potravy u XX myší ve světlé fázi byl způsoben anticipačním jídlem, které začalo asi 1,5 hodiny před jejich XY protějšky [74]. Kromě zvýšené akumulace tukové tkáně se u XX myší krmených stravou s vysokým obsahem tuku po dobu 16 týdnů vyvinuly stavy související s obezitou, jako je ztučnění jater, zvýšená hladina celkového cholesterolu v krvi a zvýšená hladina inzulínu [73]. Je pravděpodobné, že tyto metabolické poruchy jsou sekundární ke zvýšené akumulaci tuku u XX myší krmených stravou s vysokým obsahem tuku, protože nejsou pozorovány u XX myší krmených stravou.
Údaje od myší FCG jasně ukázaly účinek chromozomů XX ve srovnání s chromozomy XY na adipozitu a morbidity související s obezitou. Tyto studie však samy o sobě nerozlišovaly mezi účinkem dávkování chromozomu X (dva versus jeden X) nebo účinkem přítomnosti nebo nepřítomnosti chromozomu Y. Analýza myších modelů s dalšími genotypy pohlavních chromozomů umožnila identifikovat relevantní efekt pohlavních chromozomů. Použitím neobvyklého chromozomu Y se sekvenčními duplikacemi v pseudoautozomální oblasti (známý jako model XY*, [71]) byla u myší s chromozomy XX, XY, XO a XXY hodnocena tělesná hmotnost a adipozita. Výsledky ukázaly, že přítomnost dvou X chromozomů (XX a XXY myši) vedla k vyšší tělesné hmotnosti/tuk než jeden X chromozom (XY a XO); přítomnost chromozomu Y neměla vliv (obrázek 2) [73].

cistanche stonek
6. PŮSOBENÍ SEXCHROMOZOMŮ NA HLADINY LIPIDŮ
Za adipozitou,sexChromozomový komplement u myší a lidí ovlivňuje hladiny lipidů v plazmě. Zvýšené hladiny celkového plazmatického cholesterolu a specifických lipoproteinových podtříd mají dobře známé epidemiologické souvislosti s kardiovaskulárním onemocněním. Na obecné úrovni je zvýšení hladin lipoproteinů s nízkou hustotou (LDL) a snížení hladin lipoproteinů s vysokou hustotou (HDL) spojeno se zvýšeným rizikem kardiovaskulárních onemocnění [78]. Současné výsledky naznačují, že specifické složky lipidového profilu jsou nezávisle ovlivněny dávkováním chromozomu X, přítomností chromozomu Y a gonadálními hormony; pozorované rozdíly mezi pohlavími jsou pravděpodobně složeninou všech těchto příspěvků. Zdá se například, že gonadální hormony regulují metabolismus lipoproteinů, protože ženy před menopauzou mívají vyšší hladiny HDL a nižší hladiny LDL než muži a po menopauze se profily lipoproteinů stávají více podobnými mužům (přehled v odkazu [18]). . Důkaz pro účinky chromozomu Y pochází z důkazu, že genetické variace na chromozomu Y jsou spojeny s lipoproteinovými profily u mužů [79,80] a myší [81]. Studie s myším modelem FCG navíc odhalily účinky dávkování chromozomu X na hladiny HDL cholesterolu, zatímco gonádové hormony měly vliv na hladiny triglyceridů a mastných kyselin [18,77].
7. POHLAVÍ ROZDÍLY V ZÁNĚTI A IMUNOMETABOLISMU
Obezita je zánětlivé onemocnění a u myší bylo prokázáno, že samci a samice se liší v zánětlivé odpovědi, která se vyskytuje u obezity vyvolané dietou [82]. Rozdíly mezi pohlavími v zánětlivé odpovědi, kterou u myší vyvolává dieta s vysokým obsahem tuku, zahrnují zvýšenou infiltraci tukové tkáně makrofágy M1 (CD11cþ) u samců, ale makrofágy M2 (CD11ce) u samic a zvýšené hladiny zánětlivých cytokinů u samců ve srovnání se samicemi [ 83]. Studie transplantace kostní dřeně prokázaly, že pohlavně závislá zánětlivá odpověď souvisí s buněčným vnitřním sexuálním dimorfismem ve složení nebo aktivaci populací hematopoetických kmenových buněk [83].
Autoimunitní onemocnění patří k těm nejsilnějšímsex- zaujatý všemi nemocemi a 80 procent autoimunitních pacientů jsou ženy [84]. Obezita je rizikovým faktorem autozánětlivých a autoimunitních onemocnění včetně systémového lupus erythematodes, diabetu 1. typu, revmatoidní artritidy a psoriázy [85]. Pravděpodobné mechanické vazby mezi obezitou a autoimunitní dysfunkcí zahrnují na pohlaví závislé změny v hladinách adipokinů produkovaných adipocyty (např. leptin, resistin, adiponektin, visfatin) a produkci zánětlivých cytokinů (např. tumor nekrotizující faktor-a, interleukin{{ 7}}). Jak gonadální hormony, tak dávkování chromozomu X se podílejí na ženském zkreslení autoimunitního onemocnění [86]. V souladu s účinky gonadálních hormonů je sexuální zkreslení u autoimunitních onemocnění patrnější po pubertě. Estrogeny a androgeny mají zřetelný vliv na produkci cytokinů a diferenciaci T buněk. Testosteron potlačuje jak adaptivní, tak vrozenou imunitní odpověď, zatímco estrogen může podporovat zánětlivé reakce [87,88]. Interakce mezi složením střevních mikrobů v raném věku a hladinami gonadálních hormonů byla identifikována u diabetu 1. typu u neobézních diabetických myší [89]. V tomto modelu komenzální bakterie ve střevě zvýšily hladiny testosteronu v séru u mužů, což bylo protektivní proti diabetu 1. typu. Přenos střevních mikrobiálních populací z dospělých mužů na nezralé ženy vedl ke zvýšeným hladinám testosteronu, snížení zánětu pankreatických ostrůvků a ochraně proti diabetu 1. typu. Tyto účinky byly závislé na aktivitě androgenního receptoru.
Kromě účinků gonadálních hormonů na autoimunitu,sexroli pravděpodobně hraje komplement chromozomů. Použitím FCG myšího modelu ke studiu experimentální autoimunitní encefalomyelitidy (relevantní pro roztroušenou sklerózu) a spontánního lupusu bylo onemocnění závažnější u XX ve srovnání s XY myšmi se samičími gonádami [90e92]. Studie metylace DNA naznačují, že otisk genů chromozomu X od matky proti otcovu by mohl přispět ksexrozdíly u experimentální imunitní encefalitidy [93]. Dávkování genu chromozomu Y se také podílí na autoimunitním onemocnění. Například přirozená genetická variace v počtu kopií genů s více kopiemi na chromozomu Y je spojena s náchylností k experimentální alergické encefalomyelitidě a experimentální myokarditidě u myší [94]. Studium konsomických myších kmenů chromozomu Y (které mají chromozom Y z jednoho inbredního myšího kmene na pozadí jiného inbredního kmene) odhalilo souvislost mezi počtem kopií dvou specifických genů chromozomu Y a genovou expresí v imunitních buňkách [94]. Role sekvencí chromozomu Y jako trans-působícího regulátoru genové exprese může přispívat k sexuálnímu dimorfismu u autoimunitních onemocnění. Interpretace takových zjištění je však složitá. Na jedné straně by mohly naznačovat, že chromozom Y může být částečně zodpovědný za udělení pozorovaných rozdílů mezi pohlavími v náchylnosti k autoimunitním onemocněním. Na druhé straně se předpokládá, že genová exprese z chromozomu Y působí jako „vyvažovač“ účinků chromozomu X. Z tohoto pohledu exprese genů z chromozomu Y činí muže více podobnými ženám, takže změněné dávkování genu chromozomu Y může narušit rovnováhu a ovlivnit rozdíly mezi pohlavími u autoimunitních onemocnění a dalších znaků [95].

8. POTENCIÁLNÍ MECHANISMY PRO ÚČINKY SEXCHROMOZOMŮ NA METABOLISMUS
Existuje několik mechanismů, které mohou být základem účinkůsexkomplementu chromozomů na obezitu, metabolismus lipidů, autoimunitu a další znaky. Přítomnost chromozomů XX nebo XY zásadně ovlivňuje vývojovou cestu a vytváří celoživotní rozdíl mezi pohlavími v hladinách gonadálních hormonů. Jak gonadální hormony, tak pohlavní chromozomy ovlivňují genovou expresi, která je pravděpodobně základem fenotypových rozdílů pozorovaných mezi muži a ženami. Časné studie genové exprese u samců a samic myší z genetického křížení dvou inbredních kmenů odhalily rozdíly mezi samci a samicemi v genové expresi v tukové tkáni, játrech a kosterním svalstvu (tisíce genů) a také v mozku (stovky genů) [96]. Tato studie také poskytla důkazy pro globální regulaci podskupin genů, které byly rozdílně exprimovány mezi genypohlaví. Následná studie na stejné intercrossové populaci myší odhalila korelace mezi hladinami tělesného tuku a lipidů a pohlavně specifickými moduly genové exprese v tukové tkáni a játrech; Ukázalo se, že mnoho modulů je regulováno gonadálními hormony [97]. Další studie odhalily vliv gonadálních hormonů na transkripční profily podkožních a viscerálních zásob tukové tkáně [31,36].

Myší modely také odhalily účinky pohlavních chromozomů na genovou expresi. Je třeba poznamenat, že pohlavní chromozomy ovlivňují expresi stovek autozomálních genů a některé z těchto účinků jsou modulovány přítomností genu určujícího varlata, Sry [98e100]. MikroRNA (miRNA), které modulují hladiny genové exprese interakcí se specifickými druhy mRNA, aby se zvýšila jejich degradace nebo interferovaly s translací, je také ovlivněna pohlavím. Použitím FCG myšího modelu k analýze účinků gonadálního a chromozomálního pohlaví, celkový profil exprese miRNA ukázal zkreslení směrem k vyšší expresi u mužů ve srovnání se ženskou gonadální tukovou tkání [101]. Toto zkreslení bylo normalizováno po gonadektomii, což ukazuje na roli cirkulujících gonadálních hormonů při modulaci hladin miRNA. U myší krmených stravou s vysokým obsahem tuku byly hladiny miRNA vyšší u myší s komplementem chromozomu XX oproti XY. Existuje tedy složený účinek gonadálních hormonů a pohlavních chromozomů na expresi miRNA a pravděpodobně na mRNA regulované těmito miRNA.
A recent analysis of human transcriptome data from the GTEx project is consistent with mouse data in detecting thousands of genes that are differentially expressed in male and female tissues [102]. The GTEx project includes RNA-seq data from >50 tkání od stovek mužů a žen [103]. Většina genů, u kterých byly zjištěny rozdíly v hladinách exprese mezi pohlavími, vykazovala tyto rozdíly v jedné nebo několika tkáních [102]. Naproti tomu 16 genů X-chromozomu mělo rozdíly mezi pohlavími v nejméně šesti tkáních, což naznačuje rozšířené účinky. Z tkání nalezených jak u mužů, tak u žen se genová exprese nejvíce pohlavně diferencovaných vyskytla v prsní tkáni, což je v souladu se sexuálně dimorfní fyziologií a strukturou prsní tkáně [102].
Je přímočaré si představit, jak by gonadální hormony mohly ovlivnit genovou expresi v genomu, ale méně intuitivní pochopit, jak by rozdíly v komplementu pohlavních chromozomů mohly změnit expresi genů na autosomech. Přítomnost dvou chromozomů X v buňce propůjčuje jedinečné vlastnosti, které nejsou přítomny v buňce XY. V buňkách XX je jeden chromozom X transkripčně umlčen v buňkách mimo zárodečnou linii, aby se snížila exprese většiny genů chromozomu X, takže hladiny jsou srovnatelné mezi buňkami XX a XY. Některé geny chromozomu X však „uniknou“ inaktivaci a zůstávají transkripčně aktivní na obou chromozomech X v buňkách XX. Důležité je, že geny, které unikají inaktivaci X, jsou mezi lidmi a myší z velké části konzervovány [104e108].
Geny unikající inaktivaci X vykazují zvýšenou expresi v tkáních od žen ve srovnání s muži, včetně metabolických tkání, jako je tuková tkáň a játra. Profil exprese u mužů a žen pro reprezentativní gen uniklého chromozomu X (KDM6A) je znázorněn na obrázku 3. Odpovídající myší gen (Kdm6a) vykazuje zvýšené hladiny exprese u XX ve srovnání s XY FGC myšmi, což ukazuje, že tento účinek je určen pohlavím chromozomový komplement spíše než gonadální hormony (obrázek 3). Odhaduje se, že 3e6 procent genů myšího chromozomu X unikne inaktivaci a tytéž geny plus další (přibližně 15 procent genů chromozomu X) uniknou inaktivaci u lidí [104e108]. Některé geny X escapee mají partnerské geny, které byly zachovány na chromozomu Y, a únik z inaktivace může pomoci normalizovat expresi těchto genů mezi buňkami XX a XY. Mnohem více genů chromozomu X však unikne inaktivaci, než mají partneři na chromozomu Y [107]. Geny X escapee kódují proteiny, které mohou široce ovlivňovat genovou expresi, včetně enzymů modifikujících histony, proteinů iniciujících translaci a helikáz RNA, abychom jmenovali alespoň některé. Rozdíly také existují mezi buňkami XX a XY kvůli otisku rodiče původu. Genomický imprinting je dědičná methylace DNA nebo histonu ve specifických oblastech chromozomů, která vede k umlčení transkripce. Otisky se zakládají v zárodečné linii matky nebo otce a předávají se potomkům tak, že alela pouze jednoho rodiče bude vyjádřena v potomstvu. Buňky XX obdrží chromozom X od otce i matky, zatímco buňka XY obdrží X výhradně od matky. Pouze buňky XX tedy podléhají otisku otcovského chromozomu X, což může vést k rozdílům v genové expresi u XX ve srovnání s buňkami XY. Pro rozsáhlejší diskusi o těchto mechanismech odkazujeme čtenáře na vynikající nedávné přehledy [47,71].
9. BUDOUCÍ PERSPEKTIVY
Navrhujeme, že nebudeme plně rozumět mnoha aspektům metabolismu, dokud nepochopíme rozdíly mezi pohlavími v metabolismu. Patří sem rozdíly mezi ženami a muži v riziku a rozvoji obezity a v projevech souvisejících nemocí. Identifikace těchto rozdílů může odhalit, jak je jedno pohlaví chráněno před specifickými následky onemocnění ve srovnání s druhým, a navrhnout nové možnosti prevence a léčby pro obě pohlaví. Nejúplnější pochopení poskytnou výzkumné přístupy, které berou v úvahu složky vlivu zkreslení pohlaví, včetně rozdílů diktovaných typem gonád a komplementem pohlavních chromozomů. Studium myších modelů s unikátními kombinacemi pohlavních chromozomů a lidí s přirozeně se vyskytujícími variacemi pohlavních chromozomů již začalo naznačovat důležité účinky pohlavních chromozomů na obezitu, metabolismus lipidů a záněty. Další porozumění bude vyžadovat úplnější objasnění molekulárních rozdílů způsobených přítomností komplementů chromozomů XX nebo XY. Současné uznání pohlaví jako důležité biologické proměnné, kterou je třeba vzít v úvahu ve výzkumu [109e111], pravděpodobně poskytne novou (a vítanou) motivaci k posunu oboru kupředu.

REFERENCE
[1]Voskuhl, R., 2011. Pohlavní rozdíly u autoimunitních onemocnění. Biologie pohlavních rozdílů 2(1):1.
[2]Klein, SL, Flanagan, KL, 2016. Pohlavní rozdíly v imunitních odpovědích. Nature Reviews Immunology 16(10):626e638.
[3]Jaillon, S., Berthenet, K., Garlanda, C., 2017. Sexuální dimorfismus ve vrozené imunitě. Klinické přehledy v alergii a imunologii.
[4]Aswat, KA, 2017. Genderové rozdíly u osteoporózy. Journal of Clinical Medicine Research 9(5):382e387.
[5]Zákony, KR, Irvine, K., Gale, TM, 2018. Pohlavní rozdíly u Alzheimerovy choroby. Aktuální názor v psychiatrii 31(2):133e139.
[6]Rainville, JR, Tsyglakova, M., Hodes, GE, 2017. Dešifrování rozdílů mezi pohlavími v imunitním systému a depresi. Hranice v neuroendokrinologii.
[7]Werling, DM, Geschwind, DH, 2013. Pohlavní rozdíly u poruch autistického spektra. Aktuální názor v neurologii 26(2):146e153.
[8]Jurado-Coronel, JC, Cabezas, R., Ávila Rodríguez, MF, Echeverria, V., García-Segura, LM, Barreto, GE, 2017. Pohlavní rozdíly u Parkinsonovy choroby: vlastnosti klinických příznaků, léčba výsledek, sexuální hormony a genetika. Hranice v neuroendokrinologii.
[9]Li, R., Ma, X., Wang, G., Yang, J., Wang, C., 2016. Proč rozdíly mezi pohlavími u schizofrenie? Journal of Translational Neuroscience 1(1):37e42.
[10]Regitz-Zagrosek, V., 2012. Pohlaví a genderové rozdíly ve zdraví. EMBO Reports 13(7):596e603.
[11]Dobyns, W., 206. Vzor dědičnosti X-vázaných znaků není dominantní ani recesivní, pouze X-vázaný. Acta Paediatrica 95(0):11e15.
[12]Shah, RR, Bird, AP, 2017. Mutace MeCP2: pokrok směrem k pochopení a léčbě Rettova syndromu. Genomová medicína 9(1):17.
[13]Mauvais-Jarvis, F., Clegg, DJ, Hevener, AL, 2013. Role estrogenů při řízení energetické rovnováhy a homeostázy glukózy. Endokrinní recenze 34(3):309e338.
[14]Karastergiou, K., Smith, SR, Greenberg, AS, Fried, SK, 2012. Pohlavní rozdíly v lidských tukových tkáních a biologie tvaru hrušky. Biologie pohlavních rozdílů 3(1):13.
[15]Karpe, F., Pinnick, KE, 2015. Biologie vazby tukové tkáně horní a dolní části těla na celotělové fenotypy. Nature Reviews Endocrinology 11(2): 90e100.
[16]Karastergiou, K., Fried, SK, 2017. Buněčné mechanismy ovlivňující pohlavní rozdíly v biologii tukové tkáně a tvaru těla u lidí a myších modelů. Pokroky v experimentální medicíně a biologii 1043:29e51.
[17]Mundi, MS, Koutsari, C., Jensen, MD, 2014. Účinky zvýšené dostupnosti volných mastných kyselin na ukládání mastných kyselin v tukové tkáni u mužů. The Journal of Clinical Endocrinology & Metabolism 99(12): E2635eE2642.
[18]Link, JC, Reue, K., 2017. Genetický základ pro rozdíly mezi pohlavími v obezitě a metabolismu lipidů. Výroční přehled výživy 37(1):225e245.
[19]Pulit, SL, Karaderi, T., Lindgren, CM, 2017. Sexuální dimorfismy v genetických lokusech souvisejících s distribucí tělesného tuku. Bioscience Reports 37(1).
[20]Bouchard, C., Pérusse, L., Leblanc, C., Tremblay, A., Thériault, G., 1988. Dědičnost množství a rozložení lidského tělesného tuku. International Journal of Obesity 12(3):205e215.







