Část 1: Přírodní bioaktivní sloučeniny v léčbě orálních chorob u nefropatických pacientů
Jun 20, 2022
Pro více informací Kontakttina.xiang@wecistanche.com
Abstraktní: Mezi chronická nepřenosná degenerativní onemocnění (CDNCD),chronické onemocnění ledvin(CKD) představuje globální problém veřejného zdraví. Nedávné studie prokazují vzájemný vztah příčina-účinek mezi CKD a orálními chorobami, ve kterých přítomnost jednoho indukuje nástup a rychlejší progresi druhého. Zejména změny v dutině ústní, které jsou u pacientů s CKD častější, jsou chronická periodontitida, kostní léze, infekce dutiny ústní a léze rakoviny dutiny ústní. V současné době chybí standardizovaná terapie pro léčbu onemocnění dutiny ústní. Z tohoto důvodu jsou přírodní bioaktivní sloučeniny (NBC), vyznačující se několika zdravotními účinky, jako napřantioxidant, antimikrobiální,protizánětlivé, aprotirakovinnéakce, představují novou možnou adjuvantní terapii v managementu těchto patologických stavů. Mezi NBC hrají polyfenoly vedoucí roli díky pozitivní modulaci orální mikroflóry, prevenci a nápravě orální dysbiózy. Kromě toho tyto sloučeniny vykazují protizánětlivé účinky, jako je inhibice produkce prozánětlivých cytokinů a exprese cyklooxygenázy-2. V tomto světle formulace nové ústní vody/gelu/gingivální pasty s vysokým obsahempolyfenolyve spojení s NBC charakterizovanými antimikrobiálním účinkem by mohla představovat budoucí terapii onemocnění dutiny ústní u pacientů s CKD.
Klíčová slova: chronické onemocnění ledvin; chronická onemocnění parodontitidy; polyfenoly; orální mikroflóra; renální substituční terapie; speciální péče stomatologie
Kliknutím sem se dozvíte o organické cistanche
1. Úvod
Onemocnění ústní dutiny patří mezi nejrozšířenější patologické stavy na světě a rychle se šíří a v posledních několika letech se stávají skutečnou globální epidemií. Orální onemocnění jsou často spojena s vysilujícími stavy, které snižují kvalitu života pacientů a zvyšují náklady na veřejné zdraví[1]. Z tohoto důvodu byla v průběhu let věnována větší pozornost orální preventivní výchově, podpoře používání správných hygienických postupů a odrazování od špatných životních návyků, jako je kouření, zneužívání alkoholu a nadměrná konzumace cukru [2,3]. Zdá se, že zdraví ústní dutiny úzce souvisí s celkovým zdravím jedince [4]. Nástup onemocnění dutiny ústní, například kazu nebo parodontitidy, se zdá být důležitým rizikovým faktorem pro rozvoj několika chronických nepřenosných degenerativních onemocnění (CDNCD), včetně chronického onemocnění ledvin (CKD)[5,6]. Několik studií naznačuje, že chronická parodontitida (CPD) je spojena se zvýšeným rizikem diabetes mellitus, arteriální hypertenze, aterosklerózy a neurodegenerativních onemocnění [7-13]. Orální onemocnění a CKD se zdají být spojeny ve vzájemném vztahu příčina-účinek, ve kterém přítomnost jednoho indukuje nástup a progresi druhého|14,15. Nedávné epidemiologické studie naznačují, že pacienti s CKD jsou ve srovnání s běžnou populací náchylnější k onemocněním dutiny ústní [16,17]. Mechanismy, které jsou základem tohoto vztahu, jsou však stále nedostatečně prozkoumány a dostupné údaje je třeba potvrdit většími randomizovanými klinickými studiemi. Možnou souvislost mezi těmito dvěma nemocemi by mohla představovat změna ústní mikrobioty, souboru symbiotických bakterií v dutině ústní[18]. Ve skutečnosti na jedné straně ústní onemocnění vyvolávají změnu ústní mikroflóry, která ztrácí schopnost chránit hostitele před patogenními bakteriemi, které mohou vstoupit ústním otvorem. Z tohoto důvodu by změna složení orální mikrobioty mohla představovat rizikový faktor pro nástup CDNCD. Tato systémová onemocnění by tedy mohla vyvolat změnu orální mikroflóry, která je spojena se zvýšenou náchylností ke vzniku orálního onemocnění [19,20]. V současné době je jedním z hlavních témat výzkumu zaměření na využití strategií k prevenci změn ústní mikroflóry a k ochraně celkového zdraví hostitele[18]. V této souvislosti by použití přírodních produktů, které bez vedlejších účinků, působí tak, že působí proti výskytu orální mikrobioty dysbiózy a chrání před CDNCD, mohlo představovat platnou adjuvantní strategii [21].
Přírodní bioaktivní sloučeniny (NBC) jsou biologické molekuly potravinového původu, obsažené především v potravinách rostlinného původu, které mají důležité příznivé účinky na lidský organismus [22,23]. NBC obsažené v potravinách rostlinného původu se nazývají fytochemikálie a lze je rozdělit do různých kategorií, jako jsou polyfenoly, karotenoidy, alkaloidy, fytosteroly, dusík a organické sloučeniny síry [24]. Několik studií in vitro a in vivo ukazuje, že se zdá, že NBC mají důležité protizánětlivé, antioxidační, antimikrobiální, protirakovinné, kardioprotektivní, neuroprotektivní, hepatoprotektivní, hypoglykemické a antihypertenzní účinky [25-28]. Kromě toho mohou NBC pozitivně modulovat složení orální mikroflóry [18]. V důsledku toho by příjem NBC mohl představovat platnou strategii schopnou působit proti nástupu a progresi CDNCD, včetně CKD. V tomto ohledu je účelem tohoto přehledu definovat vztah mezi orálními onemocněními a CKD a analyzovat možnou roli spotřeby NBC v prevenci a léčbě orálních onemocnění. Zejména z onemocnění dutiny ústní v tomto přehledu zkoumáme infekce dutiny ústní, změny kostní tkáně zubů a dutiny ústní, modifikace slin a výdechů a negativní změny měkkých tkání dutiny ústní.

2. Metody výzkumu
Abychom dosáhli účelu článku, vybrali jsme seznam studií na základě výzkumných online položek „přírodní bioaktivní sloučeniny“ a „orální onemocnění“ a „chronické onemocnění ledvin“ a „parodontitida“ ve spojení s „epigalokatechin galátem“ a/nebo „polyfenoly“. „a/nebo „orální mikroflóra" a/nebo „zánět dutiny ústní" a/nebo „renální substituční terapie" a/nebo „hemodialýza" a/nebo „peritoneální dialýza" a/nebo „transplantace ledvin" a/nebo „xerostomie". Do ledna 2022 byly použity databáze PubMed a Web of Science. Všechny studie byly v anglickém jazyce a autoři je stahovali ručně.
3. Orální zdraví a chronické onemocnění ledvin (CKD)
Orální zdraví pacientů s CKD je významně ohroženo a odhaduje se, že téměř 90 procent z nich vykazuje změny v dutině ústní, včetně onemocnění parodontu, poruchy mineralizace kostní matrix, hyperplazie dásní a změn sekrece a složení slin [29]. . Navíc pacienti s CKD vykazují větší predispozici k orálním infekcím[30]. Tyto změny mohou souviset jak se samotným CKD, tak s účinkem renální substituční terapie (RRT) [31,32]. Současně může špatná péče o ústní hygienu podporovat a zhoršovat chronický zánětlivý stav nízkého stupně, typický pro CKD [33]. K prevenci onemocnění dutiny ústní u pacientů s CKD je nutné vyvinout specifickou ústní hygienu
strategie. Navíc se ukázalo, že přítomnost léze nebo jiných patologických procesů v dutině ústní, pokud nejsou léčeny, mohou urychlit progresi nebo vyvolat nástup komorbidit CKD [31]. Zdá se, že orální onemocnění a CKD mají obousměrnou korelaci s recipročním vztahem příčina-účinek (obrázek 1) [34].
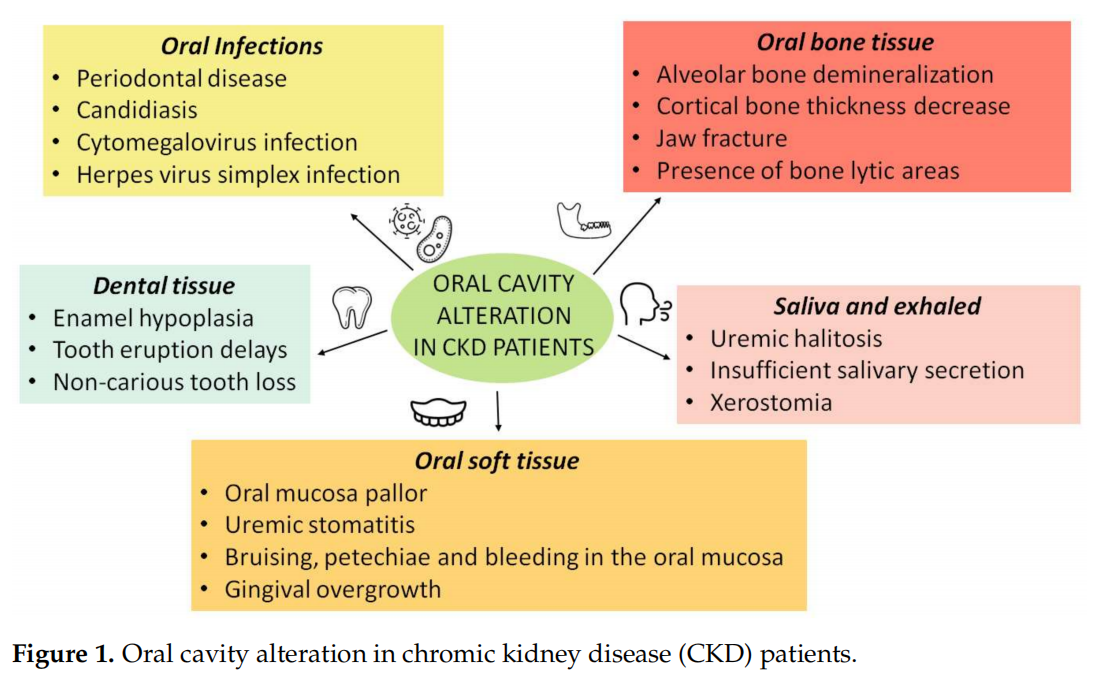

3.1. Účinky komorbidit CKD na orální zdraví
Některé z hlavních uremických komorbidit mohou představovat důležité rizikové faktory pro nástup orálních změn, včetně akumulace uremických toxinů, normochromní a normocytární anémie, nerovnováhy vody a elektrolytů a změn metabolismu vápníku a fosforu a možné doprovodné malnutrice [35].
3.1.1. Sliny a vydechované změny
Téměř jedna třetina pacientů s terminálním onemocněním ledvin (ESRD) vykazuje stav známý jako uremická halitóza [36]. Ztráta funkce ledvin, zvláště v pokročilejších stádiích CKD, vyvolává akumulaci močoviny jak ve slinách, tak v séru. V dutině ústní je přebytek urey přeměněn na amoniak mikrobiální flórou pozitivní na ureázu, která je odpovědná za typickou halitózu pacientů s ESRD [35]. Několik studií prokázalo přímou korelaci mezi akumulací močoviny a jiných uremických toxinů v séru s přítomností amoniaku ve výdechu pacientů s CKD [37]. Akumulace amoniaku v dutině ústní je zodpovědná za snížení průtoku slin a vysychání úst, což jsou jevy obvykle pozorované u pacientů s ESRD [36]. Kromě toho tento stav vede k vnímání kovové a nepříjemné chuti po požití potravy, což vede pacienta ke snížení příjmu kalorií a bílkovin, což přispívá k rozvoji syndromu plýtvání energií (PEW), typického pro pacienty s chronickým onemocněním ledvin. 38]. Pacienti s CKD mají často tento syndrom, který je charakterizován svalovým hyperkatabolismem, chronickým zánětlivým stavem a metabolickou acidózou [38-40]. Tento stav způsobuje neúmyslné snížení tělesné hmotnosti a ztrátu svalové hmoty se současným zvýšením prozánětlivých cytokinů, jako je tumor nekrotizující faktor (TNF)- a interleukin (IL)-6, částečně odpovědné za nástup chronického zánětlivého stavu [41. Navíc prozánětlivý stav má tendenci snižovat albumin v oběhu, což zhoršuje stav malnutrice [42. Vznik a zhoršení PEW syndromu zvyšuje míru hospitalizace a celkovou mortalitu pacientů s CKD [38]. Ztráta svalové hmoty vede k dalšímu zvýšení hladiny močoviny v krvi a slinách, zesiluje uremickou halitózu a vede k rozvoji začarovaného kruhu [35]. Kromě vysokých hladin močoviny v séru jsou další faktory, které se pravděpodobně podílejí na nástupu uremické halitózy, zvýšení koncentrace fosforu v séru a změna pH slin [43-45]. Uremická halitóza může být spojena i s pocitem pálení na rtech a jazyku neuropatického původu [46] nebo dokonce s pocitem zvětšeného jazyka.
3.1.2. Změny měkkých tkání ústní dutiny
Jiné orální abnormality, které se často vyskytují u pacientů s CKD, se týkají měkkých tkání dutiny ústní. Pacienti s CKD v pokročilejších stadiích často vykazují normochromní a normocytární anémii, zejména v důsledku deficitu produkce erytropoetinu a zkrácení poločasu červených krvinek. Anémie je základem charakteristické bledosti sliznic, která je často pozorována u pacientů s CKD [47].
Navíc se u pacientů s ESRD může vyskytnout klinický stav známý jako uremická stomatitida. Jedná se o orální komplikaci neznámé etiologie, která je relativně neobvyklá [43,46,48]. Klinicky je uremická stomatitida charakterizována přítomností erytematózních lézí v dutině ústní, které mohou být lokalizované nebo generalizované. Tyto léze jsou pokryty pseudomembranózním exsudátem, který lze odstranit, přičemž zůstane intaktní nebo ulcerovaná sliznice [45]. Uremická stomatitida je určena lézemi, které se často spontánně hojí, ale pro podporu jejich hojení se jako účinná jeví léčba mírně kyselým výplachem, jako je 10procentní peroxid vodíku.
3.1.3. Změny zubní tkáně
V přítomnosti CKD je možné pozorovat anomálie na chrupu. Často se vyskytujícím znakem u pacientů s CKD je hypoplazie skloviny. Je spojena především se změnou metabolismu vápníku a fosforu [48]. Hypoplazie zubní skloviny je patologický stav charakterizovaný nedostatečným vývojem zubní skloviny, která proto představuje kvantitativní deficit a zmenšenou tloušťku. Pacient trpící hypoplazií skloviny má problémy nejen estetického charakteru, ale tento patologický stav může představovat i významný rizikový faktor pro rozvoj závažnějších onemocnění dutiny ústní [47]. Zdraví zubní skloviny je hluboce ovlivněno nutričním stavem pacienta. Nedostatek vitaminu D, vápníku, vitaminu A a přítomnost PEW jsou spojovány s hypoplazií skloviny, stavy, které také vedou ke zvýšené náchylnosti k zubnímu kazu [49]. Hypoplazie skloviny je stav, který se často vyskytuje u dětských pacientů s CKD. Dlouhodobý nedostatek vitaminu A, vitaminu D a vápníku během vývoje zubů může vést k atrofii skloviny a defektní apozici a kalcifikaci dentinu |49]. Zejména Bawden a kol. předpokládali, že hypovitaminóza D vede k nedostatečnému transportu vápníku, což je užitečné pro vývoj zubních tkání [50]. Nedostatek vitaminu D ovlivňuje stavbu zubů a oddaluje jejich fyziologickou erupci. V přítomnosti nedostatku vitaminu D jsou zuby mikroskopicky charakterizovány rozšířenou vrstvou prevence, přítomností interglobulárního dentinu a tvorbou nerovnováhy skloviny [51]. U dospělých pacientů s CKD může naopak hypovitaminóza D vést ke zúžení nebo kalcifikaci dřeňové komory [35].
V současné době neexistuje jednoznačný konsenzus ohledně zvýšeného rizika vzniku zubního kazu u pacientů s CKD [44]. Potenciální antibakteriální účinek byl připisován zvýšení pH slin v důsledku hydrolýzy močoviny slinami, což naznačuje její ochranný účinek proti zubnímu kazu [47l. Naproti tomu nekariózní ztráta zubů je u pacientů s CKD rozšířenější než u běžné populace. Tato ztráta může být vyvolána uremickou gastritidou a gastroezofageálním refluxem, který se často vyskytuje u pacientů s ESRD a může být odpovědný za erozi zubů [35].
3.1.4. Změna kostní tkáně ústní dutiny
U pacientů s CKD jsou další změny v dutině ústní spojeny se změnou metabolismu vápníku a fosforu, abnormálním metabolismem vitaminu D a kompenzační hyperplazií příštítných tělísek, což způsobuje rozvoj CKD-minerální a kostní poruchy (CKD-MBD)[35] ]. Na úrovni dutiny ústní je CKD-MBD charakterizována demineralizací alveolární kosti, redukcí trabekulární kosti, snížením tloušťky kortikální kosti, metastatickými kalcifikacemi měkkých tkání, fibrocystickými lézemi, oblastmi lytické kosti, zlomeninou čelisti (spontánní popř. po stomatologických zákrocích), abnormální hojení kosti po extrakci a někdy i pohyblivost zubů sekundární k úbytku kostní hmoty.

3.2. Účinky renální substituční terapie na zdraví ústní dutiny
Kromě orálních změn způsobených komorbiditami souvisejícími s CKD a samotným CKD mohou být RRT indukovány další anomálie v dutině ústní, jako je dialýza (hemodialýza-HD a peritoneální dialýza) a transplantace ledvin.
3.2.1.Orální změny u dialyzovaných pacientů
U HD pacientů je časté krvácení z ústní sliznice. Může to být způsobeno samotným CKD, jako jsou funkce změny krevních destiček a normochromní a normocytární anémie [52,53], nebo léčba HD. Ten může vyvolat nebo zhoršit stav trombocytopenie způsobený mechanickým poškozením a použitím heparinu během HD procedury. Z těchto důvodů HD predisponuje pacienty k tvorbě modřin, petechií a krvácení v ústní sliznici.
Navíc kvůli sníženému příjmu vody a polyfarmacii se u HD a pacientů na peritoneální dialýze často vyskytuje xerostomie [44]. Xerostomie je charakterizována suchostí dutiny ústní v důsledku nedostatečné sekrece slin nebo úplného nedostatku slin. Na základě své patogeneze je klasifikována jako pravá xerostomie (primární xerostomie), která je důsledkem špatné funkce slinných žláz, nebo pseudoxerostomie, známá také jako symptomatická xerostomie (xerostomia spuria), během níž má pacient subjektivní dojem sucho v ústech navzdory normální funkci slinných žláz [54]. Xerostomie může ovlivnit funkci dutiny ústní a může ohrozit pohodu pacienta. Slinné sekrety jsou životně důležité pro zdraví ústní dutiny, protože se podílejí na mechanickém čištění s ochrannou funkcí. Hyposalivace může také zvýšit riziko orálních infekcí, jako je kandidóza, a náchylnost pacienta k zubnímu kazu, periodontálnímu onemocnění a ztrátě zubů. U HD pacientů epidemiologické studie ukazují, že ústní hygiena je obvykle špatná, takže usazeniny zubního kamene a plaku mohou být zvýšeny [35]. V současné době je v literatuře k dispozici jen málo údajů o vztahu mezi peritoneální dialýzou a CPD.
3.2.2. Orální změny u pacientů po transplantaci ledvin
Pacienti po transplantaci ledvin často podstupují imunosupresivní léčbu, která je činí náchylnějšími k infekcím a rozvoji malignit [55]. Pacienti po transplantaci ledvin jsou proto zranitelnější vůči plísňovým infekcím, včetně Candida albicans, které mohou vyvolat léze sliznice dutiny ústní a periorální dutiny [35]. Jednou z hlavních komplikací plísňových infekcí je úhlová cheilitida, což je zánětlivé onemocnění, které postihuje koutky úst. Úhlová cheilitida je pozorována u více než 4 procent pacientů po transplantaci ledvin. Jiné formy kandidózy byly hlášeny u pacientů po transplantaci ledvin, včetně pseudomembranózní (1,9 procenta), erytematózní (3,8 procenta) a chronické atrofické - nazývané také protetická stomatitida (3,8 procenta).
Mezi virovými infekcemi jsou cytomegalovirus (CMV) a herpes virus simplex (HSV) často spojeny s použitím imunosupresivní terapie. Zejména ulcerace sliznice dutiny ústní je často spojena s infekcí CMV, přičemž se preferují laterální okraje jazyka.
Kromě toho může být u pacientů po transplantaci ledvin pozorován sekundární účinek terapie cyklosporinem, známý jako gingivální přerůstání (GO). GO sekundární po imunosupresivní léčbě je nejvíce studovanou perorální změnou u pacientů po transplantaci ledvin. Bylo pozorováno, že pokud jsou pacienti léčeni kombinací cyklosporinu a nifedipinu, prevalence GO se zvyšuje na 50 procent. Studie Marshalla a kol. zdůraznil, jak k tomuto účinku dochází do 3 měsíců od začátku této farmakologické léčby. Tento přerůst, který normálně začíná na interdentálních papilách, je nejčastější v předních segmentech úst a na labiálních plochách zubů [56]. Zdá se, že GO nemá predilekci pro maxilu nebo mandibulu [35]. Vzhledem k četným vedlejším účinkům cyklosporinu na dutinu ústní byly vyvinuty další terapeutické alternativy. Ve skutečnosti se takrolimus, rapamycin a mykofenolát mofetil používají k nahrazení cyklosporinu. Tyto terapeutické alternativy se vyznačují poklesem GO. Tyto léky jsou však dražší a dosud nejsou známy všechny jejich vedlejší účinky. Z těchto důvodů zůstává v mnoha případech cyklosporin první imunosupresivní terapeutickou možností.
U pacientů po transplantaci ledviny byly také popsány případy maligních lézí, jako je spinocelulární karcinom a Kaposiho sarkom, které by se mohly vyvinout v oblastech GO indukovaných cyklosporinem. Zvýšené riziko maligních lézí v dutině ústní u pacientů po transplantaci ledviny je přímým důsledkem dlouhodobé imunosupresivní léčby.
3.3. Periodontální onemocnění a CKD
CPD je infekční onemocnění způsobené gramnegativními bakteriemi odpovědnými za destrukci podpůrných tkání zubů. Přítomnost těchto bakterií v subgingiválním biofilmu způsobuje uvolňování proteolytických enzymů, schopných degradovat gingivální tkáň 57l. Parodontální patogeny nejen indukují zánět a lokální destrukci ústních tkání, ale jsou také spojovány s nástupem systémového zánětlivého stavu. Zajímavá studie provedená na 359 pacientech s CKD zdůraznila, jak nechirurgická parodontologická léčba indukuje snížení systémového zánětu, monitorovaného prozánětlivými cytokiny [58]. Proto se předpokládá, že léčba CPD u pacientů s CKD může mít pozitivní vliv na oxidační stres (OS) a na systémový zánětlivý stav [16,59] Tyto poslední představují prognostické faktory spojené s náhlějším zhoršením reziduálních renálních funkcí [60 ]. Je tedy možné předpokládat, že CPD může představovat důležitý rizikový faktor pro vznik a progresi CKD58]. Kromě toho se zdá, že úmrtnost pacientů s CKD je v přítomnosti parodontitidy výrazně zvýšena.
Mikrobiální komplexy v subgingiválním biofilmu během CPD byly klasifikovány podle jejich patogenního potenciálu do pěti skupin: červená, zelená, oranžová, žlutá a fialová [61]. Za hlavní a závažnou příčinu CPD byla identifikována červená skupina, kterou tvoří Tannerella forsythia, Treponema identická a Porphyromonas gingivalis [61]. Zdá se, že tyto jevy souvisí s dysbiózou ústní mikroflóry charakterizovanou zvýšenou mikrobiální diverzitou a přítomností anaerobních bakteriálních druhů, což ukazuje na nové potenciální patogenní druhy spojené s CPD, jako je Filifactor alocis, Fretibacterium fastidious a Treponema Vincenti [64,65 ]. Bakterie červeného komplexu a Candida albicans jsou navíc u pacientů s CKD s CPD přítomny častěji než u zdravých jedinců [58]. Proto je nezbytné provádět pravidelné vyšetření dutiny ústní u pacientů s CKD, aby byla umožněna časná diagnóza a rychlá léčba CPD.
Některé z těchto parodontálně-patogenních mikroorganismů hrají přímou roli v progresi CKD. Zejména parodontální bakterie mohou ohrozit zdraví ledvin prostřednictvím několika mechanismů: (i) nepřímých, jako je systémová bakteriémie, která se vyvíjí z ulcerací dásní a která umožňuje patogenním mikroorganismům vstoupit do krevního řečiště, a uvolňování prozánětlivých cytokinů, které jsou odpovědné pro destrukci tkáně; (ii) přímá, jako je destrukce alveolární kosti.
Při zánětu parodontu vede interakce mezi patogenním mikroorganismem a imunitním systémem k sekreci prozánětlivých cytokinů, které následně přitahují další buňky imunitního systému, konkrétněji proti rozpoznanému patogenu, zesilující zánětlivý stav. Cytokiny jsou vylučovány různými buněčnými skupinami a mohou působit jako zesilovače zánětu i jako zodpovědné za přímou destrukci tkáně. Zánětlivé cytokiny zvyšují vaskulární permeabilitu, což zase může zvýšit bakteriémii a stimulovat fibroblasty a zánětlivé buňky, což indukuje uvolňování dalších cytokinů. Během zánětu se také zvyšuje exprese endoteliálních adhezních molekul, jako je intercelulární adhezní molekula (ICAM)-1 a vaskulární buněčná adhezní molekula (VCAM)-1, E-selektin a chemokiny (monocytový chemoatraktant protein -1 a TI8)
Mezi dalšími typickými rysy spojenými s CPD hraje OS klíčovou roli ve vztahu mezi parodontitidou a CKD. U CPD jsou reaktivní formy kyslíku (ROS) důležitým primárním obranným systémem a jsou produkovány zánětlivými buňkami [68]. Je pravděpodobné, že OS má významný dopad na lokální periodontální léze. Účinky OS na systémový zánět byly prokázány několika výzkumnými skupinami. Například tkáňové hladiny 8-hydroxydeoxyguanosinu (8-OHdG), markeru OS, jsou zvýšeny ve více orgánech, jako jsou játra, srdce, ledviny a mozek na zvířecím modelu zánětu parodontu [ 69]. Proto se předpokládá, že rovnováha mezi prooxidačními a antioxidačními druhy je spojena se vznikem, závažností a progresí CPD a jejími systémovými komplikacemi [59].
