1. Cukr nebo tuk? Renální tubulární metabolismus zhodnocen v Health and Disease
Apr 17, 2023
Abstraktní
Ledviny jsou vysoce metabolicky aktivní orgán, který se spoléhá na specializované epiteliální buňky složené z renálních tubulů, které reabsorbují většinu filtrované vody a rozpuštěných látek. Velká část této reabsorpce je zprostředkována proximálním tubulem, který vyžaduje velké množství energie k usnadnění pohybu rozpuštěné látky. Proto proximální tubul využívá oxidaci mastných kyselin jako preferovanou metabolickou cestu a oxidace mastných kyselin produkuje více adenosintrifosfátu (ATP) než metabolismus glukózy. Po poškození ledvin mají metabolické změny za následek sníženou oxidaci mastných kyselin a zvýšenou produkci laktátu. Tento přehled pojednává o metabolických rozdílech mezi proximálním a distálním tubulárním segmentem jednotky zdravé ledviny. Kromě toho jsou diskutovány metabolické změny při akutním poškození ledvin a chronickém onemocnění ledvin a také o tom, jak tyto metabolické změny ovlivňují tubulární opravu a progresi chronického onemocnění ledvin.
Klíčová slova
proximální tubul; akutní poškození ledvin; chronické onemocnění ledvin; oxidace mastných kyselin; poškození ledvin; metabolismus ledvin;Výhody Cistanche.
Úvod
Ledviny přijímají 25 procent srdečního výdeje a filtrují asi 180 litrů vody denně, ale vyloučí pouze 1 - 2 litrů. Kromě toho se přefiltruje více než 1,6 kg soli, ale vyloučí se pouze 3 - 20 g. Kromě glukózy a dalších filtrovaných rozpuštěných látek je vynaloženo mnoho energie na zachování tak velkého procenta vody a soli. Lidská ledvina je komplexní orgán s přibližně 1 milionem nefronů, z nichž každý obsahuje glomerulus a následně tubulární segment. Tubulární kompartment se skládá z proximálních tubulů (segment S1 nejblíže glomerulu, S2 a S3), kolaterál Henleho, distálních stočených tubulů a sběrných kanálků. Renální tubuly jsou zodpovědné za zachování 99 procent vody a rozpuštěných látek v glomerulárním filtrátu a udržování acidobazické rovnováhy. Metabolické požadavky a preference substrátu (např. glukóza a mastné kyseliny) závisí na specifických tubulárních segmentech.
Ledviny mohou být poškozeny akutně ischemií, toxiny, léky a infekcemi nebo chronicky cukrovkou, hypertenzí, glomerulonefritidou nebo těžkým akutním poškozením ledvin. Renální tubuly, zejména proximální tubuly, jsou citlivými místy pro akutní ledvinové (AKI) a chronické onemocnění ledvin (CKD). Existují silné důkazy, že renální tubulární metabolismus je změněn jak u AKI, tak u CKD. Objevující se důkazy naznačují, že náprava některých z těchto metabolických změn může snížit zranění nebo podpořit zotavení, ale zůstává otázka, které metabolické poruchy jsou adaptivní a maladaptivní. Tento přehled bude diskutovat o tom, co je známo o metabolismu zdravých renálních tubulů, jak se tubulární metabolismus mění při poškození ledvin a jak metabolické změny ovlivňují nezodpovězené otázky tubulární reparace a progrese tubulární intersticiální fibrózy (charakteristický znak CKD).

Pro nákup klikněte zdeExtrakt z cistanche
Metabolismus ve zdravých ledvinách
1. Oxidace mastných kyselin
Hlavní buňky odpovědné za velkou reabsorpční kapacitu ledvin jsou proximální tubuly, které recyklují přibližně 70 procent filtrovaných rozpuštěných látek a vody. Pro usnadnění transportu velkého množství vody a rozpuštěných látek jsou zapotřebí transportéry, které spotřebovávají velké množství ATP. Mitochondrie jsou hojné v proximálních tubulech, aby produkovaly potřebný ATP. podobně jako metabolicky aktivní kardiomyocyty jsou proximální tubuly závislé na oxidaci mastných kyselin (FAO), protože tento zdroj paliva poskytuje 106 jednotek ATP, zatímco metabolismus glukózy poskytuje 36 jednotek ATP (obrázek 1A). Většina vnější ledviny nebo kůry se skládá z proximálních tubulů. V souladu s velkým počtem proximálních tubulů rané studie ukázaly, že dvě třetiny spotřeby kyslíku v lidských ledvinách pochází z oxidace mastných kyselin.

Obrázek 1. Metabolismus v neporaněném nefronu a proximálním tubulu. (A) Segment proximálního tubulu má glukoneogenní kapacitu a přednostně využívá oxidaci mastných kyselin k tvorbě ATP. Naproti tomu distální tubuly nemají glukoneogenní potenciál, ale jsou lépe vybaveny pro tvorbu ATP prostřednictvím glykolýzy. (B) Schéma metabolismu v proximálním tubulu ukazující, že glukóza je vychytávána na apikální straně transportéry SGLT1/2 a uvolňována na bazální straně prostřednictvím CLUT1/2. Mastné kyseliny (FA) procházejí plazmatickou membránou přes CD36, proteiny vázající mastné kyseliny (FABP a transportní proteiny mastných kyselin (FATP), přeměňují se na acetyl-CoA a jsou transportovány do mitochondrií přes karnitinový raketoplán zahrnující karnitin palmitoyl-transferázy CPTla a CPT2. Beta oxidace mastného acylu CoA produkuje acetyl-CoA, který vstupuje do cyklu TCA (trikarboxylové kyseliny). Oxidace acetyl-CoA pomocí TCA produkuje NADH, který vstupuje do elektronového transportního řetězce (EIC) a vytváří ATP. Vytvořeno pomocí BioRen-com .
Mastné kyseliny mohou být vychytávány ledvinovými tubuly především prostřednictvím receptorů CD36 exprimovaných na plazmatické membráně, ale také prostřednictvím proteinů vázajících mastné kyseliny (FABP) a transportních proteinů mastných kyselin (FATP) (obrázek 1B). Kromě toho mohou být produkovány syntázou mastných kyselin v cytoplazmě a také metabolismem fosfolipidů fosfolipázou A2. Mastné kyseliny s dlouhým řetězcem (LCFA), jako je kyselina palmitová, vyžadují kyvadlový transport karnitinu do mitochondrií, kde dochází k oxidaci a produkci ATP. Karnitinový člunek se skládá z karnitin palmitoyltransferázy 1 (CPT1) umístěné na vnější mitochondriální membráně, která přeměňuje lipidový acyl CoA na acylkarnitin s dlouhým řetězcem, což umožňuje pohyb do mitochondriální matrix. Enzym karnitin palmitoyltransferáza 2 (CPT2) pak rekonstituuje acyl CoA, který podléhá oxidaci v mitochondriích. Syntetizovaný acetylkoenzym a vstupuje do cyklu trikarboxylové kyseliny (TCA) a je oxidován, což vede k redukci NAD (nikotinamid adenindinukleotid) a FAD (flavinadenindinukleotid) na NADH a FADH. NADH a FADH pak vstupují do elektronového transportu řetězce (ETC) a poskytují elektrony pro generování elektrochemického gradientu vedoucího k produkci ATP.
CPT1 je považován za enzym omezující rychlost oxidace mastných kyselin. existují tři izoformy CPT1 (a, b a c), CPT1a je vysoce exprimován v ledvinách, játrech a dalších orgánech, zatímco CPT1b je převážně exprimován v kosterním svalu, srdci a tukové tkáni a CPT1c je lokalizován v mozku a varlata. Nedávné studie jednobuněčného transkriptomu u dospělých myší a lidských ledvin potvrdily převahu izoformy CPT1a a její obecnou expresi v ledvinách. CPT1 je vyžadován pro mitochondriální import LCFA, ale nikoli pro mastné kyseliny se středně dlouhým řetězcem (MCFA). Na základě studií izotopového značení byly perfundované ledviny potkana schopny přijímat LCFA (palmitát) a MCFA (oktanoát). Mastné kyseliny s velmi dlouhým řetězcem (VLCFA) mohou být oxidovány peroxisomy, ale tyto organely postrádají enzymy dýchacího řetězce, a proto nemohou vytvářet ATP. Naproti tomu produkty peroxizomální oxidace mohou být transportovány do mitochondrií k další oxidaci na acetylkoenzym a a produkci ATP prostřednictvím ETC. Nejvyšší hustota peroxisomů v ledvinách se nachází v proximálním tubulu, což naznačuje, že oxidace proximálních tubulárních mastných kyselin (FAO) může být zprostředkována jak mitochondriemi, tak peroxisomy. Peroxizomální oxidace mastných kyselin s dlouhým řetězcem, jako je kyselina palmitová, může kompenzovat zhoršenou mitochondriální oxidaci, která má důležité důsledky pro poškození ledvin. Ačkoli všechny renální tubulární segmenty jsou schopné oxidovat mastné kyseliny, zdá se, že rychlost oxidace přímo souvisí s mitochondriálním obsahem, který je největší v proximálních tubulárních segmentech a distálních tubulárních segmentech. Vzhledem k omezené schopnosti zdravých proximálních tubulů metabolizovat glukózu je FAO preferovaným energetickým substrátem pro tento tubulární segment.

Doplňky Cistanche
2. Metabolismus glukózy
FAO může být preferovaným energetickým substrátem pro proximální tubul, ale ledviny jsou důležitým orgánem pro reabsorpci, produkci a využití glukózy. Většina přefiltrované glukózy, celkem 180 g za den, je získána jedním ze dvou sodíkově závislých kotransportérů glukózy (SGLT) umístěných na apikálním povrchu proximálního tubulu. SGLT2 je nízkoafinitní, vysokoobjemový transportní protein umístěný primárně v segmentech S1 a S2 proximálního tubulu. SGLT2 spojuje transport sodíku a glukózy v poměru 1:1 a reabsorbuje až 90 procent přefiltrované glukózy. Naproti tomu SGLT1 je vysoce afinitní, nízkoobjemový transportní protein umístěný v segmentu S3 proximálního tubulu, který transportuje sodík a glukózu v poměru 2:1. V posledních letech si SGLT2 získal pozornost jako cíl pro mnoho léků (např. empagliflozin a dapagliflozin), které jsou nefroprotektivní a kardioprotektivní i u pacientů bez diabetu. Mechanismy ochrany proti CKD a srdečnímu selhání zprostředkované SGLT2-přesahují rámec tohoto přehledu, ale zdůrazňují důležitost manipulace s glukózou v ledvinách.
Velké množství glukózy vstupuje do proximálního tubulu, ale jak bylo popsáno dříve, v nepoškozeném proximálním tubulu je metabolizováno jen málo glukózy. Naproti tomu rodina facilitovaných transportních proteinů GLUT se nachází na bazolaterální membráně a umožňuje glukóze pohybovat se po koncentračním gradientu zpět do oběhu. afinitní tok glukózy iniciovaný SGLT2 na apikálním povrchu. Podobně GLUT1 poskytuje výstupní cestu pro glukózu přes SGLT1 do segmentu S3. Proximální tubuly jsou tedy primárně závislé na energii FAO, ale v těchto buňkách dochází k podstatnému toku glukózy a narušení tohoto pohybu glukózy se používá k léčbě CKD a srdečního selhání.
Ledviny a játra jsou jediné dva orgány schopné uvolňovat glukózu do oběhu, protože ostatní tkáně postrádají glukózo 6-fosfatázu, která je nezbytná pro tvorbu glukózo-6-fosfátu. Glukóza může být produkována buď glykogenolýzou nebo glukoneogenezí. Glykogen se při glykogenolýze rozkládá na glukózo-6-fosfát, ale ledviny nemají žádné významné zásoby glykogenu. Při glukoneogenezi mohou substráty jako laktát, glycerol, alanin a glutamin vést k produkci glukózo-6-fosfátu. V ledvinách studie ukázaly, že laktát je hlavním prekurzorem glukoneogeneze. Počáteční studie měření renálních arteriálních a venózních koncentrací glukózy nezjistily velké čisté variace glukózy v ledvinách. Studie využívající izotopicky značenou glukózu však ukázaly, že ledviny produkují a metabolizují značné množství glukózy. Podobné metody u lidí naznačují, že ledviny tvoří přibližně 25 procent veškeré glukózy uvolněné do oběhu. U diabetických pacientů existují důkazy, že glukoneogeneze je dále regulována prostřednictvím ledvin a jater. Tyto výsledky naznačují, že renální glukoneogeneze může být spojena s hyperglykémií u diabetických pacientů. U diabetických pacientů s chronickým onemocněním ledvin může ztráta renální glukoneogenní aktivity vést k hypoglykemickým epizodám a snížené clearance inzulínu v důsledku poruchy funkce ledvin.

Herba Cistanche
Ledviny produkují a spotřebovávají glukózu, ale tyto činnosti jsou striktně rozděleny na specifické typy tubulových buněk. Glukoneogeneze je omezena na proximální tubuly, které exprimují klíčové enzymy nezbytné pro tento proces: glukózo-6-fosfatázu, fosfoenolpyruvátkarboxykinázu (PEPCK) a fruktózu-1,6 -difosfatázu (obrázek 2). Naproti tomu ve zdravých ledvinách je využití glukózy jako metabolického paliva omezeno na distální tubuly. Glykolýza je metabolická přeměna glukózy na pyruvát, který může být dále oxidován nebo metabolizován na laktát prostřednictvím cyklu TCA. Glykolytické enzymy, jako je hexokináza, fosfofruktokináza a pyruvátkináza, jsou nejvíce exprimovány v hrubé ascendentní končetině, distálních a sběrných tubulech. V souladu s hladinami exprese enzymu byly oxidace glukózy a glukoneogeneze ATP významně nižší v proximálních tubulech mikrodisekovaných potkanů než v distálních tubulárních segmentech. Studie prokázaly, že distální tubuly mohou metabolizovat glukózu na laktát i za aerobních podmínek a tato schopnost je značně zvýšena působením antimycinu A, který zabraňuje oxidačnímu dýchání. Naproti tomu v mikrodisekovaných proximálních tubulech krys glukóza produkovala málo laktátu a antimycin A nedokázal vyvolat zvýšený laktát, což naznačuje, že zdravé proximální tubuly mají omezenou schopnost metabolizovat glukózu na laktát. Glukóza je tedy produkována proximálním tubulem prostřednictvím glukoneogeneze, zatímco segment distální renální jednotky je metabolizován glykolýzou.
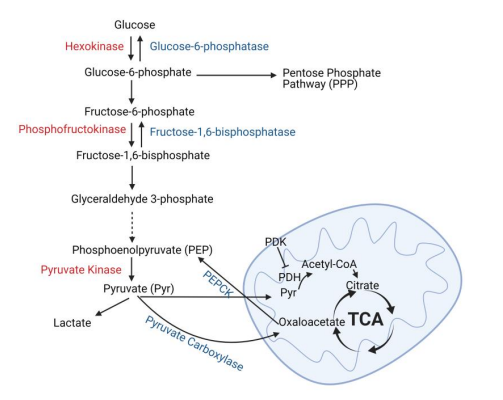
Obrázek 2. Metabolismus a produkce glukózy v ledvinových tubulech. Glukóza je metabolizována na glukózo-6-fosfát, který může vstoupit do pentózofosfátové dráhy nebo být metabolizován na pyruvát (glykolýza). Klíčové enzymy nezbytné pro glykolýzu jsou uvedeny červeně a tyto enzymy jsou převážně exprimovány v distálních tubulech ledviny. Pyruvát může být buď přeměněn na laktát (anaerobní glykolýza), nebo vstoupit do mitochondrií, kde je přeměněn na acetyl-CoA pomocí pyruvátdehydrogenázy (PDH) a oxidován cyklem trikarboxylové kyseliny (TCA). Enzymy spojené s glukoneogenezí jsou znázorněny modře a jejich exprese v ledvinách je omezena na proximální tubuly. Fosfoenolpyruvát karboxykináza (PEPCK), pyruvát dehydrogenáza kináza (PDK). Vytvořeno pomocí BioRender.com.
3. Metabolismus aminokyselin
Téměř 70 g volných aminokyselin denně je filtrováno glomerulem a jejich reabsorpce z lumen je zprostředkována především proximálním tubulem. Aminokyseliny jsou absorbovány do renálních tubulů difúzí, usnadněnou difúzí a aktivním transportem závislým na sodíku. Aminokyselinové transportní proteiny jsou vysoce exprimovány na kartáčkovém okraji lumen proximálního tubulu, ale bazolaterální aminokyselinové transportní proteiny také reabsorbují aminokyseliny pro specifické funkce. Jak bylo uvedeno výše, některé z těchto reabsorbovaných aminokyselin mohou působit jako substráty pro cykloizomerizaci. Kromě toho mohou aminokyseliny vstoupit do cyklu TCA a být oxidovány v různých bodech. Aminokyseliny s rozvětveným řetězcem (BCAA), sestávající z leucinu, valinu a isoleucinu, jsou také důležitými zdroji energie. BCAA podléhají počátečnímu metabolismu transamináz aminotransferázou s rozvětveným řetězcem (BCAT) za vzniku ketokyselin s rozvětveným řetězcem, které jsou pak oxidativně dekarboxylovány komplexem dehydrogenázy ketokyselin s rozvětveným řetězcem (BCKDH). Metabolity BCAA vstupují do cyklu TCA jako acetylkoenzym a nebo sukcinyl metabolity BCAA vstupují do cyklu TCA ve formě acetylkoenzymu a nebo sukcinylkoenzymu a, kde podléhají oxidaci. bCAT a BCKDH jsou exprimovány a aktivní v ledvinách, kde je oxidační tok BCAA vyšší než v jakékoli jiné tkáni kromě srdce a hnědého tuku. Odhaduje se, že přibližně 8-13 procent metabolismu lidských BCAA probíhá v ledvinách.
Metabolismus určitých aminokyselin usnadňuje další biologické funkce nezávislé na produkci energie, jako je úloha metabolismu glutaminu v acidobazické homeostáze. Glutamin může být metabolizován proximálním tubulem na glutamát, který se zase přemění na meziprodukt cyklu TCA -ketoglutarát. Tyto reakce také produkují amoniak, z nichž část vstupuje do moči přes sodík-vodíkový výměník-3 (NHE3), a hydrogenuhličitan, který je reabsorbován do oběhu přes bazolaterální sodík-vázaný bikarbonátový kotransportér, izomer 1A (NBCe{{{{101} 6}}A). Během acidózy je metabolismus glutaminu v proximálních renálních tubulech za vzniku amoniaku a recyklace bikarbonátu upregulován, což pomáhá udržovat acidobazickou homeostázu. Toho je dosaženo upregulací glutaminázy (enzym, který katalyzuje metabolismus glutaminu) a zvýšením exprese proteinů bazolaterálního transportéru glutaminu, aby se zvýšil příjem do proximálního tubulu. Metabolismus ostatních aminokyselin také přispívá k působení amoniaku a reabsorpci bikarbonátu, ale hlavním zdrojem je glutamin.

Standardizované Cistanche
Ledviny jsou důležitým místem pro metabolismus ostatních aminokyselin a hrají důležitou biologickou roli. Citrulin je produkován enterocyty tenkého střeva, absorbován hlavně ledvinami a metabolizován na arginin. Arginin je prekurzorem oxidu dusnatého (NO), který je důležitý pro funkci endotelu a regulaci průtoku krve, ale i další účinky (imunitní odpověď, syntéza bílkovin). Ledviny také přeměňují fenylalanin na tyrosin prostřednictvím fenylalaninhydroxylázy, která je exprimována jak v ledvinách, tak v játrech. Tyrosin hraje důležitou roli při produkci neurotransmiterů a hormonů štítné žlázy a přeměna fenylalaninu na tyrosin je u pacientů s terminálním onemocněním ledvin ve srovnání s normální funkcí ledvin snížena o 50 procent. Toto nejsou jediné příklady významu renálního metabolismu aminokyselin, který byl obšírněji přezkoumán jinými. Ačkoli glukóza a mastné kyseliny mohou být důležitějšími zdroji energie pro zdravé ledviny, metabolismus aminokyselin v ledvinách hraje nedílnou roli v intraorganismální homeostáze.
Reference
1. Marton, A.; Kaneko, T.; Kovalik, J.-P.; Yasui, A.; Nishiyama, A.; Kitada, K.; Titze, J. Ochrana orgánů inhibitory SGLT2: Role ochrany metabolické energie a vody. Nat. Rev. Nephrol. 2021, 17, 65–77.
2. Simon, N.; Hertig, A. Změna oxidace mastných kyselin v buňkách tubulárního epitelu: od akutního poškození ledvin k renální fibrogenezi. Přední. Med. (Lausanne) 2015, 2, 52.
3. Nieth, H.; Schollmeyer, P. Substrátové využití lidské ledviny. Nat. Cell Biol. 1966, 209, 1244–1245.
4. Trimble, ME transport mastných kyselin s dlouhým řetězcem perfuzní ledvinou krys. Kidney Blood Press. Res. 1982, 5, 136–142.
5. Susztak, K.; Ciccone, E.; McCue, P.; Sharma, K.; Böttinger, EP Multiple Metabolic Hits Converge on CD36 jako nový mediátor tubulární epiteliální apoptózy u diabetické nefropatie. PLoS Med. 2005, 2, e45.
6. Murea, M.; Freedman, BI; Parks, JS; Antinozzi, PA; Elbein, SC; Ma, L. Lipotoxicita u diabetické nefropatie: Potenciální role oxidace mastných kyselin. Clin. J. Am. Soc. Nephrol. 2010, 5, 2373–2379.
7. Gai, Z.; Wang, T.; Visentin, M.; Kullak-Ublick, GA; Fu, X.; Wang, Z. Akumulace lipidů a chronické onemocnění ledvin. Živiny 2019, 11, 722.
8. Houten, SM; Violante, S.; Ventura, FV; Wanders, RJ Biochemie a fyziologie mitochondriální be-ta-oxidace mastných kyselin a jejích genetických poruch. Annu. Physiol. 2016, 78, 23–44.
9. Szeto, HH Farmakologické přístupy ke zlepšení mitochondriální funkce u AKI a CKD. J. Am. Soc. Nephrol. 2017, 28, 2856–2865.
10. Wu, H.; Uchimura, K.; Donnelly, EL; Kirita, Y.; Morris, SA; Humphreys, BD srovnávací analýza a upřesnění diferenciace organoidů ledvin odvozených od lidských PSC pomocí jednobuněčné transkriptomiky. Cell Stem Cell 2018, 23, 869–881.
11. Ransick, A.; Lindström, NO; Liu, J.; Zhu, Q.; Guo, J.-J.; Alvarado, GF; Kim, AD; Černá, HG; Kim, J.; McMahon, AP Single-Cell Profiling odhaluje pohlaví, rodokmen a regionální rozmanitost v myší ledvině. Dev. Buňka 2019, 51, 399–413.e7.
12. Trimble, ME Příjem a využití mastných kyselin s dlouhým a středně dlouhým řetězcem perfundovanými ledvinami potkana. Int. J. Biochem. 1980, 12, 173–176.
13. Vasko, R. Peroxisomes and Kidney Injury. Antioxid. Redoxní signál. 2016, 25, 217–231.
14. Le Hir, M.; Dubach, UC Peroxizomální a mitochondriální beta-oxidace v ledvinách potkana: Distribuce aktivit mastné acyl-koenzym A oxidázy a 3-hydroxyacyl-koenzym A dehydrogenázy podél nefronu. J. Histochem. Cyto-chem. 1982, 30, 441–444.
15. Litwin, JA; Völkl, A.; Müller-Höcker, J.; Fahimi, HD Imunocytochemická demonstrace peroxizomálních enzymů v biopsiích lidských ledvin. Vircows Arch. B Cell Pathol. Vč. Mol. Pathol. 1987, 54, 207–213.
16. Violante, S.; Achetib, N.; Van Roermund, CWT; Hagen, J.; Dodatko, T.; Vaz, FM; Waterham, HR; Chen, H.; Baes, M.; Yu, C.; a kol. Peroxisomy mohou oxidovat mastné kyseliny se středním a dlouhým řetězcem cestou zahrnující ABCD3 a HSD17B4. FASEB J. 2019, 33, 4355–4364.
17. Subramanya, AR; Ellison, DH distální stočený tubulus. Clin. J. Am. Soc. Nephrol. 2014, 9, 2147–2163.
18. Guder, WG; Wagner, S.; Wirthensohn, G. Metabolická paliva podél nefronu: Dráhy a intracelulární mechanismy interakce. Kidney Int. 1986, 29, 41–45.
19. Wright, EM; Hirayama, BA; Loo, DF Aktivní transport cukru ve zdraví a nemoci. J. Intern. Med. 2007, 261, 32–43.
20. Aronson, PS; Sacktor, B. Transport d-glukózy membránami kartáčového lemu izolovanými z kůry ledvin. Biochim. Biophys. Acta (BBA) Biomembr. 1974, 356, 231–243.
21. Barfuss, DW; Schäfer, JA Rozdíly v aktivním a pasivním transportu glukózy podél proximálního nefronu. Dopoledne. J. Physiol. Physiol. 1981, 241, F322–F332.
22. Turner, RJ; Morán, A. Heterogenita sodíkově závislých transportních míst D-glukózy podél proximálního tubulu: Důkazy ze studií vezikul. Dopoledne. J. Physiol. Physiol. 1982, 242, F406–F414.
23. Turner, RJ; Moran, A. Další studie heterogenity transportu D-glukózy v proximální tubulární membráně kartáčového lemu. J. Membr. Biol. 1982, 70, 37–45.
24. Quamme, GA; Freeman, HJ Důkaz pro vysoce afinitní transportní systém D-glukózy závislý na sodíku v ledvinách. Dopoledne. J. Physiol. Physiol. 1987, 253, F151–F157.
25. Lee, WS; Kanai, Y.; Wells, RG; Hediger, MA Kotransportér Na plus/glukóza s vysokou afinitou. Přehodnocení funkce a distribuce výrazu. J. Biol. Chem. 1994, 269, 12032–12039.
26. Packer, M.; Anker, SD; Butler, J.; Filippatos, G.; Pocock, SJ; Carson, P.; Januzzi, J.; Verma, S.; Tsutsui, H.; Brueckmann, M.; a kol. Kardiovaskulární a renální výsledky s empagliflflozinem u srdečního selhání. N. Engl. J. Med. 2020, 383, 1413–1424.
27. Heerspink, HJL; Stefansson, BV; Correa-Rotter, R.; Chertow, GM; Greene, T.; Hou, F.-F.; Mann, JF; McMurray, JJ; Lindberg, M.; Rossing, P.; a kol. Dapagliflflozin u pacientů s chronickým onemocněním ledvin. N. Engl. J. Med. 2020, 383, 1436–1446.
28. Dominguez, JH; Camp, K.; Maianu, L.; Garvey, WT Glukózové transportéry krysího proximálního tubulu: Diferenciální exprese a subcelulární distribuce. Dopoledne. J. Physiol. Physiol. 1992, 262, F807–F812.
29. Thorens, B.; Lodish, HF; Brown, D. Diferenciální lokalizace dvou izoforem přenašeče glukózy v ledvinách potkana. Dopoledne. J. Physiol. Physiol. 1990, 259, C286-C294.
30. Stumvoll, M.; Meyer, C.; Mitrakou, A.; Nadkarní, V.; Gerich, JE Renální produkce glukózy a její využití: Nové aspekty u lidí. Diabetologia 1997, 40, 749–757.
31. Meyer, C.; Stumvoll, M.; Dostou, J.; Welle, S.; Haymond, M.; Gerich, J. Renální výměna substrátu a glukoneogeneze u normálních postabsorpčních lidí. Dopoledne. J. Physiol. Metab. 2002, 282, E428–E434.
32. Cersosimo, E.; Judd, RL; Miles, JM Inzulínová regulace renálního metabolismu glukózy u psů při vědomí. J. Clin. Vyšetřování. 1994, 93, 2584–2589.
33. Stumvoll, M.; Chintalapudi, U.; Perriello, G.; Welle, S.; Gutierrez, O.; Gerich, J. Příjem a uvolňování glukózy lidskou ledvinou. Postabsorpční rychlosti a reakce na epinefrin. J. Clin. Vyšetřování. 1995, 96, 2528–2533.
34. Meyer, C.; Woerle, HJ; Dostou, JM; Welle, SL; Gerich, JE Abnormální renální, jaterní a svalový metabolismus glukózy po požití glukózy u diabetu 2. typu. Dopoledne. J. Physiol. Metab. 2004, 287, E1049–E1056.
35. Lee, JB Peterhm Vliv napětí kyslíku na metabolismus glukózy v kůře a dřeni králičích ledvin. Dopoledne. J. Physiol. Obsah 1969, 217, 1464–1471.
36. Lee, JB; Vance, VK; Cahill, GF Metabolismus C14-značených substrátů kůrou a medullou králičích ledvin. Dopoledne. J. Physiol. Obsah 1962, 203, 27–36.
37. Burch, HB; Narins, RG; Chu, C.; Fagioli, S.; Choi, S.; McCarthy, W.; Lowry, OH Distribuce tří enzymů glukoneogeneze při acidóze a hladovění podél nefronu potkana. Dopoledne. J. Physiol. Physiol. 1978, 235, F246–F253.
38. Burch, HB; Lowry, OH; Perry, SG; Fan, L.; Fagioli, S. Vliv věku na distribuci pyruvátkinázy a laktátdehydrogenázy v ledvinách potkana. Dopoledne. J. Physiol. Obsah 1974, 226, 1227–1231.
39. Guder, WG; Ross, BD Distribuce enzymů podél nefronu. Kidney Int. 1984, 26, 101–111.
40. Schmid, H.; Mall, A.; Scholz, M.; Schmidt, U. Nezměněná glykolytická kapacita v ledvinách potkana za podmínek stimulované glukoneogeneze. Stanovení fosfofruktokinázy a pyruvátkinázy v mikrodisekovaných nefronových segmentech hladovějících a acidotických zvířat. Hoppe-Seyler's Zeitschrift für physiologische Chemie 1980, 361, 819–827.
41. Klein, KL; Wang, M.-S.; Torikai, S.; Davidson, WD; Kurokawa, K. Oxidace substrátu izolovanými jednotlivými nefronovými segmenty krysy. Kidney Int. 1981, 20, 29–35.
42. Uchida, S.; Endou, H. Specifičnost substrátu pro udržení buněčného ATP podél myšího nefronu. Dopoledne. J. Physiol. Physiol. 1988, 255, F977–F983.
43. Bagnasco, S.; Dobře, D.; Balaban, R.; Burg, M. Produkce laktátu v izolovaných segmentech nefronu potkana. Dopoledne. J. Physiol. Physiol. 1985, 248, F522–F526.
44. Young, GA Aminokyseliny a ledviny. Amino Acids 1991, 1, 183–192.
45. Verrey, F.; zpěvák, D.; Ramadan, T.; Vuille-Dit-Bille, RN; Mariotta, L.; Camargo, SMR Přenos aminokyselin ledvinami. Pflflügers Arch. Eur. J. Physiol. 2009, 458, 53–60.
46. Neinast, MD; Jang, C.; Hui, S.; Murashige, DS; Chu, Q.; Morscher, RJ; Li, X.; Zhan, L.; White, E.; Anthony, TG; a kol. Kvantitativní analýza celotělového metabolického osudu aminokyselin s rozvětveným řetězcem. Cell Metab. 2019, 29, 417–429.e4.
47. Suryawan, A.; Hawes, JW; Harris, RA; Shimomura, Y.; Jenkins, AE; Hutson, SM Molekulární model lidského metabolismu aminokyselin s rozvětveným řetězcem. Dopoledne. J. Clin. Nutr. 1998, 68, 72–81.
48. Weiner, ID; Mitch, WE; Sands, JM Metabolismus močoviny a amoniaku a kontrola renálního vylučování dusíku. Clin. J. Am. Soc. Nephrol. 2014, 10, 1444–1458.
49. Moret, C.; Dave, MH; Schulz, N.; Jiang, JX; Verrey, F.; Wagner, CA Regulace renálních přenašečů aminokyselin během metabolické acidózy. Dopoledne. J. Physiol. Renální Physiol. 2007, 292, F555–F566.
50. Brosnan, ME; Brosnan, JT Renální metabolismus argininu. J. Nutr. 2004, 134, 2791S–2795S.
51. Kopple, JD Metabolismus fenylalaninu a tyrosinu při chronickém selhání ledvin. J. Nutr. 2007, 137, 1586S–1590S.
52. Boirie, Y.; Albright, R.; Bigelow, M.; Nair, KS Porucha přeměny fenylalaninu na tyrosin v konečném stadiu renálního onemocnění způsobujícího nedostatek tyrosinu. Kidney Int. 2004, 66, 591–596.
53. van de Poll, MC; Soeters, PB; Deutz, NE; Fearon, KC; Dejong, CH Renální metabolismus aminokyselin: Jeho role v meziorgánové výměně aminokyselin. Dopoledne. J. Clin. Nutr. 2004, 79, 185–197.
Klikněte sem a přečtěte si část Ⅱ.
