Část Ⅱ: Onemocnění ledvin a riziko demence: Dánská celostátní kohortová studie
Apr 10, 2023
Výsledek
Studijní kohorta se skládala z kohorty s onemocněním ledvin 82 690 pacientů s onemocněním ledvin a srovnávací kohorty 413 405 odpovídajících jedinců z obecné populace bez onemocnění ledvin. Střední věk byl 69 let (IQR: 56-78 let). Ženy tvořily 41 procent všech účastníků, přičemž 71 procent se zapsalo mezi 2004 - 2016 a zbývajících 29 procent se zapsalo mezi 1995 - 2003. KVO a KVO rizikové faktory byly diagnostikovány mnohem častěji v kohortě renálního onemocnění ve srovnání se srovnávací kohortou. Kromě toho měla skupina s onemocněním ledvin nižší příjem, vyšší nezaměstnanost a nižší dosažené vzdělání. Doba sledování byla kratší ve skupině s onemocněním ledvin než v kontrolní skupině, s mediánem 3,7 a 5,2 roku. Tento rozdíl odráží vyšší míru úmrtnosti ve skupině s onemocněním ledvin než v kontrolní skupině:{16}}roční a 10-letá úmrtnost byla u pacientů s onemocněním ledvin dvakrát vyšší než v běžné populaci (obrázek 2 ). Během sledovaného období zemřelo 466 071 (94 procent), 78 555 (95 procent) v kohortě s onemocněním ledvin a 387 516 (94 procent) ve srovnávací kohortě.
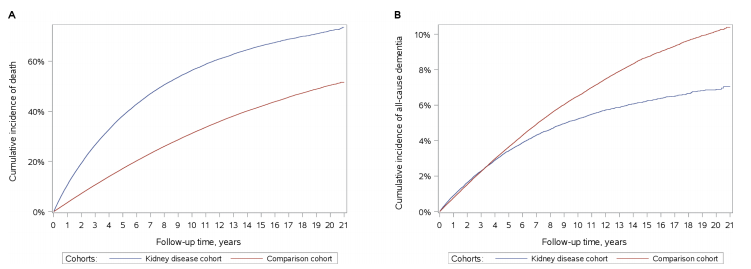
Obrázek 2 Kumulativní incidence (A) úmrtí a (B) demence ze všech příčin u pacientů s onemocněním ledvin (kohorta onemocnění ledvin) a jedinců v odpovídající populaci bez onemocnění ledvin (srovnávací kohorta).
Onemocnění ledvin a riziko rozvoje demence
Během sledování se u 3 462 (4,19 procenta z 82 690) pacientů s onemocněním ledvin a u 21 879 (5,29 procenta ze 413 405) pacientů ve srovnávací kohortě rozvinula demence, z nichž většina byla klasifikována jako jiná demence. Alzheimerova choroba byla častější ve srovnávací kohortě a vaskulární demence byla častější v kohortě s onemocněním ledvin.
5-, 10- a 22-roční riziko demence ze všech příčin bylo nižší u pacientů s onemocněním ledvin než u běžné populace: 2,90 procenta (95 procent CI 2,78 procenta až 3,08 procenta) , 4,96 procenta (4,79 procenta až 5,14 procenta) a 7,05 procenta (6,70 procenta až 7,41 procenta) ve skupině s onemocněním ledvin a 2,98 procenta (2,92 procenta až 3,04 procenta), 6,03 procenta (5,94 procenta až 6,12 procenta) a 1017 procenta (1017 procenta) procent na 10,60 procent) (obrázek 2).
Nejnižší odhadovanou hodnotu měl subtyp demence Alzheimerovy choroby a nejvyšší odhadovanou hodnotu vaskulární demence.
Upravená HR (aHR) pro demenci ze všech příčin zůstala v průběhu času stabilní. 1.06 (1.{4}} až 1,12) při sledování až 5 let, 1,08 (1,03 až 1,13) při sledování až 10 let a 1,08 (1,03 až 1.12) až po 22 letech sledování. Když jsme omezili expozici nefropatie na chronické onemocnění ledvin, aHR pro demenci ze všech příčin byla 1,04 (0,98 až 1,10) po dobu až 22 let sledovánía velmi podobné pro kratší sledování
V analýzách stratifikovaných podle věku se HR pro demenci ze všech příčin progresivně snižovala s věkem: 1,14 (0.78 - 1,67), 1,32 (1.09 - 1,61), 1,16 (1 .08 - 1.24), 1.{18}}1 ( 0.95 - 1.08) a 0,90 (0.77 - 1.04 ). Nebyly zjištěny žádné rozdíly v prevalenci demence ze všech příčin podle pohlaví, kalendářního roku data indexu nebo socioekonomických faktorů. Onemocnění ledvin bylo také spojeno se zvýšenou HR pro demenci ve většině podskupin KVO (infarkt myokardu, mrtvice, onemocnění periferních tepen, žilní tromboembolismus, srdeční selhání a onemocnění srdečních chlopní) a rizikové faktory KVO (fibrilace síní, hypertenze, obezita a diabetes) , ale odhady byly nepřesné. Výsledky pro subtypy demence ukázaly konzistentní výsledky.

Pro získání klikněte semvýhody Cistanchepro ledviny
Závažnost onemocnění ledvin a riziko rozvoje demence
V kohortě s onemocněním ledvin se u méně pacientů s terminálním onemocněním ledvin během sledování vyvinula demence ve srovnání s pacienty s jinými onemocněními ledvin: 3,3 procenta (61 z 1 866) pacientů léčených dialýzou nebo transplantací ledvin a 4,2 procenta (3 401 z 80 982 ) pacientů, kteří tyto zákroky nepodstoupili.
Diskuse
V této národní studii zahrnující téměř 500{1}} účastníků jsme zjistili, že diagnóza onemocnění ledvin byla spojena s mírně zvýšeným rizikem rozvoje demence v budoucnu. Tato asociace byla podobná, když jsme omezili expozici pouze chronickému onemocnění ledvin.
Zjistili jsme mnohem menší odhad ve srovnání s jedinou předchozí populační studií, kde výzkumníci na Tchaj-wanu zjistili HR 1,41 pro demenci ze všech příčin u pacientů s onemocněním ledvin ve srovnání s běžnou populací (1,32 až 1,50). část k rozdílům mezi asijskou a evropskou populací, k rozdílům v designu studie nebo k obojímu. Naše studie zahrnovala novější data, 5krát více účastníků, přesnější shodu podle věku a delší dobu sledování. Kromě toho jsme do definice onemocnění ledvin zahrnuli dialyzační léčbu, transplantaci ledvin a hypertenzní nefropatii a nevyloučili jsme účastníky na základě jiných diagnóz souvisejících s ledvinami. Naproti tomu tchajwanská studie tyto pacienty a několik dalších diagnóz souvisejících s ledvinami vyloučila. Naše studie tedy mohla zahrnovat relativně velký počet pacientů s těžkým onemocněním ledvin do kohorty s onemocněním ledvin a pacientů s lehkým onemocněním ledvin do srovnávací kohorty. A konečně, ačkoli jsme vyloučili pacienty s diagnostikovanou demencí do 1 roku od diagnózy onemocnění ledvin, což nebylo provedeno v tchajwanské studii, poměr incidence v této populaci s méně než 2 roky sledování byl významně vyšší než incidence poměr frekvence s 2 a více lety sledování.
Metaanalýza průřezových a kohortových studií zahrnujících více než 50000 účastníků prokázala souvislost mezi onemocněním ledvin (eGFR < 60 ml/min/1,73 m2) a kognitivní poruchou Primárně ovlivněné kognitivní domény (tj. orientace pozornost, tvorba konceptu a uvažování) se liší od těch, které jsou postiženy demencí, což naznačuje, že asociace onemocnění ledvin a jiných kognitivních poruch může být silnější než asociace s demencí. Data o kognitivní výkonnosti bohužel nemáme.
Je zajímavé, že studie, které primárně zahrnovaly měření eGFR v normálním rozmezí, ukázaly silnější spojení mezi proteinurií a demencí než mezi eGFR a demencí. Toto zjištění naznačuje, že proteinurie může být lepším markerem pokročilého onemocnění ledvin než eGFR. Bohužel nemáme žádné údaje o proteinurii nebo eGFR.

Bylinná cistanche
Neexistence silné souvislosti mezi onemocněním ledvin a demencí může být částečně způsobena vysokou úmrtností pacientů s onemocněním ledvin, a tedy existencí předsudku o přežití, že demence narůstá s věkem a že pacienti s onemocněním ledvin nemusí žít dostatečně dlouho. k rozvoji demence. Ve skutečnosti byla demence diagnostikována u nižšího podílu pacientů s těžkým onemocněním ledvin než u pacientů s mírným onemocněním ledvin (3,3 procenta pacientů léčených dialýzou nebo transplantací ledvin a 4,2 procenta pacientů, kteří tyto intervence nepodstoupili). Toto zjištění může odrážet zkreslení týkající se přežití nebo může naznačovat, že lékaři častěji poddiagnostikují demenci v přítomnosti život ohrožujícího onemocnění a zkrácené délky života (detekční zkreslení). Tento závěr je dále podpořen naší stratifikovanou analýzou, která naznačuje, že odhady rizika jsou nižší v přítomnosti kardiovaskulárního onemocnění (např. infarktu myokardu), rizikového faktoru kardiovaskulárního onemocnění, o kterém je známo, že je spojen se zvýšenou úmrtností. pacienti s infarktem myokardu na 1 573 193 jedincích v obecné populaci uvedli, že infarkt myokardu byl spojen s vysokým rizikem vaskulární demence spojené s demencí ze všech příčin nebo rizikem pro jiné podtypy Souhrnně tato zjištění naznačují, že lékaři mohou s větší pravděpodobností diagnostikovat vaskulární demence u pacientů s demencí, onemocněním ledvin nebo infarktem myokardu a s menší pravděpodobností diagnózy Alzheimerovy choroby než u pacientů bez těchto poruch, a proto může docházet k chybné klasifikaci subtypů demence.
Vzhledem k tomu, že HR se mohou v průběhu času měnit, mírná souvislost pozorovaná mezi onemocněním ledvin a demencí může být omezena na několik prvních let po diagnóze onemocnění ledvin. Na druhou stranu, HR manažeři pro konkrétní období jsou v naší studii náchylní k inherentnímu výběrovému zkreslení, což se promítá do upřednostňování kontroly pacientů kvůli úmrtí pro sledování od začátku kohorty s onemocněním ledvin. Jak se doba sledování prodlužuje, může to vést k relativnímu zvýšení podílu jedinců citlivých na demenci ve srovnávací kohortě, což vysvětluje, proč se neupravené HR s prodlužující se dobou sledování zmenšují. Kvůli tomuto vestavěnému zkreslení výběru nebylo možné zachovat shody, takže jsme do upravených analýz zahrnuli odpovídající kovariáty. To může vysvětlovat, proč se neupravená HR s prodlužující se dobou sledování zmenšuje, zatímco HR se s prodlužující se dobou sledování nezmenšuje.
Hlavní předností naší studie je její design: Velká kohortová studie národního registru s daty na individuální úrovni a kompletním sledováním odpovídající srovnávací kohorty obecné populace všech dánských pacientů s nemocničně diagnostikovaným onemocněním ledvin a bez onemocnění ledvin během studie období 1995 až 2016.
Mezi omezení této studie patří výběrové zkreslení, zkreslení přežití a zkreslení sledování. Vyloučení účastníků s chybějícími hodnotami může zkreslit naše odhady, protože jsme neprovedli vícenásobné imputace pro příjem, status zaměstnání a úroveň vzdělání. Pokud však chybějící hodnoty nejsou náhodné, došlo by pouze ke zkreslení odhadů. Pokud jsou chybějící hodnoty spojeny s nižší úrovní příjmů, zaměstnanosti a vzdělání, pak mohou být nezkreslené odhady větší. Dalšími omezeními jsou chybná klasifikace (onemocnění ledvin, demence a kovariáty), neměřené nebo reziduální zmatení, kvalita kódování a diagnostická validita. Byla hlášena pozitivní prediktivní hodnota 100 procent pro onemocnění ledvin kódované v dánském národním registru pacientů, zatímco úplnost může být pouze 37 procent; to znamená, že nebyli zachyceni všichni pacienti s onemocněním ledvin. Přestože pozitivní prediktivní hodnoty pro demenci ze všech příčin a Alzheimerovu chorobu v Dánském národním registru pacientů byly 86 procent a 81 procent, v daném pořadí, pozitivní prediktivní hodnoty pro ostatní podtypy demence byly nižší.

Doplňky Cistanche
Výsledky týkající se subtypů demence by proto měly být interpretovány opatrně. Toto upozornění je zvláště důležité, protože naše výsledky jsou v souladu s nesprávnou klasifikací identifikace subtypů demence u pacientů s onemocněním ledvin, kde jsou vaskulární rizikové faktory zvláště časté a vaskulární riziko je v běžné populaci nízké. Jako datum všech diagnóz jsme navíc použili datum přijetí nebo zahájení ambulantního sledování, protože přesné termíny nebyly k dispozici. To mohlo vést k zkreslení, zejména na začátku sledování. Kromě toho existuje proměnná doba zpoždění mezi začátkem demence a datem diagnózy. A konečně, protože všechny diagnózy zaznamenávají nemocniční lékaři, mírné onemocnění ledvin a mírná demence léčená pouze praktickými lékaři by se nezaznamenávala, pokud by nebyly také hodnoceny v nemocnici nebo ambulantně.
Závěrem lze říci, že u pacientů s diagnózou onemocnění ledvin je mírně zvýšené riziko, že jim bude diagnostikována budoucí demence. Tato asociace je primárně řízena diagnózou vaskulární demence, která může být omezena na několik prvních let po diagnóze onemocnění ledvin. Na druhou stranu u pacientů s onemocněním ledvin nemusí být demence diagnostikována kvůli vysoké mortalitě a dalším komorbiditám s vyšší prioritou a skutečné riziko budoucí demence může být poněkud vyšší, než naznačuje naše studie.
Standardizované Cistancheje výborným doplňkem pro ty, kteří trpí onemocněním ledvin nebo chtějí zlepšit své zdraví ledvin. Jeho schopnost zlepšovat funkci ledvin, chránit před oxidativním stresem, snižovat záněty a mít mírný diuretický účinek z něj činí cenný nástroj v boji proti onemocněním souvisejícím s ledvinami. Stejně jako u každého doplňku je nezbytné, abyste se před zahájením užívání přípravku Cistanche poradili se zdravotníkem.

Účinky Cistanche na ledviny
REFERENCE
1. Arvanitakis Z, Shah RC, Bennett DA. Diagnostika a léčba demence: přehled. JAMA 2019;322:1589–99.
2. Knopman DS. Záhada snižování výskytu demence. JAMA Netw Open 2020;3:e2011199.
3. World Alzheimer Report 2015: globální dopad demence: analýza prevalence, incidence, nákladů a trendů. ročník 2020, 2015.
4. Spolupráce GBD na chronické onemocnění ledvin. Globální, regionální a národní zátěž chronickým onemocněním ledvin, 1990-2017: systematická analýza studie globální zátěže nemocí z roku 2017. Lancet 2020;395:709–33.
5. Barnes DE, Yaffe K. Předpokládaný účinek snížení rizikových faktorů na prevalenci Alzheimerovy choroby. Lancet Neurol 2011;10:819–28.
6. Ikram MA, Vernooij MW, Hofman A, et al. Funkce ledvin souvisí s onemocněním malých cév mozku. Mrtvice 2008;39:55–61.
7. Bugnicourt JM, Godefroy O, Chillon JM a kol. Kognitivní poruchy a demence u CKD: opomíjená osa ledvina-mozek. J Am Soc Nephrol 2013;24:353–63.
8. Cheng KC, Chen YL, Lai SW, a kol. Pacienti s chronickým onemocněním ledvin mají zvýšené riziko demence: populační kohortová studie na Tchaj-wanu. BMC Nephrol 2012;13:129.
9. Deckers K, Camerino I, van Boxtel MPJ a kol. Riziko demence u renální dysfunkce: systematický přehled a metaanalýza prospektivních studií. Neurologie 2017;88:198–208.
10. Gabin JM, Romundstad S, Saltvedt I, et al. Středně zvýšená albuminurie, chronické onemocnění ledvin a incidentní demence: studie HUNT. BMC Nephrol 2019;20:261.
11. Takae K, Hata J, Ohara T, et al. Albuminurie zvyšuje riziko Alzheimerovy choroby i vaskulární demence u japonských starších lidí žijících v komunitě: studie Hisayama. J Am Heart Assoc 2018;7.
12. Paterson EN, Williams MA, Passmore P, a kol. Odhadovaná rychlost glomerulární filtrace není spojena s Alzheimerovou chorobou v kohortě ze Severního Irska. J Alzheimers Dis 2017;60:1379–85.
13. Berger I, Wu S, Masson P, a kol. Poznání u chronického onemocnění ledvin: systematický přehled a metaanalýza. BMC Med 2016;14:206.
14. Heide-Jørgensen U, Adelborg K, Kahlert J, et al. Strategie odběru vzorků pro výběr kohort pro srovnání obecné populace. Clin Epidemiol 2018;10:1325–37.
15. Mors O, Perto GP, Mortensen PB. Dánský centrální psychiatrický výzkumný registr. Scand J Public Health 2011;39:54–7.
16. Schmidt M, Schmidt SAJ, Sandegaard JL, et al. Dánský národní registr pacientů: přehled obsahu, kvality dat a výzkumného potenciálu. Clin Epidemiol 2015;7:449–90.
17. Schmidt M, Schmidt SAJ, Adelborg K, et al. Dánský systém zdravotní péče a epidemiologický výzkum: od kontaktů na zdravotní péči po záznamy v databázi. Clin Epidemiol 2019;11:563–91.
18. Levey AS, de Jong PE, Coresh J, et al. Definice, klasifikace a prognóza chronického onemocnění ledvin: zpráva kontroverzní konference KDIGO. Kidney Int 2011;80:17–28.
19. Phung TKT, Andersen BB, Høgh P a kol. Platnost diagnóz demence v registrech dánské nemocnice. Dement Geriatr Cogn Disord 2007;24:220–8.
20. Webster AC, Nagler EV, Morton RL, a kol. Chronické onemocnění ledvin. Lancet 2017;389:1238–52.
21. Pottegård A, Schmidt SAJ, Wallach-Kildemoes H, et al. Profil zdroje dat: Dánský národní registr receptur. Int J Epidemiol 2017;46:798–798f.
22. Petersson F, Baadsgaard M, Thygesen LC. Dánské registry o osobní příslušnosti na trhu práce. Scand J Public Health 2011;39:95–8.
23. Guerville F, De Souto Barreto P, Coley N, a kol. Funkce ledvin a kognitivní pokles u starších dospělých: zkoumání role neurodegenerace. J Am Geriatr Soc 2021;69:651-659.
24. Hernán MA. Rizika poměrů rizik. Epidemiologie 2010;21:13–15.
25. Yusuf S, Joseph P, Rangarajan S, et al. Upravitelné rizikové faktory, kardiovaskulární onemocnění a úmrtnost u 155 722 jedinců z 21 zemí s vysokými, středními a nízkými příjmy (PURE): prospektivní kohortová studie. Lancet 2020;395:795–808.
26. Sundbøll J, Horváth-Puhó E, Adelborg K, et al. Vyšší riziko vaskulární demence u pacientů po infarktu myokardu. Náklad 2018;137:567–77.
27. Thygesen SK, Christiansen CF, Christensen S, et al. Prediktivní hodnota diagnostického kódování ICD-10 používaná k posouzení podmínek Charlsonova indexu komorbidity v populačním dánském národním registru pacientů. BMC Med Res Methodol 2011;11:83.
28. Winkelmayer WC, Schneeweiss S, Mogun H a kol. Identifikace jedinců s CKD z údajů o nárocích Medicare: ověřovací studie. Am J Kidney Dis 2005;46:225–32.
29. Vestergaard SV, Christiansen CF, Thomsen RW a kol. Identifikace pacientů s CKD v lékařských databázích: srovnání různých algoritmů. Clin J Am Soc Nephrol 2021;16:543–51.
Alisa D Kjaergaard1,2,Benjamin R Johannesen2Henry T Sørensen2,3Victor W Henderson2,4,Christian F Christiansen2
1. Steno Diabetes Center Aarhus, Aarhus University Hospital, Aarhus, Dánsko
2. Oddělení klinické epidemiologie, Aarhus University Hospital, Aarhus, Dánsko
3. Excellence Research Center, Stanford University, Stanford, Kalifornie, USA
4. Ústav epidemiologie a populačního zdraví a neurologie a neurologických věd, Stanford University, Stanford, Kalifornie, USA
