Část první Dysfunkce endoteliálních buněk a zvýšené kardiovaskulární riziko u pacientů s chronickým onemocněním ledvin
Jun 07, 2023
Abstraktní
Endotel je považován za strážce cévní stěny, který udržuje a reguluje vaskulární integritu. U pacientů s chronickým onemocněním ledvin jsou funkce ochranných endoteliálních buněk narušeny v důsledku prozánětlivého, protrombotického a uremického prostředí způsobeného poklesem funkce ledvin, což přispívá k nárůstu kardiovaskulárních komplikací u této zranitelné populace pacientů. V tomto přehledu diskutujeme o fungování endoteliálních buněk ve zdravých podmínkách a příspěvku dysfunkce endoteliálních buněk ke kardiovaskulárním onemocněním. Dále shrnujeme fenotypové změny endotelu u pacientů s chronickým onemocněním ledvin a vztah dysfunkce endoteliálních buněk ke kardiovaskulárnímu riziku u chronického onemocnění ledvin. Také přezkoumáváme mechanismy, které jsou základem endoteliálních změn u chronického onemocnění ledvin, a zvažujeme potenciální farmakologické intervence, které mohou zlepšit endoteliální zdraví.
Klíčová slova
ateroskleróza, kardiovaskulární onemocnění, chronická onemocnění ledvin, endoteliální buňky, ztuhlost cév.

Kliknutím sem zakoupíte doplněk Cistanche
ZVÝŠENÉ KARDIOVASKULÁRNÍ RIZIKO PŘI CHRONICKÉM ONEMOCNĚNÍ LEDVIN
Chronické onemocnění ledvin (CKD) je definováno poškozením ledvin nebo sníženou filtrační funkcí ledvin (rychlost glomerulární filtrace<60 mL/minute per 1.73 m²) for a period beyond 3 months that affects health.1 With a global prevalence of ≈13.4%,2 CKD imposes a serious burden on our socioeconomic and healthcare system. CKD is a progressive disease, classified into stages 1 to 5 based on the reduction in kidney function (Figure 1A).1 In end-stage kidney disease (CKD stage 5: glomerular filtration rate <15 mL/minute per 1.73 m²), patients require kidney support therapy as dialysis or kidney transplantation to replace the failing kidney function.

Je třeba poznamenat, že pacienti se středně pokročilým až pokročilým CKD mají zvýšené kardiovaskulární riziko ve srovnání s běžnou populací a pacienti s mírným CKD, s nižší odhadovanou rychlostí glomerulární filtrace a vyšší albuminurií identifikovanými jako rizikové faktory pro všechny příčiny a kardiovaskulární mortalitu, nezávisle na tradiční kardiovaskulární rizikové faktory.5,6 Celkově 33,3 % až 37,1 % pacientů s CKD3(a/b) a 39,9 % pacientů s CKD4 umírá na kardiovaskulární onemocnění (CVD) ve srovnání s 21,7 % až 26 % běžné populace (obrázek 1B). 3 U pacientů s terminálním onemocněním ledvin ve věku 25 až 34 let je roční úmrtnost dokonce 500 až 1000krát vyšší ve srovnání s podobně starými kontrolami se zdravou funkcí ledvin a je srovnatelná s 85-letými v běžné populaci, podtrženo vysoká kardiovaskulární zátěž u CKD.6
V obecné populaci jsou infarkt myokardu a cerebrovaskulární příhody nejdůležitějšími kardiovaskulárními příčinami úmrtí, které jsou základem ≈ 75 procent všech úmrtí souvisejících s KVO (obrázek 1C).4 Také u pacientů s CKD5 na dialýze (CKD5D) zůstávají tyto typy KVO důležité, protože představují 45 procent (infarkt myokardu) a 13 procent (cerebrovaskulární příhody) úmrtí z kardiovaskulárních příčin, ačkoli se společnou odpovědností ≈ 58 procent všech úmrtí souvisejících s KVO, jejich relativní význam je ve srovnání s obecnou populace. Místo toho pacienti s CKD5D vykazují relativní nárůst náhlé srdeční smrti a srdečního selhání, které jsou zodpovědné za 28 procent a 9 procent všech úmrtí souvisejících s KVO ve srovnání s 2 procenty a 7 procenty, jak je pozorováno u běžné populace (obrázek 1C). odhaluje vysoký nárůst zejména rizika náhlé srdeční smrti u pokročilého CKD.4
1. Ateroskleróza a infarkt myokardu
Hlavní příčinou jak infarktu myokardu, tak cévní mozkové příhody je ateroskleróza, zánětlivé onemocnění středních až velkých tepen vyvolané lipidy, které spouští vývoj aterosklerotických lézí.7 Tyto léze postupně rostou a mohou nakonec omezit průtok krve nebo vyvolat trombózu ruptura nebo eroze plátu.7,8 Pacienti s CKD3-5D vykazují zvýšenou prevalenci subklinických aterosklerotických lézí ve srovnání s běžnou populací, s větším nárůstem pokročilejších stadií CKD po úpravě podle pohlaví, věku a diabetu. 9,10 Kromě toho ve srovnání s pacienty bez progrese CKD vykazovali pacienti s progresí CKD v průběhu 24 měsíců častěji také progresi aterosklerotických lézí detekovaných ultrazvukem.10,11 Po akutním infarktu myokardu vykazují pacienti s CKD v průběhu času snížené přežití ve srovnání s pacienty bez CKD se zvýšeným rizikem úmrtí a také nefatálních srdečních příhod se zvyšujícím se stádiem CKD.12
2. Náhlá srdeční smrt a uremická kardiomyopatie
V běžné populaci je ischemická choroba srdeční odpovědná za 80 procent náhlých srdečních úmrtí.13 Neúměrný nárůst náhlé srdeční smrti u pacientů s pokročilým CKD naznačuje rozdíly v její patofyziologii a příčinách poklesu funkce ledvin. Hypertrofie levé komory je významně spojena se zvýšeným rizikem náhlé srdeční smrti v běžné populaci14 a může být způsobena srdečním preloadem (intravaskulární objemové přetížení), srdečním afterloadem (tlakové přetížení) nebo afterloadem/preload nezávislými faktory.15 Pacienti s CKD se častěji projevuje hypertrofií levé komory, s prevalencí až 40 procent a dokonce 75 procent u pacientů s CKD5D.16 Spolu se srdeční fibrózou je hypertrofie levé komory jedním z charakteristických znaků uremické kardiomyopatie a může vyvolat srdeční elektrické poruchy a letální arytmie.15

Cistanche tubulosa
3. Endoteliální (buněčná) dysfunkce jako přispěvatel ke kardiovaskulárnímu riziku
Hlavním přispěvatelem ke zvýšenému kardiovaskulárnímu riziku je dysfunkce endoteliálních buněk, která zahrnuje celou řadu maladaptivních změn ve funkčním fenotypu endoteliálních buněk spojených se zvýšeným kardiovaskulárním rizikem. Tento termín byl navržen ve vynikajícím přehledu Gimbrone et al17, aby poskytl odlišení od užšího termínu „endoteliální dysfunkce“, který se obvykle používá k označení endoteliálních abnormalit spouštějících snížení biologické dostupnosti oxidu dusnatého a související vaskulární relaxaci. Významná endoteliální heterogenita existuje napříč vaskulárním stromem, například při porovnávání tepen versus žíly, stejně jako mikrovaskulatury (včetně velkých elastických a svalových konduitních tepen) versus mikrovaskulatury (včetně kapilár, arteriol a venul) a obojí dysfunkce endoteliálních buněk na makro- a mikrovaskulární úrovni přispívá ke zvýšenému kardiovaskulárnímu riziku. V tomto přehledu diskutujeme o příspěvku dysfunkce endoteliálních buněk ke KVO se zvláštním zaměřením na pacienty s CKD. Revidujeme poznatky o molekulárních mechanismech, které jsou základem dysfunkce endoteliálních buněk u CKD, a diskutujeme také o dopadu farmakologických intervencí.
DYSFUNKCE ENDOTELIÁLNÍCH BUNĚK JAKO PŘISPĚVEK KE KARDIOVASKULÁRNÍMU RIZIKU
1. Dysfunkce endoteliálních buněk a aterosklerotické riziko
Vrstva endoteliálních buněk vaskulatury poskytuje semipermeabilní bariéru umožňující regulovanou výměnu tekutin, molekul a buněk a hraje důležitou roli při udržování zdraví cév (obrázek 2). Dysfunkce makrovaskulárních endoteliálních buněk je časnou událostí ve vývoji aterosklerotických lézí. Na jedné straně je ovlivněna hemodynamickými faktory: v oblastech arterií odolných vůči ateroskleróze přispívá laminární proudění krve k protektivnímu fenotypu endoteliálních buněk. Oblasti arteriální vaskulatury náchylné k ateroskleróze jsou však vystaveny narušenému, oscilačnímu průtoku krve a souvisejícímu nízkému časově zprůměrovanému smykovému stresu, který vyvolává oxidační stres, endoteliální fenotypové změny a změny buněčných spojů a také obrat endoteliálních buněk (jak bylo diskutováno podrobněji v přehledu Gimbrone et al17). Kromě toho k dysfunkci endoteliálních buněk přispívají zánětlivé spouštěče, jako jsou prozánětlivé cytokiny, oxLDL (oxidovaný protein s nízkou hustotou), stejně jako různé kardiovaskulární rizikové faktory, jako jsou metabolické poruchy a kouření. Nadměrné napínání krevních cév může také vyvolat propustnost endotelu, zánětlivé reakce a oxidační stres.18 Společně to spouští prozánětlivou signalizaci v endoteliálních buňkách s upregulací prozánětlivých cytokinů (např. IL [interleukin]-1, IL{ {8}}), chemokiny (např. chemokinový ligand 2 s motivem CC) a endoteliálně-leukocytární adhezní molekuly (VCAM-1 [vaskulární buněčná adhezní molekula 1], ICAM-1 [intercelulární adhezní molekula 1] , P-selektin), snižuje endoteliální produkci ateroprotektivního oxidu dusnatého a zvyšuje endoteliální permeabilitu. Následkem toho se rekrutují zánětlivé leukocyty, adherují k zanícenému endotelu a infiltrují se do cévní stěny, kde spolu s nahromaděnými lipidy přispívají k rozvoji a progresi aterosklerotických lézí.7 Ateroprotektivní fenotyp endotelu je regulován hlavními transkripčními faktory jako KLF (Kruppel-like factor)-2, KLF-4 a NRF (nukleární faktor erytroidního 2-faktoru souvisejícího s erytroidem)-2, zatímco NF-κB (nukleární faktor-κB ) je klíčovým transkripčním faktorem, který řídí endoteliální zánět.17 Kromě toho endoteliální buňky vykazují dediferenciaci a zvýšenou heterogenitu během progrese aterosklerózy, se známkami přechodu z endotelu na mezenchym. Endoteliální-mezenchymální přechod je charakterizován získáváním funkcí mezenchymálních buněk jako produkce ECM (extracelulární matrix) a je řízen především transkripčními faktory Snail, Slug a Twist1. Jeho rozsah byl spojen se závažností aterosklerotických plátů v lidských tepnách19,20 a studie na zvířatech zkoumající klíčové regulátory endoteliálního přechodu na mezenchymální naznačovaly důležitou roli v progresi plátů20 a kalcifikaci,21 jak je podrobně diskutováno ve vynikajícím přehledu od Souilhol a kol.22

Je třeba poznamenat, že dysfunkce endoteliálních buněk nepřispívá pouze k iniciaci, progresi a destabilizaci plátu s následnou rupturou plátu, ale také k erozi aterosklerotického plátu, u níž se očekává, že je zodpovědná za jednu třetinu akutních koronárních syndromů. Zde může chronická aktivace endotelu nízkého stupně například ligandy TLR (toll-like receptor)-2 v kombinaci s apoptózou endoteliálních buněk a katabolismem komponent bazální membrány vyvolat oddělení endoteliálních buněk s následnou tvorbou trombu na obnažené oblasti.8
2. Dysfunkce endoteliálních buněk a trombotické riziko
Zdravá funkční endoteliální vrstva na makro- a mikrovaskulární úrovni je klíčová v regulaci hemostázy a zasahuje jak na úrovni primární, tak i sekundární hemostázy, aby se zabránilo nežádoucí aktivaci a koagulaci krevních destiček (obrázek 2). Na úrovni primární hemostázy endotel vyvolává silnou inhibici krevních destiček kontinuální sekrecí oxidu dusnatého (NO) a prostacyklinu, což způsobuje zvýšení intraagregačních hladin cGMP (cyklický guanosinmonofosfát) a cAMP (cyklický adenosinmonofosfát). aktivace krevních destiček extracelulárním ATP a ADP, endoteliální vrstva exprimuje CD39 a CD73, exonukleázy, které přeměňují ATP a ADP na adenosin, inhibitor krevních destiček, který zvýšením hladin cAMP krevních destiček zvyšuje práh aktivace krevních destiček.24 Kromě toho endoteliální glykokalyx odpuzuje krevní destičky jeho negativní náboj a jako takový napomáhá k prevenci adheze krevních destiček.25,26 Na úrovni sekundární hemostázy, v rámci glykokalyx, se heparansulfátové proteoglykany vážou a podporují aktivitu ATIII (antitrombin III), silného inhibitoru mnoha koagulačních faktorů včetně trombinu, FIXa, FXa, FXIa a FXIIa.26,27 Kromě toho endoteliální buňky exprimují TFPI (tkáňový faktor pathway inhibitor), serinovou proteázu, která – jak název napovídá – interferuje s koagulací indukovanou TF (tkáňový faktor), a tím omezuje aktivitu vnější dráhy.27 Vedle TFPI endotelové buňky konstitutivně exprimují trombomodulin, membránově vázaný protein, který zachycuje trombin z oběhu a po navázání zvyšuje afinitu trombinu k antikoagulačnímu proteinu C. Spolu s proteinem S se aktivuje protein C deaktivuje FVa a FVIIIa.27

Při poruchách metabolismu lipidů, zánětu, oxidativním stresu a patofyziologickém smykovém stresu se rozvíjí dysfunkce endoteliálních buněk, charakterizovaná snížením antitrombotických a protizánětlivých vlastností a degradací glykokalyx. Současně dysfunkční endotel nabývá prozánětlivých a protrombotických charakteristik (obrázky 3 a 4).27 V důsledku toho klesá produkce NO a prostacyklinu, zatímco sekrece protrombotických a prozánětlivých molekul, jako je vWF (von Willebrandův faktor) a chemokin s motivem CC ligand 2 se zvyšuje.27 Kromě toho je exprese trombomodulinu silně downregulována při dysfunkci endoteliálních buněk, což má za následek downregulaci aktivace proteinu C, zatímco exprese TF je upregulována ve prospěch aktivace koagulace.27 Již během raných fází aterogeneze se neutrofily extracelulární pasti se podílejí na dysfunkci endoteliálních buněk a podporují trombozánětlivou odpověď.28

Celkově vzato se tyto protrombotické a prozánětlivé reakce dysfunkčního endotelu vymknou kontrole, čímž se vytvoří začarovaný kruh, ve kterém dysfunkce endoteliálních buněk postupuje a vaskulární integrita se ztrácí, což má za následek silně zvýšené riziko trombózy.
3. Endoteliální dysfunkce, snížená vazorelaxace, zvýšená vaskulární tuhost a kardiovaskulární riziko
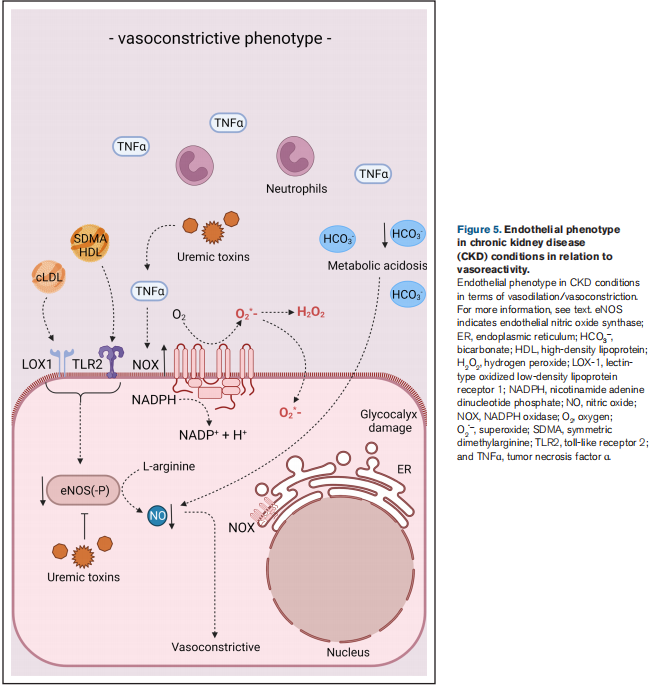
Stárnutí stejně jako patofyziologická remodelace cévní stěny kardiovaskulárními rizikovými faktory (např. hypertenze, diabetes, onemocnění ledvin) indukuje ztuhnutí tepen, což snižuje poddajnost tepen a zvyšuje pulzativní střih a tlak na vaskulaturu. Na strukturální úrovni je arteriální ztuhlost charakterizována ukládáním kolagenu a degradací elastinu v ECM.29 Kromě toho tonus buněk hladkého svalstva cév (VSMC) a endoteliální dysfunkce ovlivňují vaskulární reaktivitu se zhoršenou relaxační kapacitou VSMC a také sníženým endotelem -závislá vazorelaxace přispívající k arteriální tuhosti. Endoteliální buňky hrají důležitou roli ve vazorelaxaci prostřednictvím produkce NO pomocí eNOS (endoteliální NO syntáza; obrázek 2), přičemž snížená produkce a/nebo biologická dostupnost NO nebo jiných vazodilatačních látek snižuje vaskulární relaxační kapacitu (obrázek 5).
Zlatým standardem pro kvantifikaci arteriální tuhosti je analýza rychlosti průtoku krve, měřená jako rychlost pulzní vlny (PWV, analyzovaná jako karotická-femorální PWV nebo pažní-kotníková PWV). Alternativně tvar křivky arteriálního tlaku (analýza pulzní vlny) poskytuje náhled na tuhost arterií prostřednictvím kvantifikace indexu augmentace. Endoteliální funkce z hlediska vazodilatačních odpovědí může být měřena buď invazivně nebo neinvazivně v epikardiálních koronárních arteriích, periferních konduitních arteriích (analýza průtokem zprostředkované dilatace [FMD] brachiální arterie jako zlatý standard) nebo v koronární či periferní mikrovaskulatuře ( Obrázek 6). Bylo hlášeno, že periferní a koronární endoteliální dysfunkce spolu korelují,30,32 ačkoli jiní uvádějí spíše mírné korelace mezi periferní a koronární endoteliální dysfunkcí a naznačují potenciální odraz různých patologií nebo cévních řečišť.33 Navíc, zatímco PWV a augmentace Ukázalo se, že index dobře koreluje, ne vždy tomu tak bylo u indexu augmentace a „indexu reaktivní hyperémie“ jako neinvazivního endoteliálního funkčního zobrazení na periferii, potenciálně kvůli dopadu jiných faktorů než endoteliální funkce na tuhost cév.34

Cévní ztuhlost je časným prognostickým markerem ischemické choroby srdeční.35 Cévní ztuhlost zvyšuje zátěž srdce; vybízí k větší energetické potřebě pro srdeční ejekci a spouští srdeční hypertrofii.29 Se zvýšenou arteriální tuhostí, která je spojena se sníženou Windkesselovou funkcí (tj. snížením elastické tlumicí kapacity potřebné k tlumení kolísání krevního tlaku), arteriální tuhost také vyvolává zvýšenou pulsatilita na mikrocirkulaci a zesílené cyklické roztažení na endoteliálních buňkách. Nedávno se ukázalo, že posledně jmenovaný spouští sekreci proteinu GAS6 (specifická pro zástavu růstu 6) endoteliálními buňkami s následnou prozánětlivou signalizací GAS6/Axl v monocytech a jejich transformací na makrofágy a dendritické buňky. Jak je ukázáno na myším modelu chronické remodelace aorty indukované angiotensinem II, toto pak přispělo k zánětu cév a ledvin,36,37 spojujícím arteriální ztuhlost s dalším poškozením koncových orgánů.
Vzhledem k tomu, že endoteliální dysfunkce je časnou událostí u KVO, která předchází makrovaskulárním komplikacím, byly také intenzivně studovány endoteliální funkční analýzy z hlediska regulace vaskulárního tonu z hlediska prediktivní schopnosti kardiovaskulárního rizika nad rámec tradičních kardiovaskulárních rizikových faktorů. V mnoha studiích mohla makro a mikrovaskulární endoteliální dysfunkce nezávisle predikovat kardiovaskulární příhody u pacientů s rizikem onemocnění koronárních artérií.31 Například ve vztahu k endoteliální reaktivitě konduitových arterií (mikrovaskulatuře) střední až nízké endoteliální funkci zaznamenané FMD brachiální arterie byla spojena se zvýšeným rizikem srdečních příhod u pacientů s onemocněním periferních tepen podstupujících cévní operaci.38 Také u pacientů s chronickým srdečním selháním byla endoteliální dysfunkce analyzovaná pomocí brachiální a radiální FMD spojena s budoucími srdečními příhodami nebo mortalitou.39–41 zdravá endoteliální funkce zaznamenaná pažní FMD u zdánlivě zdravých jedinců vede k významně vyššímu přežití během 5-ročního sledování, a to i po úpravě na tradiční rizikové faktory.42,43 Dysfunkce endoteliálních buněk tedy může přidat důležité informace na kardiovaskulární riziko nad rámec tradičních rizikových faktorů.30 Je třeba poznamenat, že tato hodnota analýzy endoteliální dysfunkce pro predikci kardiovaskulárního rizika se zdá být ovlivněna analyzovanou kohortou pacientů, protože jiní nemohli potvrdit hodnotu předpovědi kardiovaskulárního rizika pro analýzu endoteliální dysfunkce založenou na FMD ve starší kohortě, potenciálně v důsledku snížené arteriální poddajnosti (tj. vaskulární schopnosti expandovat při zvýšení tlaku) u starších subjektů.44 Nicméně tato studie zaznamenala souvislost periferní mikrovaskulární endoteliální dysfunkce se zvýšeným kardiovaskulárním rizikem, jak je uvedeno v následující odstavec podrobněji.

Cistanche prášek
4. Mikrovaskulární dysfunkce a kardiovaskulární riziko
Zatímco aterosklerotickými změnami jsou postiženy převážně větší tepny, dysfunkce mikrovaskulatury – sítě arteriol, kapilár a venul umožňujících tkáňovou perfuzi – je jiná. Mikrovaskulární dysfunkce (MVD) se může vyvinout na úrovni koronární mikrocirkulace i na periferii při absenci nebo přítomnosti obstrukční arteriální choroby větších cév. Rozvoj MVD je multifaktoriální a může být výsledkem funkčních nebo strukturálních změn nebo jejich kombinací v závislosti na základním onemocnění. Z hlediska funkčních změn stojí za MVD zhoršené vazodilatační odpovědi – alespoň částečně závislé na endotelu. Kromě toho zvýšení hladin vazokonstrikčních látek v kombinaci se zvýšenou citlivostí na tyto stimuly se podílí na MVD, což přispívá k výskytu vaskulárních spazmů. Strukturální změny spojené s MVD zahrnují luminální zúžení mikrovaskulatury v důsledku nepříznivé vaskulární remodelace a perivaskulární fibrózy; mikrovaskulární komprese; mikrovaskulární redukce vedoucí ke ztrátě koherentních mikrovaskulárních stromů (kapilár, malých arteriol a venul); a mikroembolizace aterosklerotického a trombotického materiálu.45–48
Pokud jde o makrovaskulární endoteliální dysfunkci, také mikrovaskulární endoteliální dysfunkce byla spojena s kardiovaskulárním rizikem.49 Tak tomu bylo například v populační prospektivní studii, ve které byla periferní mikrovaskulární endoteliální dysfunkce – ale ne FMD zprostředkovaná endoteliální funkce arterií konduitů — koreluje s kardiovaskulárními příhodami (infarkt myokardu, cévní mozková příhoda nebo smrt) u starších pacientů během 5 let sledování, a to i mimo hlavní kardiovaskulární rizikové faktory z Framinghamského rizikového skóre.44 Ve stejné linii periferní mikrovaskulární endoteliální dysfunkce predikovala ischemické srdce onemocnění a dokonce si vedl lépe v predikci budoucího kardiovaskulárního rizika u neobstrukčního onemocnění koronárních tepen ve srovnání s jinými rizikovými skóre.50 Také retinální arteriolární endoteliální dysfunkce nezávisle predikovala MACE u pacientů s nebo s vysokým rizikem onemocnění koronárních tepen.51
Také o srdečním selhání, a to jak pacientů se srdečním selháním se sníženou ejekční frakcí levé komory, tak pacientů se srdečním selháním se zachovanou ejekční frakcí s mikrovaskulární dysfunkcí. Při selhání se sníženou ejekční frakcí levé komory byla analýza periferní mikrovaskulární endoteliální funkce spojena se zvýšeným výskytem příhod souvisejících se srdečním selháním. vykazují snížení srdeční mikrovaskulární hustoty54 a také zvýšení markerů dysfunkce endoteliálních buněk v biopsiích myokardu, včetně upregulace endoteliálních adhezních molekul (E-selektin, ICAM-1), prooxidačních regulátorů (NOX{{ 7}}) a eNOS uncoupling.55 Bylo navrženo, že koronární mikrovaskulární dysfunkce přispívá ke ztuhnutí srdeční stěny a diastolické dysfunkci u pacientů se srdečním selháním se zachovanou ejekční frakcí. Nicméně, zda se jedná o skutečný kauzální vztah nebo spíše nekauzální souvislost mezi koronární mikrovaskulární dysfunkcí a srdečním selháním se zachovanou ejekční frakcí, zůstává diskutováno.56,57 Je třeba poznamenat, že koronární mikrovaskulární dysfunkce může mít patofyziologickou a prognostickou roli i u jiných typů CVD, pro který odkazujeme na vynikající nedávný přehled od Del Buona et al.46

Herba Cistanche a extrakt z Cistanche
5. Dysfunkce endoteliálních buněk a vaskulární stárnutí
Dysfunkce endoteliálních buněk se sníženou endoteliální vazodilatační kapacitou zvýšená zánětlivost a permeabilita a zlepšené protrombotické vlastnosti, vše popsané výše, je důležitým znakem vaskulárního stárnutí. Dysfunkce endoteliálních buněk není pozorována pouze v makrocirkulaci, ale také přispívá k mikrovaskulární dysfunkci při stárnutí. Cévní stárnutí je dále charakterizováno funkčními a strukturálními změnami cévní stěny a adventicie procesy např. zánětu, cévní kalcifikace a remodelace ECM, které dále přispívají ke zvýšené vaskulární tuhosti a kardiovaskulárnímu riziku.58
REFERENCE
1. Inker LA, Astor BC, Fox CH, Isakova T, Lash JP, Peralta CA, Kurella Tamura M, Feldman HI. Komentář KDOQI US ke směrnici klinické praxe KDIGO z roku 2012 pro hodnocení a léčbu CKD. Am J Kidney Dis. 2014;63:713–735. doi: 10.1053/j.ajkd.2014.01.416
2. Hill NR, Fatoba ST, Oke JL, Hirst JA, O-Callaghan CA, Lasserson DS, Hobbs FDR. Globální prevalence chronického onemocnění ledvin – systematický přehled a metaanalýza. PLoS One. 2016;11:e0158765. doi: 10.1371/journal.pone.0158765
3. Thompson S, James M, Wiebe N, Hemmelgarn B, Manns B, Klarenbach S, Tonelli M; Alberta Kidney Disease Network. Příčina smrti u pacientů se sníženou funkcí ledvin. J Am Soc Nephrol. 2015;26:2504–2511. doi: 10.1681/ASN.2014070714
4. Roberts MA, Polkinghorne KR, McDonald SP, Ierino FL. Sekulární trendy kardiovaskulární úmrtnosti pacientů na dialýze ve srovnání s běžnou populací. Am J Kidney Dis. 2011;58:64–72. doi: 10.1053/j.ajkd.2011.01.024
5. van der Velde M, Matsushita K, Coresh J, Astor BC, Woodward M, Levey A, de Jong P, Gansevoort RT, Matsushita K, Coresh J a kol; Konsorcium pro prognózu chronického onemocnění ledvin. Nižší odhadovaná rychlost glomerulární filtrace a vyšší albuminurie jsou spojeny se všemi příčinami a kardiovaskulární mortalitou. Kolaborativní metaanalýza vysoce rizikových populačních kohort. Kidney Int. 2011;79:1341–1352. doi 10.1038/ki.2010.536
6. Jankowski J, Floege J, Fliser D, Bohm M, Marx N. Kardiovaskulární onemocnění u chronického onemocnění ledvin: patofyziologické poznatky a terapeutické možnosti. Oběh. 2021;143:1157–1172. doi: 10.1161/CIRCULATIONAHA.120.050686
7. Weber C, Noels H. Ateroskleróza: současná patogeneze a terapeutické možnosti. Nat Med. 2011;17:1410–1422. doi: 10,1038/nm,2538
8. Quillard T, Franck G, Mawson T, Folco E, Libby P. Mechanismy eroze aterosklerotických plátů. Curr Opin Lipidol. 2017;28:434–441. doi: 10.1097/MOL.0000000000000440
9. Betrui A, Martinez-Alonso M, Arcidiacono MV, Cannata-Andia J, Pascual J, Valdivielso JM, Fernández E; Vyšetřovatelé ze studie NEFRONA. Prevalence subklinické ateromatózy a souvisejících rizikových faktorů u chronického onemocnění ledvin: studie NEFRONA. Transplantace nefrolových čísel. 2014;29:1415–1422. doi 10.1093/ndt/gfu038
10. Valdivielso JM, Rodríguez-Puyol D, Pascual J, Barrios C, BermúdezLópez M, Sánchez-Niño MD, Pérez-Fernández M, Ortiz A. Ateroskleróza u chronického onemocnění ledvin: více, méně nebo jen jinak?. Arterioscler Thromb Vasc Biol. 2019;39:1938–1966. doi: 10.1161/ATVBAHA.119.312705
11. Gracia M, Betrui A, Martinez-Alonso M, Arroyo D, Abajo M, Fernández E, Valdivielso JM; Vyšetřovatelé NEFRONA. Prediktory progrese subklinické ateromatózy během 2 let u pacientů s různými stádii CKD. Clin J Am Soc Nephrol. 2016;11:287–296. doi: 10.2215/CJN.01240215
12. Anavekar NS, McMurray JJV, Velazquez EJ, Solomon SD, Kober L, Rouleau JL, White HD, Nordlander R, Maggioni A, Dickstein K, et al. Vztah mezi renální dysfunkcí a kardiovaskulárními výsledky po infarktu myokardu. N Engl J Med. 2004;351:1285–1295. doi: 10.1056/NEJMoa041365
13. Myerburg RJ, Junttila MJ. Náhlá srdeční smrt způsobená ischemickou chorobou srdeční. Oběh. 2012;125:1043–1052. doi: 10.1161/CIRCULATIONAHA.111.023846
14. Haider AW, Larson MG, Benjamin EJ, Levy D. Zvýšená hmota levé komory a hypertrofie jsou spojeny se zvýšeným rizikem náhlé smrti. J Am Coll Cardiol. 1998;32:1454–1459. doi: 10.1016/s0735-1097(98)00407-0
15. Glassock RJ, Pecoits-Filho R, Barberato SH. Hmota levé komory u chronického onemocnění ledvin a ESRD. Clin J Am Soc Nephrol. 2009;4:S79–S91. doi: 10.2215/CJN.04860709
16. Middleton R, Parfrey PS, Foley RN. Hypertrofie levé komory u renálního pacienta. J Am Soc Nephrol. 2001;12:1079–1084. doi 10.1681/ASN.V1251079
17. Gimbrone MA Jr, Garcia-Cardena G. Dysfunkce endoteliálních buněk a patobiologie aterosklerózy. Circ Res. 2016;118:620–636. doi: 10.1161/CIRCRESAHA.115.306301
18. Meza D, Musmacker B, Steadman E, Stransky T, Rubenstein DA, Yin W. Biomechanické odezvy endoteliálních buněk jsou závislé jak na napětí ve smyku tekutiny, tak na napětí v tahu. Cell Mol Bioeng. 2019;12:311–325. doi 10.1007/s12195-019-00585-0
19. Evrard SM, Lecce L, Michelis KC, Nomura-Kitabayashi A, Pandey G, Purushothaman KR, d'Escamard V, Li JR, Hadri L, Fujitani K a kol. Endoteliální přechod na mezenchymální je běžný u aterosklerotických lézí a je spojen s nestabilitou plaku. Nat Commun. 2016;7:11853. doi: 10.1038/ncomms11853
20. Chen PY, Qin L, Baeyens N, Li G, Afolabi T, Budatha M, Tellides G, Schwartz MA, Simons M. Endoteliální-mezenchymální přechod řídí progresi aterosklerózy. J Clin Invest. 2015;125:4514–4528. doi: 10.1172/JCI82719
21. Bostrom KI, Yao J, Guihard PJ, Blazquez-Medela AM, Yao Y. Endoteliální mezenchymální přechod v kalcifikaci aterosklerotických lézí. Ateroskleróza. 2016;253:124–127. doi 10.1016/j.aterosclerosis.2016.08.046
22. Souilhol C, Harmsen MC, Evans PC, Krenning G. Endoteliálně-mezenchymální přechod u aterosklerózy. Cardiovasc Res. 2018;114:565–577. doi: 10.1093/cvr/cvx253
23. Mitchell JA, Ali F, Bailey L, Moreno L, Harrington LS. Úloha oxidu dusnatého a prostacyklinu jako vazoaktivních hormonů uvolňovaných endotelem. Exp Physiol. 2008;93:141–147. doi: 10.1113/expphysiol.2007.038588
24. Johnston-Cox HA, Ravid K. Adenosin a krevní destičky. Purinergní signál. 2011;7:357–365. doi: 10.1007/s11302-011-9220-4
25. Born GV, Palinski W. Neobvykle vysoké koncentrace kyselin sialových na povrchu cévního endotelu. Br J Exp Pathol. 1985;66:543–549.
26. Reitsma S, Slaaf DW, Vink H, van Zandvoort MAMJ, oude Egbrink MGA. Endoteliální glykokalyx: složení, funkce a vizualizace. Pfugers Arch. 2007;454:345–359. doi 10.1007/s00424-007-0212-8
27. Yau JW, Teoh H, Verma S. Endoteliální buněčná kontrola trombózy. BMC Cardiovasc Disord. 2015;15:130. doi: 10,1186/s12872-015-0124-z
28. Döring Y, Soehnlein O, Weber C. Neutrofilní extracelulární pasti u aterosklerózy a aterotrombózy. Circ Res. 2017;120:736–743. doi: 10.1161/CIRCRESAHA.116.309692
29. Zieman SJ, Melenovský V, Kass DA. Mechanismy, patofyziologie a terapie arteriální tuhosti. Arterioscler Thromb Vasc Biol. 2005;25:932– 943. doi 10.1161/01.ATV.0000160548.78317.29
30. Flammer AJ, Anderson T, Celermajer DS, Creager MA, Deanfield J, Ganz P, Hamburg NM, Lüscher TF, Shechter M, Taddei S, et al. Hodnocení endoteliální funkce: od výzkumu do klinické praxe. Oběh. 2012;126:753–767. doi: 10.1161/CIRCULATIONAHA.112.093245
31. Alexander Y, Osto E, Schmidt-Trucksass A, Shechter M, Trifunovic D, Duncker DJ, Aboyans V, Back M, Badimon L, Cosentino F a kol. Endoteliální funkce v kardiovaskulární medicíně: konsensus pracovní skupiny Evropské kardiologické společnosti pro aterosklerózu a vaskulární biologii, aortu a periferní vaskulární onemocnění, koronární patofyziologii a mikrocirkulaci a trombózu. Cardiovasc Res. 2021;117:29–42. doi: 10.1093/cvr/cvaa085
32. Lerman A, Zeiher AM. Endoteliální funkce: srdeční příhody. Oběh. 2005;111:363–368. doi 10.1161/01.CIR.0000153339.27064.14
33. Schnabel RB, Schulz A, Wild PS, Sinning ČR, Wilde S, Eleftheriadis M, Herkenhoff S, Zeller T, Lubos E, Lackner KJ, et al. Neinvazivní měření cévních funkcí v komunitě: průřezové vztahy a srovnání metod. Circ Cardiovasc Imaging. 2011;4:371–380. doi: 10.1161/CIRCIMAGING.110.961557
34. Perrault R, Omelchenko A, Taylor CG, Zahrádka P. Stanovení zaměnitelnosti parametrů arteriální tuhosti, ale nikoli parametrů endoteliální funkce u zdravých jedinců. BMC Cardiovasc Disord. 2019;19:190. doi: 10,1186/s12872-019-1167-3
35. Bonarjee VVS. Arteriální tuhost: prognostický marker u ischemické choroby srdeční. Dostupné metody a klinická aplikace. Přední Cardiovasc Med. 2018;5:64. doi: 10.3389/fcvm.2018.00064
36. Van Beusecum JP, Barbaro NR, Smart CD, Patrick DM, Loperena R, Zhao S, de la Visitacion N, Ao M, Xiao L, Shibao CA a kol. Zánět a hypertenzi specifická pro zastavení růstu-6 a Axl koordinují. Circ Res. 2021;129:975–991. doi: 10.1161/CIRCRESAHA.121.319643
37. Chen W, Van Beusecum JP, Xiao L, Patrick DM, Ao M, Zhao S, Lopez MG, Billings FT, Cavinato C, Caulk AW a kol. Role Axl při zánětu a poškození cílových orgánů v důsledku hypertenzní remodelace aorty. Am J Physiol Heart Circ Physiol. 2022;323:H917–H933. doi: 10.1152/ajpheart.00253.2022
38. Huang AL, Silver AE, Shvenke E, Schopfer DW, Jahangir E, Titas MA, Shpilman A, Menzoian JO, Watkins MT, Raffetto JD a kol. Prediktivní hodnota reaktivní hyperémie pro kardiovaskulární příhody u pacientů s onemocněním periferních tepen podstupujících cévní operaci. Arterioscler Thromb Vasc Biol. 2007;27:2113–2119. doi: 10.1161/ATVBAHA.107.147322
39. Fischer D, Rossa S, Landmesser U, Spiekermann S, Engberding N, Hornig B, Drexler H. Endoteliální dysfunkce u pacientů s chronickým srdečním selháním je nezávisle spojena se zvýšeným výskytem hospitalizací, transplantací srdce nebo úmrtí. Eur Heart J. 2005;26:65–69. doi: 10.1093/eurheartj/ehi001
40. Meyer B, Mörtl D, Strecker K, Hülsmann M, Kulemann V, Neunteufl T, Pacher R, Berger R. Vasodilatace zprostředkovaná průtokem předpovídá výsledek u pacientů s chronickým srdečním selháním: srovnání s natriuretickým peptidem typu B. J Am Coll Cardiol. 2005;46:1011–1018. doi 10.1016/j.jacc.2005.04.060
41. Katz SD, Hryniewicz K, Hriljac I, Balidemaj K, Dimayuga C, Hudaihed A, Yasskiy A. Vaskulární endoteliální dysfunkce a riziko mortality u pacienta s chronickým srdečním selháním. Oběh. 2005;111:310–314. doi 10.1161/01.CIR.0000153349.77489.CF
42. Yeboah J, Crouse JR, Hsu FC, Burke GL, Herrington DM. Dilatace zprostředkovaná brachiálním průtokem předpovídá incidentní kardiovaskulární příhody u starších dospělých: Cardiovascular Health Study. Oběh. 2007;115:2390–2397. doi: 10.1161/CIRCULATIONAHA.106.678276
43. Yeboah J, Folsom AR, Burke GL, Johnson C, Polak JF, Post W, Lima JA, Crouse JR, Herrington DM. Prediktivní hodnota dilatace zprostředkované brachiálním průtokem pro incidentní kardiovaskulární příhody v populační studii: multietnická studie aterosklerózy. Oběh. 2009;120:502–509. doi: 10.1161/CIRCULATIONAHA.109.864801
44. Lind L, Berglund L, Larsson A, Sundström J. Endoteliální funkce v odporových a konduitních tepnách a 5-roční riziko kardiovaskulárního onemocnění. Oběh. 2011;123:1545–1551. doi: 10.1161/CIRCULATIONAHA.110.984047
45. Vancheri F, Longo G, Vancheri S, Henein M. Koronární mikrovaskulární dysfunkce. J Clin Med. 2020; 9:2880. doi: 10,3390/jcm9092880
46. Del Buono MG, Montone RA, Camili M, Carbone S, Narula J, Lavie CJ, Niccoli G, Crea F. Koronární mikrovaskulární dysfunkce napříč spektrem kardiovaskulárních onemocnění: JACC State-of-the-Art review. J Am Coll Cardiol. 2021;78:1352–1371. doi 10.1016/j.jacc.2021.07.042
47. Ehling J, Babickova J, Gremse F, Klinkhammer BM, Baetke S, Knuechel R, Kiessling F, Floege J, Lammers T, Boor P. Kvantitativní mikropočítačové tomografické zobrazování vaskulární dysfunkce u progresivních onemocnění ledvin. J Am Soc Nephrol. 2016;27:520–532. doi 10.1681/ASN.2015020204
48. Prommer HU, Maurer J, von Websky K, Freise C, Sommer K, Nasser H, Samapati R, Reglin B, Guimaraes P, Pries AR a kol. Chronické onemocnění ledvin vyvolává systémovou mikroangiopatii, tkáňovou hypoxii a dysfunkční angiogenezi. Sci Rep. 2018;8:5317. doi: 10,1038/s41598-018-23663-1
49. Querfeld U, Mak RH, Pries AR. Mikrovaskulární onemocnění u chronického onemocnění ledvin: základ ledovce v kardiovaskulární komorbiditě. Clin Sci (Londýn). 2020;134:1333–1356. doi 10.1042/CS20200279
50. Matsuzawa Y, Sugiyama S, Sugamura K, Nozaki T, Ohba K, Konishi M, Matsubara J, Sumida H, Kaikita K, Kojima S, et al. Digitální hodnocení funkce endotelu a ischemické choroby srdeční u žen. J Am Coll Cardiol. 2010;55:1688–1696. doi 10.1016/j.jacc.2009.10.073
51. Tam JD, Al-Fiadh AH, Amirul Islam FM, Patel SK, Burrell LM, Wong TY, Farouque O. Porucha mikrovaskulární funkce sítnice předpovídá dlouhodobé nežádoucí příhody u pacientů s kardiovaskulárním onemocněním. Cardiovasc Res. 2021;117:1949–1957. doi: 10.1093/cvr/cvaa245
52. Fujisue K, Sugiyama S, Matsuzawa Y, Akiyama E, Sugamura K, Matsubara J, Kurokawa H, Maeda H, Hirata Y, Kusaka H, et al. Prognostický význam periferní mikrovaskulární endoteliální dysfunkce u srdečního selhání se sníženou ejekční frakcí levé komory. Circ J. 2015;79:2623–2631. doi: 10.1253/circa.CJ-15-0671
53. Maréchaux S, Samson R, van Belle E, Breyne J, de Monte J, Dédrie C, Chebai N, Menet A, Banfi C, Bouabdallaoui N, et al. Cévní a mikrovaskulární endoteliální funkce u srdečního selhání se zachovanou ejekční frakcí. Selhání karty J. 2016;22:3–11. doi: 10.1016/j.cardfail.2015.09.003
54. Mohammed SF, Hussain S, Mirzoyev SA, Edwards WD, Maleszewski JJ, Redfield MM. Koronární mikrovaskulární vzácnost a fibróza myokardu u srdečního selhání se zachovanou ejekční frakcí. Oběh. 2015;131:550– 559. doi: 10.1161/CIRCULATIONAHA.114.009625
55. Franssen C, Chen S, Unger A, Korkmaz HI, De Keulenaer GW, Tschöpe C, Leite-Moreira AF, Mussters R, Niessen HWM, Linke WA a kol. Mikrovaskulární aktivace zánětlivého endotelu myokardu při srdečním selhání se zachovanou ejekční frakcí. Selhání srdce JACC. 2016;4:312–324. doi: 10.1016/j.jchf.2015.10.007
56. D'Amario D, Migliaro S, Borovac JA, Restivo A, Vergallo R, Galli M, Leone AM, Montone RA, Niccoli G, Aspromonte N, et al. Mikrovaskulární dysfunkce u srdečního selhání se zachovanou ejekční frakcí. Přední Physiol. 2019;10:1347. doi: 10.3389/Phys.2019.01347
57. Cornuault L, Rouault P, Duplàa C, Couffinhal T, Renault MA. Endoteliální dysfunkce u srdečního selhání se zachovanou ejekční frakcí: jaké jsou experimentální důkazy? Přední Physiol. 2022;13:906272. doi: 10.3389/Phys.2022.906272
58. Harvey A, Montezano AC, Alves Lopes R, Rios F, Touyz RM. Cévní fibróza při stárnutí a hypertenzi: molekulární mechanismy a klinické implikace. Může J Cardiol. 2016;32:659–668. doi 10.1016/j.cjca.2016.02.070
Constance CFMJ Baaten, Sonja Vondenhoff, Heidi Noels






