Metabolismus a metabolický zánět jsou klíčové procesy, které ovlivňují i jsou ovlivňovány stárnutím
Sep 16, 2022
Další informace vám poskytne oscar.xiao@wecistanche.com
Souhra metabolismu a imunitní paměti
Metabolismus a metabolický zánět jsou klíčové procesy, které stárnutí ovlivňují a jsou ovlivňovány. Metabolická onemocnění, jako je diabetes mellitus 2. typu, kardiovaskulární onemocnění a obezita, jsou také považovány za onemocnění související s věkem. Tyto stavy jsou doprovázeny chronickým zánětem, nazývaným metaflammace, který je způsoben nadbytkem živin. Ačkoli se spouštěče mohou lišit, mechanismy metaflammace a zánětu jsou velmi podobné.

Mitochondriální dysfunkce, akumulace senescentních buněk a buněčného odpadu a hyperaktivace vrozených imunitních odpovědí, jako je inflammasom, přispívají k oběma procesům [120]. Proto je klíčové porozumět souhře mezi buněčným stárnutím, metabolismem a zánětem při chronologickém stárnutí a metabolickými chorobami souvisejícími s věkem, abychom je mohli vrátit.
Metabolismus T buněk
Tiché T buňky využívají hlavně katabolické procesy, zatímco aktivované buňky spoléhají na anabolické procesy, aby podpořily produkci a proliferaci proteinů. Buňky potřebují aktivovat kritickou serin/threonin kinázu, savčí cíl rapamycinu (mTOR), aby vyvolaly anabolické dráhy [121]. Zatímco řídí růst a proliferaci, mTOR také upreguluje transport glukózy a glykolýzu.cistanche tubulosa dávkování redditGlykolýza je jednou z hlavních cest k výrobě energie. Ačkoli není energeticky účinný — — z jedné molekuly glukózy lze generovat pouze 2 molekuly adenosintrifosfátu (ATP), generuje energii velmi rychle, což je užitečné pro aktivní a proliferující T buňky[122]. Zpracování glukózy poskytuje ATP, NADH a pyruvát. Pyruvát je poté přeměněn na laktát a exportován jako kyselina mléčná v případě glykolýzy nebo jinak transportován do mitochondrií pro oxidativní fosforylaci (OXPHOS).

OXPHOS je mnohem účinnější bioenergetická cesta, která produkuje 36 molekul ATP z každé molekuly glukózy [123]. V tomto případě je pyruvát přeměněn na acetyl-CoA a vstupuje do cyklu trikarboxylové kyseliny (cyklus TCA), který je spojen s elektronovým transportním řetězcem (TCA) prostřednictvím donorů elektronů NADH a FADH2. Cyklus TCA lze doplnit aminokyselinami a oxidací mastných kyselin. Oxidaci mastných kyselin (FAO) využívají hlavně buňky s nízkou energetickou náročností a hraje klíčovou roli v paměti CD8 a vývoji CD4 plus Treg [124]. Aktivované T buňky upregulují svůj příjem glutaminu a provádějí glutaminolýzu za vzniku -ketoglutarátu, který vstupuje do cyklu TCA.
Metabolity cyklu TCA navíc mohou regulovat imunitní funkce jinými způsoby, než je produkce energie. Například acetyl-CoA působí jako klíčový kofaktor pro acetylaci histonů [125]. V aktivovaných T buňkách je acetyl-CoA vyžadován pro produkci IFNy prostřednictvím acetylace histonů [126]. Acetyl-CoA také přispívá k acetylaci mitochondriálních proteinů[127], což má rozsáhlé funkční důsledky pro vrozené i adaptivní imunitní buňky [128].
Tiché naivní T buňky uspokojují své energetické potřeby pomocí OXPHOS [129].cistanche แอ ม เว ย์Signalizace IL-7 a TCR jsou zásadní pro jejich metabolickou regulaci a přežití [130, 131]. Když jsou T buňky aktivovány, nastává okamžitá potřeba energie pro efektorové funkce a tvorbu biomasy. Buňky upregulují transportéry, jako je glukózový transportér 1 (GLUT1) a zapojují se do aerobní glykolýzy, čímž podporují produkci cytokinů prostřednictvím drah, jako je fosfoinositid 3-kináza (PI3K)-AKT-mTOR osa a mitogenem aktivovaná proteinkináza (MAPK) signalizace[132]. Glylytický přepínač je vyžadován pro efektorové funkce, např. produkci IFNy, ale není nezbytný pro proliferaci [133]. OXPHOS lze také využít pro účely proliferace a přežití. Ačkoli aktivované T buňky funkčně spoléhají na glykolýzu, OXPHOS rozhodně není postradatelný: když je OXPHOS inhibován oligomycinem, aktivace a proliferace T buněk jsou blokovány [133].
Ačkoli se v klidovém stavu spoléhají na OXPHOS a FAO, paměťové T buňky potřebují reagovat rychle a efektivně na setkání s antigenem. Proto mohou přejít na glykolýzu rychleji než naivní T buňky [134]. S touto bioenergetickou výhodou byla spojena větší mitochondriální hmota a silná mitochondriální rezervní respirační kapacita [135, 136]. Kromě toho je mitochondriální fúze nezbytná pro vývoj a funkci paměťových T buněk [137].
Vliv stárnutí na metabolismus T buněk
Zvýšená aktivita p38 MAPK je jednou z charakteristik senescentních T buněk. Inhibice p38 zlepšuje telomerasovou aktivitu, proliferaci, autofagii a mitochondriální fitness způsobem nezávislým na mTOR[17]. Inhibice MAPK také zvyšuje odpovědi T buněk a protilátek u starých myší očkovaných proti chřipce[138].
Pacienti s mutacemi v PI3K mají depleci naivních T buněk, ale akumulaci senescentních efektorových buněk, stejně jako u starších pacientů [139]. Inhibice aktivity mTOR léčbou rapamycinem u těchto pacientů částečně obnovuje senescentní fenotyp. Nadměrně aktivní signalizace PI3K/AKT/mTOR je proto navržena jako jeden z hnacích motorů stárnutí T buněk.
Staré naivní T buňky mají vyšší mitochondriální hmotu, ale zajímavé je, že menší mitochondriální respirační kapacitu, pravděpodobně kvůli transkripční downregulaci genů respiračního řetězce [140]. Enzymy jednouhlíkového metabolismu jsou navíc ve stárnoucích naivních T buňkách deficitní a suplementace formiátem a glycinem, metabolity jednouhlíkového metabolismu, zlepšuje přežití a aktivaci buněk [14].
Autofagie je důležitá pro generování paměti T buněk a indukce autofagie spermidinem zlepšuje odpovědi CD8 plus T buněk proti očkování proti chřipce u starých myší [142]. CD4 plus paměťové T-buňky starších osob vykazují upregulovanou oxidativní fosforylaci, produkci reaktivních forem kyslíku (ROS) a oxidaci mastných kyselin [143].bioflavonoidyMají také vyšší expresi sirtuinu 1 (SIRT1), NAD-dependentní deacetylázy, ve srovnání s mladšími buňkami. SIRT1 a AMPK, dvě důležité molekuly pro snímání živin a negativní regulátory mTOR, se navzájem pozitivně ovlivňují [144]. vysoká glykolytická kapacita, která je spojena s jejich downregulovanou expresí SIRTI [145].
Buňky CD8 plus TEMRA mají vyšší expresi genů souvisejících s glykolýzou a glutaminolýzou a větší množství ATP ve srovnání s naivními a EM buňkami[146]. Navzdory upregulované glykolytické transkripci v buňkách TEMRA jsou hladiny bazální glykolýzy podobné jako u naivních a EM buněk. Stejně jako EM buňky mohou TEMRA buňky po aktivaci rychle zvýšit glykolýzu a OXPHOS [146]. Z hlediska funkce jsou TEMRA buňky schopné cytotoxicity a produkce cytokinů, a to i přes jejich senescentní stav a zhoršenou mitochondriální funkci [17, 36].
Dlouhodobá CMV infekce, o které je známo, že podporuje imunosenescenci, také mění buněčný metabolismus T buněk, zvyšuje vychytávání glukózy, podporuje glykolýzu, restrukturalizuje lipidové rafty a narušuje metabolismus cholesterolu [147, 148]. Kromě toho chronický zánět způsobený celoživotním CMV infekce narušuje pankreatické buňky a zvyšuje riziko diabetu 2. typu u starších osob [149].
Metabolismus B buněk
Metabolické dráhy, které regulují T buňky, jsou také nezbytné pro funkci B buněk, i když o metabolismu B buněk nebylo mnoho výzkumů. Když je B buňka aktivována po rozpoznání antigenu pomocí BCR a pomoci T buněk, aktivuje signalizaci PI3K/AKT/mTOR [150]. Stejně jako aktivované T buňky potřebují aktivované B buňky rychlou produkci energie ke zvýšení biomasy a proliferaci. V důsledku toho se zvyšuje vychytávání glukózy a glutaminu spolu se spotřebou kyslíku, OXPHOS a mitochondriální remodelací [151]. OXPHOS a glutamin-fueling cyklu TCA byly navrženy jako kritické bioenergetické dráhy pro růst a funkci B buněk, zatímco glukóza byla postradatelná [152].
Studie ukázala, že aktivované B buňky mají více mitochondrií, ale podobné množství mitochondriální DNA, což naznačuje, že po aktivaci dochází spíše ke štěpení naivních mitochondrií B buněk s více nukleoidy než k mitochondriální replikaci [152]. Další studie naznačila, že mitochondriální remodelace a hladiny ROS určují osud aktivovaných B buněk. Buňky se zvýšenou mitochondriální hmotou a vyššími hladinami ROS po aktivaci jsou předurčeny k rekombinaci se změnou třídy, zatímco buňky se sníženou mitochondriální hmotou podléhají diferenciaci plazmatických buněk[153].
Energetické potřeby aktivovaných B buněk v GC se často mění [154].kolik cistanche vzítV hypoxické světelné zóně buňky spotřebovávají méně kyslíku a jsou více glykolytické. mTORC1 zde není nezbytný pro regulaci glykolýzy, ale je spolu s c-Myc kritický pro pozitivní selekci buněk a migraci do tmavé zóny pro proliferaci a somatickou hypermutaci [155,156].

Cistanche může proti stárnutí
Po zrání GC, kdy se buňka diferencuje na paměťové B buňky, se metabolický stav stává klidnějším s dominantním OXPHOS. Rychlá reaktivace mTORC1 a glykolýza je však možná pro pozdější diferenciaci na plazmablasty produkující protilátky [157]. Paměťové B buňky mají navíc vysokou bazální autofagii, která je nezbytná pro jejich přežití, dokud nenarazí na antigen [158,159].
GC také produkují dlouhotrvající plazmatické buňky, které mohou produkovat tisíce protilátek za sekundu. To je přirozeně vysoce energeticky náročné. mTORC1 je nezbytný pro tvorbu plazmatických buněk a syntézu protilátek [160]. Plazmatické buňky mají vysoké hladiny absorpce glukózy, ale většina glukózy se používá pro glykosylaci proteinů [161]. Přežití a tvorba protilátek v plazmatických buňkách však byly narušeny, když byl odstraněn glukózový transportér Glute [162]. Také mitochondriální import pyruvátu, poskytovaný glykolýzou, je kritický pro dlouhodobé udržení plazmatických buněk [161].
Konečně B1 B buňky rezidentní v tkáni jsou aktivnější v glykolýze a OXPHOS než jiné B buňky, klasické B buňky produkující protilátky a paměťové B buňky. Kromě toho je autofagie kritická pro mitochondriální funkci a sebeobnovu B1 buněk [163].
Vliv stárnutí na metabolismus B buněk
Existuje méně literatury o tom, jak je metabolismus B buněk regulován a jak ovlivňuje funkci organismů stárnutím. Studie ukázala, že B lymfocyty vylučující protilátky u starších jedinců měly nižší expresi SIRTI a vyšší hladiny SIRT1 byly spojeny s lepší protilátkovou odpovědí na více kmenů chřipkového viru [164]. Také naivní a aktivované B buňky starších osob měly o něco menší glykolytickou kapacitu a výraznější snížení OXPHOS. U myší měly staré B buňky podobnou míru glykolýzy a OXPHOS jako jejich mladé protějšky, ale nemohly dále zvýšit OXPHOS po stimulaci[165] ]. Buňky však byly schopny upregulovat glykolýzu, aby uspokojily svou energetickou potřebu.
Leptin, prozánětlivý hormon vylučovaný adipocyty, je vyšší v oběhu u obézních jedinců [166]. Mezi neobézními lidmi jsou koncentrace leptinu nápadně vyšší u starších osob [167]. Hojnost leptinu v séru je také pozitivně spojena s křehkostí [168]. Po expozici leptinu vykazují B buňky od mladých štíhlých jedinců podobný profil jako B buňky starších štíhlých a mladých obézních jedinců, pokud jde o transkripční profil a sekreci protilátek [167]. Leptin také snižuje produkci protilátek specifických pro chřipku z B buněk in vitro. Je známo, že obezita zhoršuje reakce B buněk na očkování a studie naznačují, že za to může být částečně zodpovědný leptin [169].
Post-transkripční glykosylace protilátek navíc moduluje jejich funkci a změněné vzorce glykosylace jsou spojovány se stárnutím [170,171]. 4-Aktivita galaktosyltransferázy se zvyšuje s věkem [172], což by mělo funkční důsledky, i když dosud neprozkoumané.
Metabolismus v trénované imunitě
Metabolické přeprogramování je jedním z klíčových mechanismů, které jsou základem trénované imunity (také známé jako vrozená imunitní paměť), spolu s remodelací chromatinu. Ve skutečnosti mohou metabolické změny řídit epigenetické změny, protože určité metabolity, např. acetyl-CoA, mohou regulovat epigenetické enzymy [173]. Fumarát je jedním příkladem metabolitů TCA, které řídí epigenetické změny. Dokáže navodit trénovanou imunitu sám o sobě a jeho akumulace během tohoto procesu indukuje trimethylaci histonu 3 lysinu 4 na promotorech IL-6 a TNF [104]. To je způsobeno tím, že fumarát inhibuje aktivitu lysin-specifické histondemethylázy KDM5.
Dráha AKT/mTOR/HIFl je nejkritičtější cestou pro navození aerobní glykolýzy v monocytech trénovaných na glukan[174]. Na rozdíl od trénované imunity indukované glukanem, BCG upreguluje nejen glykolýzu, ale také OXPHOS [175]. Glutaminolýza a syntéza cholesterolu jsou další klíčové metabolické dráhy pro trénovanou imunitu indukovanou glukanem[104]. Přerušení těchto drah blokuje tyto procesy in vitro a in vivo. BCG také indukuje glutaminolýzu a dostupnost glutaminu je důležitá pro trénovanou odpověď [175].

Pro trénovanou imunitu není nezbytná samotná syntéza cholesterolu, ale spíše akumulace intermediárního mevalonátu. Blokování tvorby mevalonátu inhibuje trénovanou imunitu, zatímco samotný mevalonát může indukovat trénovanou imunitu v monocytech prostřednictvím aktivace receptoru inzulinového růstového faktoru 1 (IGF1) a mTOR [176].co je cistancheKromě toho jsou změny v glykolýzových a mevalonátových drahách pozorovány nejen v monocytech, ale také v HSPC [108].
oxLDL, nemikrobiální induktor vrozené imunitní paměti, upreguluje jak glykolýzu, tak spotřebu kyslíku a vysoká dostupnost glukózy dále zvyšuje trénovanou imunitní odpověď[103]. Podobně je katecholaminem navozená trénovaná imunita doprovázena zvýšenou glykolýzou a spotřebou kyslíku. Je třeba poznamenat, že konkrétní metabolické přepojení se může lišit pro různé induktory vrozené imunitní paměti. Například stimulace aldosteronem není spojena se zvýšenou glykolýzou nebo OXPHOS, ale je závislá na syntéze mastných kyselin [177].
Trénované imunitní reakce a související metabolické stavy nebyly dosud v kontextu stárnutí charakterizovány. Nicméně několik probíhajících rozsáhlých studií BCG vakcinace u starších osob by brzy vrhlo světlo na účinky BCG-indukované trénované imunity na metabolismus stárnutých imunitních buněk (NCT04537663, NCT04417335).
Role epigenetických změn v imunitní paměti
Epigenetické změny zahrnují modifikace histonů a metylaci DNA, které regulují způsob, jakým gen funguje. Tyto modifikace jsou dynamické a ovlivňují všechny buňky a tkáně po celý život. Životní prostředí a životní styl, stejně jako stárnutí, mohou vést k dramatickým epigenetickým změnám. Pro účely tohoto přehledu se zaměříme na to, jak věkově závislé epigenetické modifikace mění vrozenou a adaptivní imunitní paměť.
Methylace DNA v adaptivní imunitě
Metylace DNA je nejhojnější epigenetickou modifikací, ke které dochází přenosem methylové skupiny na 5. uhlík cytosinu [178]. Methylace DNA ne vždy ukazuje na nižší genovou expresi; methylace v genových promotorech je však obecně spojena se špatnou vazbou TF a sníženou transkripcí [179]. Biologické pohlaví, genetické pozadí, faktory prostředí a věk ovlivňují profil metylace DNA [180]. Mezi těmito faktory je velmi dobře charakterizována metylace závislá na věku. Je pozoruhodné, že jsou vyvinuty různé matematické modely pro predikci biologického věku na základě úrovní metylace určitých míst CpG z různých tkání nebo buněk [180-182].
Postupující věk je spojen s progresivní ztrátou methylačních značek na DNA [183], i když u některých genových promotorů jsou také pozorovány abnormální hypermetylační vzorce [184]. Změny v methylačním prostředí jsou Ztráta kostimulačního proteinu CD28 v CD4 plus T buňkách je jedním z dobře charakterizovaných známek stárnutí, což vede ke zhoršené aktivaci a diferenciaci T buněk. Srovnání methylačních profilů CD28 plus a CD28"1 T buněk odhalilo 296 odlišně metylovaných genů spojených se špatnou TCR signalizací a cytotoxickou odpovědí[194]. Navíc exprese genů zapojených do aktivace zánětu byla vyšší u CD28nul T buněk, což naznačuje že tyto buňky mají vyšší stav před aktivací. Jiná studie uvádí, že zvýšená methylace na BACH2 lokusu CD4 plus T buněk ve skupinách středního a vysokého věku vede k nižší expresi BACH2 [195]. BACH2 má regulační roli v imunitní odpovědi, modulace diferenciace CD4 plus T buněk a kontrola zánětu [196] Celkově změny ve vzorcích metylace DNA přispívají k tomu, že se CD4 plus T buňky stávají více zánětlivými u starších osob.
Několik studií vrhlo světlo na profil metylace DNA B buněk během aktivace a onemocnění [197-200]; zda jsou však B buňky ovlivněny metylačními změnami závislými na věku, je zatím známo.
Histonové modifikace v adaptivní imunitě
N-terminální histonové konce jsou cíle pro posttranslační enzymatické modifikace včetně acetylace, methylace, fosforylace, ubikvitylace a sumoylace [201]; tento přehled se však zaměří na methylaci a acetylaci, což jsou nejlépe charakterizované změny regulující strukturu histonů. Methylové skupiny se k histonu přidávají pomocí histonmethyltransferáz a odstraňují pomocí histondemethyláz [202]. Trimethylace histonu 3 lysinu 4 (H3K4me3), histonu 3 lysinu 36 (H3K36) a histonu 3 lysinu 79 (H3K79) jsou spojeny s otevřenými a aktivně transkribovanými oblastmi [203]. Na druhé straně monomethylace histonu 3 lysinu 9 (H3K9me), histonu 3 lysinu 27 (H3K27me) a histonu 4lysinu 20 (H4K20me) je spojena s uzavřenými a neaktivními oblastmi chromatinu. Kromě toho je acetylace histonů spojena s uvolněnou strukturou chromatinu a zvýšenou transkripcí genu [204]. Histonové acetyltransferázy katalyzují acetylaci lysinu, zatímco histonové deacetylázy (HDAC) modifikaci ruší [205]. Posttranslační modifikace histonů neovlivňují pouze dostupnost a transkripci genů, ale také modulují alternativní sestřih, replikaci a opravu DNA [206]. Histony a epigenetické značky na histonech podléhají přechodům se stárnutím. HSC ze starých myší mají více píku H3K4me3 a H3K27me3 ve srovnání s mladými HSC [186]. Navíc exprese FLT3, jednoho z regulátorů CLP, byla snížena v důsledku H3K27me3 u starých HSC, což naznačuje souvislost mezi špatným lymfoidním diferenciačním potenciálem HSC u seniorů. Rozsáhlá studie provedená na mladých a starých monozygotních dvojčatech ukázala, že modifikace chromatinu během stárnutí jsou nedědičné [207]. Profily modifikace histonů jsou navíc do určité míry homogenní u mladých jedinců a heterogenní u starších jedinců. Heterogenita v modifikacích histonů byla pozorována mezi jednotlivci a také typy buněk u starších osob.

Epigenetické změny jsou jednou ze základních příčin hlavních defektů pozorovaných u CD8 plus T buněk starších osob. Uzavřenější chromatinové oblasti jsou pozorovány v oblastech zesilovače a promotoru genů souvisejících se signalizací T buněk u starších osob ve srovnání s mladými [208]. Kromě toho je -7R v paměťových CD8 plus T buňkách jedním z hlavních genů souvisejících s mnohočetnými uzavřenými vrcholy chromatinu u starších osob. Protože IL-7 zajišťuje homeostázu a udržování T a B buněk, špatná signalizace IL-7 u starších osob může být základním důvodem zhoršené adaptivní imunitní odpovědi [209]. Navíc naivní CD8 plus buňky u starších osob mají nižší dostupnost chromatinu na genových promotorech spojených se špatnou vazbou nukleárního respiračního faktoru 1 (NRF1)[140]. Vzhledem k úloze NRF1 v oxidativní fosforylaci by snížená aktivita chromatinu mohla částečně vysvětlit narušený metabolismus CD8 T buněk u starších osob [210]. Dalšími významnými zjištěními studie je, že otevřené chromatinové oblasti jsou spojeny s profilem paměťových buněk a dostupnost promotorů je u starších jedinců snížena.
Jak bylo zmíněno v části methylace DNA, v CD4 plus T buňkách je pozorováno snížení exprese BACH2 související s věkem. Další mechanismus vedoucí k nižší transkripci genu BACH2 je způsoben nedostatkem meninu pozorovaným při imunitní senescenci [211]. Menin indukuje expresi BACH2 vazbou na jeho lokus a udržováním acetylace histonů. Snížená vazba Meninu na lokus BACH2 a následně snížená exprese BACH2 přispívá k imunosenescenci v CD4 plus T buňkách. Studie zkoumající epigenetické změny v prekurzorech B buněk u starých a mladých myší spojovala tyto změny s genovou expresí [212]. Ukázalo se, že staré pre-B buňky vykazují ztrátu H3K4me3 v místě promotoru substrátu inzulínového receptoru 1 (IRSI), což je spojeno s nižší transkripcí. Vzhledem k tomu, že inzulínová signalizace je nezbytná pro vývoj B buněk v kostní dřeni[213], může snížená signalizace inzulínového růstového faktoru (IGF) vést k defektům ve vývoji B buněk.
Epigenetické přeprogramování jako znak trénované imunity
Výrazný epigenetický profil reguluje trénované imunitní reakce po prvním poškození. V důsledku určitých infekcí nebo stimulací procházejí primárně aktivované buňky epigenetickým přeprogramováním, které jim umožňuje silnější odpověď na heterologní infekci usnadněním transkripce genů souvisejících se zánětem a metabolismem [106].
H3K4me3 je první charakterizovaná epigenetická značka v monocytech po léčbě -glukanem [91]. Další analýza odhalila, že píky H3K4me3 jsou obohaceny v promotorových místech genů TNF, IL6, IL18, DESTINY a MYD88, což ukazuje, že genové transkripce jsou v těchto oblastech aktivnější. Navíc zvýšený H3K27ac je dobře charakterizovaný histonový znak v trénovaných buňkách, který podporuje glykolýzu a aktivaci dráhy PI3K/AKT [174, 214]. Kromě obohacení o H3K4me3 a H3K27ac byl snížený H3K9me3 nalezen v promotorech genů souvisejících s produkcí cytokinů a glykolýzou[175]. Protože H3K9me3 je represivní značka, snížená trimethylace naznačuje přítomnost otevřených chromatinových oblastí. Tyto studie ukazují, že trénované imunitní reakce jsou modulovány epigenetickými modifikacemi, které usnadňují zesílené cytokinové reakce a specifické metabolické změny. Trénované buňky sdílejí společný epigenetický profil; různé podněty by však mohly vést k menším jedinečným epigenetickým změnám.
Infekce a určité stimulace zanechávají stopy na profilu metylace DNA, stejně jako histony, buněk vrozené imunity [215]. Studie prokazují roli metylace DNA v antimykobakteriální odezvě po BCG vakcinaci, přičemž rozlišují respondéry od nereagujících [216,217]. Respondenti na BCG vakcinaci se vyznačovali sníženou metylací DNA na promotorech zánětlivých genů [216]. Stále se však zkoumá, zda DNA(de)methylace hraje přímou roli ve vývoji nespecifických ochranných reakcí.
Stejně jako u dospělých je u starších lidí trénovaná imunita modulována modifikacemi histonů. Giamarellos-Bourboulis a kolegové nedávno ukázali, že zvýšená produkce cytokinů po BCG vakcinaci u starších osob byla doprovázena acetylací H3K27 v promotorových oblastech genů TNF a IL6 [113]. Je však třeba provést další studie, které porovnají epigenetické rozdíly po vývoji vrozené imunitní paměti mezi dospělými a staršími jedinci a prozkoumají, jak stárnutí ovlivňuje epigenetické známky v kontextu trénované imunity.
Střevní mikrobiota modulující imunitní paměť
Stárnutí způsobuje změny v celém lidském těle a biliony mikrobů žijících tam nejsou žádné výjimky. Složení a diverzita střevní mikroflóry se dynamicky posouvá v kojeneckém věku, zůstává relativně stabilní v dospělosti a se stářím začíná klesat [218].
Interakce mikrobioty a adaptivního imunitního systému
Střevní mikroflóra má zásadní roli ve výchově adaptivního imunitního systému tím, že navozuje určitou úroveň imunitní odpovědi a dolaďuje zánět. Například Bacteroides fragilis, komenzál ve střevě, zvyšuje a reguluje diferenciaci CD4 plus T buněk na T helper 1 (Th1) a Th2[219]. V přítomnosti střevních bakterií a TGF se naivní CD4 plus T buňky stávají Tregs, produkující IL-10 k udržení imunitní homeostázy. Na druhé straně buňky Tregs a Th17 v lymfoidních folikulech střeva indukují změnu třídy B buněk, což vede k sekreci IgA [220,221]. Sekrece IgA, IgM a IgG z B buněk spojená s mikrobiotou také probíhá prostřednictvím aktivace signalizace TLR bez pomoci T buněk [22].
Adaptivní imunitní systém může omezit zánětlivou reakci proti komenzálním střevním mikrobům zprostředkovanou vrozeným imunitním systémem. IgA produkovaný B buňkami je vysvětlován jako součást udržitelné interakce hostitel-mikrob, která kontroluje zánětlivou odpověď proti prospěšným mikroorganismům [223]. Kromě toho střevní Treg buňky exprimují TCR pro střevní antigeny, jako jsou metabolické produkty a komenzály, zatímco jiné Treg v těle exprimují TCR pro vlastní antigeny [224]. Tímto způsobem střevní Treg potlačují imunitní reakce proti střevním antigenům a hrají imunoregulační roli v útrobách.
Jak mikrobiota nápadně formuje vývoj adaptivního imunitního systému, bylo prokázáno také u bezmikrobních myší: nedostatek mikrobiálních druhů ve střevě je charakterizován defekty ve vývoji sekundární lymfatické tkáně [225] a nízkou produkcí IgA[226] a sníženým Th17 buňky a Tregs [227]. Je třeba poznamenat, že mastné kyseliny s krátkým řetězcem (SCFA) produkované mikrobiálními druhy ve střevě významně přispívají k rozvoji imunitního systému a reakcím [228].
Zdravé složení střevní mikroflóry je důležité pro ochranu jedinců před nemocemi. Například IL-10 vylučující IgA plus plazmatické buňky a plazmablasty pocházející ze střeva propůjčují rezistenci k experimentální autoimunitní encefalomyelitidě indukované u myší [229]. Jiná studie uvádí, že střevní mikroflóra chrání před respiračními infekcemi vyvolanými S. pneumoniae a K. pneumoniae indukcí sekrece GM-CSF a IL-17A [230].
Role dysbiózy ve stárnutí
Výskyt střevní dysbiózy, nerovnováhy mikrobiálních druhů, se zvyšuje s věkem a je spojen s četnými zdravotními problémy [231]. Není však jasné, zda buněčné a molekulární změny imunitních buněk během stárnutí ovlivňují složení a fungování střevní mikroflóry, nebo zda dysbióza související s věkem spouští defektní imunitní reakce. Je pravděpodobné, že obojí je současně pravdivé, ale k vyřešení této otázky je nutné lepší pochopení interakcí střevní mikroflóry a imunitního systému.
Jak jednotlivci stárnou, úbytek určitých prospěšných bakteriálních druhů, jako je Bifidobacterium, je nahrazen růstem patogenních druhů, tj. Enterobacteriaceae [232]. U starších lidí je také hlášen pokles Firmicutes a nárůst Proteobakterií [233]. Kromě toho je střevní dysbióza spojena s několika nemocemi souvisejícími s věkem, včetně obezity [234], diabetu 2. typu [235], Alzheimerovy choroby [236] a zvýšeného výskytu infekcí [237-239]. Riziko vzniku rakoviny je také vyšší u starších osob kvůli chronickému zánětu spojenému s dysbiózou, oslabené fagocytóze senescentních a dormantních nádorových buněk a zhoršené aktivaci nádorově specifických CD8 plus T buněk [240].
Dysbióza byla také považována za hlavní důvod různých patologií souvisejících s věkem a předčasné smrti u starších jedinců, protože spouštěla nadměrný zánět a několik komplikací, včetně prosáknutí střeva a snížených funkcí gastrointestinálního traktu [228]. V souladu s tím konkrétní složení a rozmanitost mikrobiálních druhů koreluje se zdravím, zdatností a zvýšeným přežitím u starších osob [241,242]. Nedávná studie odhalila, že zdraví starší lidé zažívají zvláštní posun ve složení mikrobioty, zatímco u křehkých starších lidí tento posun chybí [242]. Kromě toho vysoký výskyt bakterií Bacteroides během stárnutí koreluje se sníženou mírou přežití během 4-ročního sledování. Další nedávná práce s 15letým sledováním uvádí, že abundance Enterobacteriaceae byla významně spojena s úmrtími souvisejícími s gastrointestinálními a respiračními příčinami u starších osob [243].
Dysbióza může vést k poruchám integrity střevní bariéry, což vede k translokaci bakteriálních druhů do hostitelských tkání. Tyto bakterie vytvářejí zánět prostřednictvím náboru neutrofilů a diferencovaných buněk Th17 [244]. Například translokace grampozitivních patobiontů E. gallinarum, která je důsledkem defektů ve střevní bariéře, indukuje odpověď Th17 a produkci autoprotilátek [245].
Akkermansia je prospěšný komenzál, o kterém bylo prokázáno, že chrání integritu střevní bariéry [228] a zvyšuje odpověď protilátek a T buněk [246]. Ztráta Akkermansie je spojena s inzulinovou rezistencí u starých primátů a myší [247. Snížené množství butyrátu a akkermansie zvyšuje prosakování střev, což zase zvyšuje prozánětlivé reakce.
Studie na lidech na druhou stranu uvádí, že Akker-mánie je častější u starších lidí [248]. Kromě toho Akkermansia významně korelovala se sérovými IgA a CD8 plus T buňkami a negativně korelovala s CD4 plus T buňkami u starších lidí. Bacteroidetes, které jsou méně četné u starších osob, pozitivně korelovaly s hladinami IgG v séru a četností CD4 plus T buněk ve střední věkové skupině. Na závěr tato studie zdůrazňuje vztah mezi adaptivním imunitním systémem a složením střevní mikroflóry, i když mezi nimi chybí přímá souvislost.
Mikrobiota také ovlivňuje průběh onemocnění a reakce na vakcínu u starších osob. I když je antivirová terapie viru lidské imunodeficience (HIV) úspěšná a zvyšuje očekávanou délku života pacientů, starší HIV plus lidé trpí více komorbiditami než HV-starší lidé. HIV plus starší lidé mají méně CD4 plus T-buněk a více CD8 plus T-buněk než HIV jedinci starší 55 let[249]. Kromě toho je výskyt Prevotella ve střevě významně vyšší u jedinců s nízkým počtem CD4 plus T-buněk. Prevotella byla dříve spojována s kardiovaskulárními chorobami [250], ale jak interaguje s imunitním systémem, není dosud jasné. Změny střevní mikroflóry závislé na věku pravděpodobně přispívají ke špatným imunitním odpovědím po očkování [251]. Některé studie uvádějí, že probiotické doplňky zvyšují titry protilátek po vakcíně proti chřipce u starších osob [252-255], zatímco několik studií prokázalo omezený nebo žádný účinek [87,256,257]. Rozdíly ve výsledcích mohou být způsobeny více faktory, včetně velikosti vzorku, typu probiotik a cesty podání. Nicméně studie silně naznačují, že nerovnováha v mikrobiotě způsobuje zhoršené imunitní reakce a obnovení zdravého složení může být prospěšné pro lepší odpověď na vakcínu u starších lidí.
Indukce přirozené imunitní paměti střevní mikrobiotou
Jako buňky adaptivní imunity členové vrozeného imunitního systému úzce interagují se střevní mikroflórou. Několik studií naznačuje, že mikrobiota by mohla regulovat vývoj imunitní paměti primární aktivací nebo tolerizací buněk mikrobiálními antigeny a SCFA. Například -glukan, složka buněčné stěny plísní, a BCG působí prostřednictvím signálních drah Dectin-1 a NOD2 [91,100]. Vzhledem k tomu, že dektin-1 a receptory podobné Nodům (NLR) se nacházejí na různých typech buněk ve střevech, včetně neimunitních buněk, je pravděpodobné, že se u těchto buněk vyvine imunitní paměť kvůli jejich expozici střevnímu mikrobiomu . Na podporu tohoto argumentu se ukázalo, že peptidoglykanové fragmenty odvozené ze střevní mikroflóry aktivují vrozený imunitní systém a podporují schopnost zabíjení neutrofilů [258].
Dále bylo prokázáno, že střevní mikrobiota indukuje myelopoézu k ochraně myší před infekcí [259], podobně jako zvýšení počtu myeloidních progenitorů v kostní dřeni myší po trénovaném navození imunity podáváním -glukanu [108]. Další složky odvozené od mikrobioty, jako je lipopolysacharid (LPS), flagellin a -glukan, by také mohly být schopny vyvolat trénovanou imunitu ve střevech, ačkoli dávka stimulů je kritická pro imunitní paměť nebo toleranční odpověď [260]. Jak již bylo zmíněno, trénovaná imunita je zprostředkována rozsáhlým metabolickým a epigenetickým programováním. Molekuly a metabolity produkované komenzálními střevními mikroby a mikroby samotné jsou schopny vyvolat takové změny v buňkách vrozené i adaptivní imunity [261]. Například, přestože butyrát produkovaný střevními mikroby způsobuje zvýšení antimikrobiální aktivity, má účinky opačné než trénovaná imunita u makrofágů, pravděpodobně pocházející ze snížené aktivity mTOR a inhibice HDAC3 [262].
Je důležité poznamenat, že neimunitní buňky, např. fibroblasty [263], epiteliální buňky [264] a buňky intestinálního stromatu (ISC)[265], jsou také schopny vytvářet imunitní paměť a vykazují zvýšenou schopnost reagovat po sekundární infekci. Bylo prokázáno, že ISC mohou odstranit infekci rychleji během sekundární související nebo nesouvisející infekce, což ukazuje na přítomnost imunitní paměti [266]. Proto také neimunitní buňky přispívají k homeostáze mezi střevními mikroby a imunitním systémem.
S ohledem na silné vazby mezi střevní mikroflórou a indukcí vrozené imunitní paměti by bylo možné vyslovit hypotézu, že trénovaná imunitní odpověď by mohla být dysregulována dysbiózou u starších osob. Špatně trénovaná imunitní reakce by mohla způsobit, že starší lidé jsou náchylnější k infekcím, zatímco bujná reakce může přispět k patogenezi onemocnění. Je však zapotřebí více výzkumu, abychom pochopili, jak změny mikrobioty související s věkem ovlivňují vrozenou imunitní paměť.
Cross talk mezi imunitním systémem a mozkem
Stárnutí způsobuje velké poškození centrálního nervového systému (CNS) poškozením DNA, hromaděním odpadních produktů, oxidačním stresem, narušenou energetickou homeostázou a zhoršenou funkcí [267]. Mozek a zbytek CNS nejsou imunologicky izolovány, jak se kdysi myslelo: mezi imunitním systémem a CNS dochází k rozsáhlému vzájemnému propojení. Homeostáza a regenerace mozku závisí na silném imunitním systému [268]. Proto zhoršování imunitního systému ve stáří přispívá a eskaluje stárnutí mozku a neurodegenerativní onemocnění.
V parenchymu CNS je rezidentním typem imunitních buněk mikroglie, které pocházejí z primitivních progenitorů makrofágů ve žloutkovém váčku na počátku vývoje [269]. Mikroglie jsou nesmírně důležité pro udržení zdravého mozku. Provádějí imunosurveillanci, reagují na infekce, organizují komunikaci s cirkulujícím imunitním systémem, regulují neurony a další typy buněk v mozku, fagocytují buněčné zbytky, špatně složené proteiny, toxické produkty a dokonce synapse [270]. Mikroglie se stárnutím mění a přispívají k neurodegenerativním onemocněním souvisejícím s věkem [271]. Jejich fagocytární kapacita se s postupujícím věkem snižuje a přispívají ke stavu chronického zánětu nízkého stupně. Vzhledem k tomu, že se tato recenze zaměřuje na imunitní paměť, nebudeme se podrobně zabývat mikrogliemi a místo toho se zaměříme na roli adaptivní imunity a trénované imunity v kontextu stárnutí mozku.
Hematoencefalická bariéra (BBB) do značné míry zabraňuje infiltraci imunitních buněk do mozku. Některé typy imunitních buněk jsou však přítomny v mozkomíšním moku (CSF) a hematoencefalické bariéře v choroidálním plexu (CP) [272]. CP, umístěný v mozkových komorách, je síť epiteliálních buněk produkující CSF se zabudovanými kapilárami. T buňky jsou přítomny v CP a regulují transport imunitních buněk do CSF aktivací epitelu CP závislou na IFNy [273].
Imunitní buňky přispívají k přežití neuronů a neurogenezi během homeostázy, po poranění nebo za neurodegenerativních podmínek [272]. Poškození CNS vyvolává ochrannou odpověď T-buněk, která zabraňuje ztrátě neuronů [274]. CD4 plus lymfocyty hrají nejvýznamnější roli v této "neuroprotektivní imunitě".
Neuroprotektivní T-buněčná imunita
CP obsahuje CD4 plus T buňky s fenotypem efektorové paměti, které rozpoznávají CNS specifické autoantigeny [275]. Tyto buňky mohou přijímat signály z oběhu přes epitel a CNS přes CSF a organizovat integrovanou odpověď k udržení mozkové homeostázy [276]. Astrocyty, buněčný typ, který pomáhá udržovat synapse a BBB, kromě různých dalších funkcí, přebírají neuroprotektivní fenotyp a snižují neuronální apoptózu, jsou-li společně kultivovány s T buňkami [277]. Během poranění míchy migrují autoreaktivní T buňky specifické pro CNS do místa poranění, inhibují tvorbu cyst a přispívají k zachování axonů [278].
U myší s deficitem T buněk je proliferace progenitorových buněk snížena, což vede k nižšímu počtu nových neuronů, zatímco neurogeneze je posílena u transgenních myší s nadbytkem CNS-specifických autoreaktivních T buněk [268]. Suplementace cytokinu IFNy odvozeného od T-buněk může zvýšit neurogenezi u starých myší s Alzheimerovou chorobou [279]. CNS-specifické T buňky jsou také kritické pro prostorové učení a paměť. U imunodeficientních myší je prostorová paměť narušena, ale může být obnovena rekonstitucí imunitních buněk i u starých myší [280]. V modelech onemocnění motorických neuronů amyotrofická laterální skleróza (ALS) nedostatek T buněk urychluje onemocnění, zatímco rekonstituce podporuje neuroprotekci a zpomaluje progresi onemocnění [281-283]. Je však třeba poznamenat, že T buňky přispívají k smrti dopaminergních neuronů u myších modelů Parkinsonovy choroby [284].
Jedním z mechanismů, kterým T buňky zlepšují udržování mozku, je regulace neurotrofického faktoru odvozeného z mozku (BDNF). a vyhledávání [286,287] a je regulováno antidepresivní léčbou [288]. Hladiny BDNF jsou nižší u myší s deficitem T-buněk [268]. BDNF je spojen s depresivním chováním a imunizací myší peptidem odvozeným od myelinu, vytváří CNS specifickou imunitu, obnovuje hladiny BDNF, zlepšuje neurogenezi a snižuje depresivní chování [289]. Kromě toho je zdravá stresová reakce u myší spojena s obchodováním T buněk v mozku a hladinami BDNF. Úzkostné chování způsobené stresem je také sníženo imunizací peptidem odvozeným od myelinu [290]. Kromě neuronů a mikroglií se ukázalo, že samotné T buňky vylučují BDNF [291].
Ukázalo se také, že Tregs jsou protektivní a zpomalují progresi onemocnění u ALS snížením mikrogliální aktivace [292]. U modelů Alzheimerovy choroby transplantace Treg zvyšuje kognitivní schopnosti a redukuje amyloidní plaky [293]. Navíc nižší poměr Treg/Th17 koreluje se závažnějším onemocněním u pacientů s roztroušenou sklerózou, vysilujícím autoimunitním onemocněním postihujícím neurony [294].
I když by přebujněná imunitní reakce narušila funkci mozku, vyladěná imunita T buněk je jednoznačně životně důležitá pro zdravou mozkovou homeostázu a zotavení po zranění. Jakýkoli zásah zaměřený na tento jev musí být pečlivě kontrolován, aby se zabránilo zánětlivému poškození; nicméně poznatky o úloze adaptivní imunity ve zdraví mozku otevírají nové cesty, jak čelit poranění mozku nebo neurodegenerativním onemocněním souvisejícím s věkem.
Trénovaná imunita v mikroglii
Nedávné studie naznačují, že vrozená imunitní paměť může být indukována v mikrogliálních buňkách. Jedna studie zjistila epigenetické přeprogramování v mikrogliích přítomné po dobu nejméně 6 měsíců po systémovém podávání LPS [295]. Je zajímavé, že zatímco jediná injekce LPS indukovala trénovaný fenotyp u mikroglie, opakovaná injekce LPS vedla k navození tolerance. Podobně bylo zjištěno, že podávání nízkých dávek TNF také indukuje trénink mikroglií. U myšího modelu Alzheimerovy choroby trénovaná imunita nemoc zhoršila, zatímco tolerance ji zmírnila. Nedávná studie potvrdila zjištění LPS-indukovaného tréninku a prokázala, že systémové podávání glukanu může také indukovat trénovanou imunitu u mikroglií [296]. Trénovaný fenotyp mikroglie byl však pozorován pouze dva dny po primární aktivaci a již nebyl přítomen v den 7, což pravděpodobně ukazuje na nedostatek trvalého epigenetického přeprogramování. Proto stojí za to prozkoumat sílu a vytrvalost tréninku s různými dávkami a různými injekčními režimy.
Stárnoucí mozek
Mnoho mozkových funkcí se stárnutím zhoršuje, některé dokonce začínají klesat po třetí dekádě života [297]. Mezi narušené funkce patří rychlost zpracování, řešení problémů, plynulé uvažování, percepční schopnosti, verbální plynulost a pracovní paměť. Postižení však nemusí nutně korelovat s chronologickým věkem. Je to spíše výsledek zvýšených požadavků na údržbu prostřednictvím hromadění poškození a neschopnosti imunitního systému monitorovat mozek, aby tyto požadavky splnil. Stárnutí samozřejmě přispívá jak k poptávce, tak k neschopnosti imunitního systému prostřednictvím mechanismů diskutovaných dříve.
U starých mikroglií se vyvine prozánětlivý fenotyp [298]. Po poranění hlavy nebo infekci produkují nadměrné množství prozánětlivých cytokinů po delší dobu ve srovnání se zdravým mladým mozkem[299]. Tento zánětlivý stav vede k inhibované neurogenezi [300, 301]. Prozánětlivé prostředí také inhibuje modulátory dlouhodobé paměti, jako je BDNF a na aktivitě závislý cytoskeletální protein, a způsobuje dysfunkci paměti [299]. Hladiny cirkulujícího BDNF u lidí klesají s věkem a u modelů na hlodavcích se ukazuje, že hladiny v mozku klesají [302], což může odrážet pokles počtu a funkce T buněk související s věkem.
Stárnutí je také spojeno se zvýšeným náborem efektorových paměťových CD8 plus T buněk do CP a mozkových blan – membrán pokrývajících mozek [303]. Ukázalo se, že tyto buňky narušují mikrogliální funkci během homeostázy, ale zvyšují produkci prozánětlivých cytokinů po poranění. Navíc jsou počty Treg zvýšené u starších jedinců; jejich migrační kapacita a funkce jsou však pravděpodobně narušeny, protože nejsou schopny řídit neurodegeneraci. Například Tregs pacientů s roztroušenou sklerózou mají menší imunosupresivní kapacitu a nejsou schopni přežít ve sklerotických lézích v mozku [304].
V případě chronického zánětu, zatímco vrozené imunitní buňky typicky vykazují toleranci vedoucí k nižší produkci cytokinů, mikroglie získávají připravený projevovat zánětlivější fenotyp, což urychluje kognitivní pokles [305]. Navíc vysoké hladiny cirkulujícího TNFa pozorované u stárnoucích organismů může také způsobit poškození indukcí trénované imunity u mikroglií, jak je uvedeno výše. Proto je dobře vyvážená vrozená imunita pro zdravé udržování mozku stejně nezbytná jako adaptivní imunita.
Řešení imunitního stárnutí ze všech úhlů
Úsilí zpomalit nebo vrátit stárnutí není zdaleka vzácné. Měření výsledků hodnocená většinou studií jsou však omezená v tom smyslu, že nenabízejí mechanické pohledy ani se nezaměřují na konkrétní procesy. Přesto některé vzrušující intervence, včetně kalorické restrikce, metforminu a fyzického cvičení, zasahují do stárnutí na mnoha úrovních, včetně imunity, metabolismu, epigenetiky, mikrobioty a nervového systému (obr. 2). Následující kapitoly pojednávají
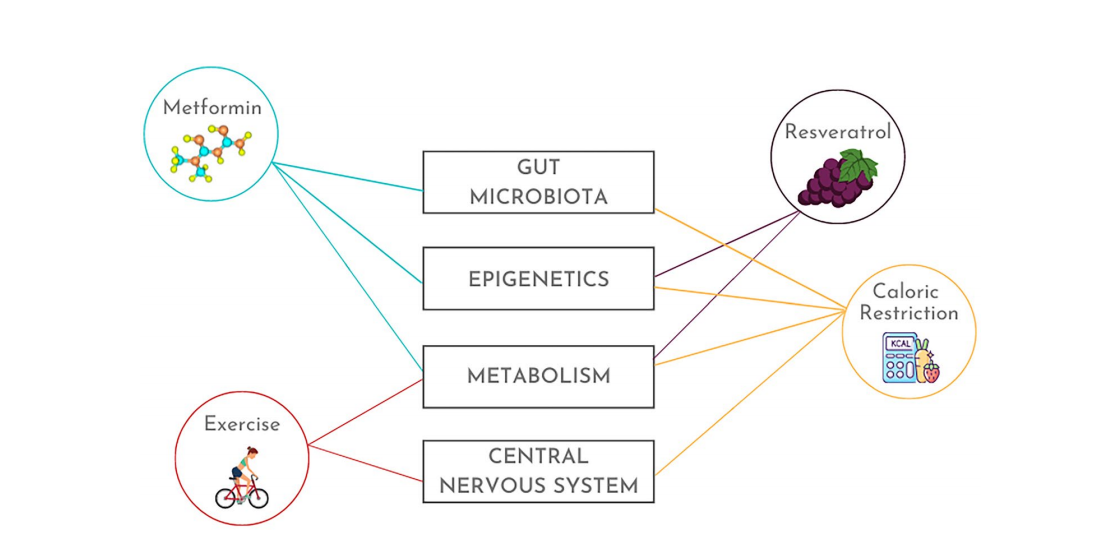
Obr. 2 Slibné intervence proti stárnutí, které se zaměřují na více aspektů procesu stárnutí. Metformin oddaluje stárnutí kmenových buněk, zlepšuje mitochondriální funkci, zabraňuje zkracování telomer, ruší epigenetické modifikace související s věkem a snižuje prosakování střev a dysbiózu. Fyzické cvičení, i když je zahájeno v pozdním věku, zlepšuje počet a funkce imunitních buněk, obnovuje mitochondriální metabolismus, zabraňuje stárnutí buněk, působí proti poklesu kognitivních funkcí a snižuje riziko neurodegenerativních onemocnění. Resveratrol, dostupný v hroznech a červeném víně, působí jako antioxidant, prodlužuje životnost v různých modelových organismech, zmírňuje systémové záněty a zpomaluje epigenetické stárnutí. Kalorické omezení o 20-40 procent prodlužuje délku života a snižuje úmrtnost ze všech příčin u subhumánních primátů, oddaluje epigenetické stárnutí, obnovuje střevní mikroflóru a zpomaluje kognitivní pokles. Mezi buněčné mechanismy sdílené těmito léčbami patří omezení osy mTOR/AKT a aktivace AMPK a SIRT1 různými způsoby, jak řešit problém stárnutí a podrobně popsat mechanismy nejslibnějších léčeb proti stárnutí.
Metabolické zásahy
Po většinu lidské evoluce byly živiny vzácné a k jejich získání bylo zapotřebí velké fyzické aktivity. Lidé se tak vyvinuli, aby se těmto podmínkám přizpůsobili. Náš současný sedavý způsob života s nadbytkem živin má za následek vysokou prevalenci metabolických onemocnění, jako je obezita, diabetes a kardiovaskulární onemocnění [306]. Kromě toho je věk rizikovým faktorem pro tyto stavy, jak již bylo zmíněno, a imunosenescence má mnoho společného s profily metabolických onemocnění. Proto je zaměření na metabolické intervence rozumným přístupem k současnému řešení stárnutí a metabolických poruch. Kalorická restrikce (CR) a cvičení, které nás přibližují k podmínkám předků, se ujímají vedení v této linii výzkumu.
CR označuje snížení celkového příjmu kalorií o 20-40 procent. Od kvasinek po neprimáty se opakovaně prokázalo, že CR prodlužuje délku života [307]. U opic rhesus snížila CR od mladé dospělosti riziko úmrtnosti na příčiny související s věkem trojnásobně a úmrtnost ze všech příčin o 1.{101} {6}}krát [308]. V jiné studii CR snížila výskyt diabetu, rakoviny a kardiovaskulárních onemocnění a zároveň oddálila nástup onemocnění [309]. Kontrastní studie neuvedla žádné zlepšení přežití, i když výskyt rakoviny a diabetu byl snížen [310].
V randomizované kontrolované studii 218 neobézních lidí 2-letá CR dieta snížila hladiny cirkulujícího TNF a nápadně snížila markery kardiometabolického rizika, jako je cholesterol a triglyceridy, bez jakýchkoli nežádoucích účinků souvisejících s intervencí [311]. Dosud neexistuje žádná studie na lidech, která by uváděla významný vliv CR na dlouhověkost. K upevnění příslibu CR u lidí jsou zapotřebí velké a rozsáhlé studie s geneticky různorodými populacemi.
Různé metabolické dopady CR zahrnují downregulaci mTOR a inzulinové signalizace a aktivaci SIRT1, které mají všechny široké dopady na funkci imunitních buněk [312]. Ukázalo se, že CR zpomaluje stárnutí T buněk u opic rhesus [313]. Dále byly rozšířeny soubory CD4t a CD8 plus naivních T-buněk a výstup thymu a proliferace T-buněk byly zvýšeny, ale produkce IFNy buňkami CD8 plus byla po CR snížena. Ačkoli se zdá, že snížení počtu přijatých kalorií zvrátilo metabolické změny vyvolané věkem a zlepšilo zdraví a dlouhověkost, je důležité poznamenat, že několik studií na hlodavcích zaznamenalo zhoršenou adaptivní reakci a zvýšenou úmrtnost na chřipku A a viry západonilské horečky u starších zvířat. po CR [314,315]. Nedávná studie na myších však odhalila ochranné účinky CR proti infekci M. tuberculosis. Tento účinek souvisel s metabolickým posunem charakterizovaným inhibicí mTOR, ale současně se zvýšenou glykolýzou a sníženým FAO
zvýšená autofagie [316]. Inhibitor mTOR rapamycin působil synergicky s CR a dále zesiloval autofagii, což vedlo k účinnější inhibici M. tuberculosis.
Podobně jako u CR je i u cvičení slibná interference s imunosenescencí. Pravidelně cvičící starší ženy měly lepší funkce NK a T buněk ve srovnání se sedavými ženami stejného věku [317]. Počet naivních T buněk a výdej thymu byly vyšší u fyzicky aktivních starších osob, podobně jako u mladých dospělých, ve srovnání se sedavými osobami [318]. Měli také nižší cirkulující IL-6 a vyšší IL-7, což je nezbytné pro vývoj T buněk. Počty senescentních CD8 plus T buněk se však mezi skupinami nelišily. Po 8-týdenním tréninkovém programu imunitní buňky starších dospělých vykazovaly zvýšenou autofagii a downregulovaný zánět NLRP3 [319]. Cvičení také zlepšilo mitofágii a mitochondriální biogenezi v buňkách kosterního svalstva i v imunitních buňkách, čímž se obnovil buněčný metabolický stav narušený stárnutím (320).
Kromě zásahů do životního stylu jsou chemické metabolické regulátory také zkoumány pro svůj potenciál proti stárnutí. Metformin, bezpečně používaný u lidí po více než 60 let pro svůj účinek snižující hladinu glukózy, zmírňuje znaky související s věkem prostřednictvím nepřeberného množství mechanismů. Patří mezi ně aktivace AMPK, inhibice mTORCl, zlepšená mitochondriální biogeneze, downregulace signalizace inzulínu/IGF1 a aktivace SIRT1 [321]. Kromě toho met-formin oddaluje stárnutí kmenových buněk a snižuje zkracování telomer. Celkově se zdá, že působí na všechny známky stárnutí. V současné době se plánuje rozsáhlá klinická studie s více než 3 000 jednotlivci ve věku 65-79, která by měla posoudit potenciál metforminu proti stárnutí (https://www.afar.org/tame-trial).
Everolimus, další inhibitor mTOR, zmírnil imunosenescenci a zlepšil protilátkovou odpověď na očkování proti chřipce u starších osob [322]. I když většina podskupin imunitních buněk nebyla v této studii změněna, T buňky pozitivní na protein 1 programované buněčné smrti (PD-1), marker vyčerpání, byly výrazně sníženy. Následná studie s 264 staršími subjekty uváděla upregulovanou antivirovou expresi, zlepšenou odpověď na očkování proti chřipce a celkově méně infekcí [323]. Aktivace SIRT1 je dalším přístupem k řešení imunosenescence. Je známo, že zlepšuje proliferaci a funkci B buněk, a proto by mohl pomoci zlepšit protilátkové odpovědi, které s věkem klesají [324]. SIRT1 může modulovat metabolické dráhy prostřednictvím deacetylace proteinů a histonů [325]. Mezi cíle SIRTl patří NF-KB, hypoxií indukovatelný faktor 1-alfa (HIFla) a transkripční faktory FOXO. Navíc aktivace SIRT1 potencuje BCG-indukovanou trénovanou imunitní odpověď [326]. Navzdory myším studiím s aktivátory SIRT1-ukazujícími opožděné fenotypy související s věkem a delší životnost [327, 328], neexistují žádné důkazy, které by naznačovaly, že SIRTl je u lidí spojen s dlouhověkostí [329].
Resveratrol, polyfenolová sloučenina nacházející se v červeném víně, je silným aktivátorem SIRT1[330]. Je také ukázáno, že aktivuje AMPK, čímž potlačuje signalizaci mTOR[331]. Kromě studií in vitro a modelů zánětlivých onemocnění vykazujících antioxidační a protizánětlivou aktivitu resveratrolu[332] odhalilo několik studií na myších jeho antivirovou kapacitu[333,334]. Pokud jde o dlouhověkost, studie neuvedly významné prodloužení životnosti resveratrolu v zdravé myši [327,335]. U myší krmených vysoce kalorickou dietou však resveratrol posunul transkripční profil směrem k standardním krmeným myším [336]. Také zlepšila citlivost na inzulín a zvýšila přežití. Podobné výsledky byly pozorovány u opic rhesus na dietě s vysokým obsahem tuků a cukrů [337]. Třicetidenní suplementace obézních mužů resveratrolem vyvolala metabolické změny prostřednictvím osy AMPK-SIRT1 a snížila systémový zánět, hladiny glukózy a triglyceridů [338]. Podobná studie však neuvedla žádné příznivé účinky resveratrolu [339].
Celkově existují vysoce slibné terapeutické přístupy zacílené na metabolické dráhy, které jsou základem imunosenescence a metabolických onemocnění souvisejících s věkem. Jsou však zapotřebí rozsáhlé randomizované kontrolní studie na lidech, aby se zjistilo, zda jsou tato vzrušující pozorování u subhumánních primátů a menších modelových organismů přeložitelná pro lidské použití.
Strategie modulující epigenetiku
Epigenetické intervence byly použity u několika nemocí souvisejících s věkem, např. rakoviny, cukrovky a Alzheimerovy choroby; pouze několik studií se však specificky zaměřuje na změny epigenetické struktury závislé na věku (340). Místo toho metabolické intervence používané k zastavení imunogenu také fungují změnou epigenetické krajiny související s věkem. Resveratrol, CR a metformin jsou tři slibné terapeutické možnosti pro rekonfiguraci věkem podmíněné metylace DNA a modifikací histonů u starších osob.
Zajímavá studie odhalila, že regenerace brzlíku vedla k o 2.{1}} roky mladšímu epigenetickému věku [341]. Účastníci ve věku 51 až 65 let podstoupili 1-letou léčbu rekombinantním lidským růstovým hormonem, dehydroepiandrosteronem (DHEA), což je prekurzor steroidního hormonu, a metforminem. Léčba vedla k obnovení funkční hmoty brzlíku, změnám v podskupinách imunitních buněk a produkci cytokinů a také ke změněnému epigenetickému profilu, který byl spojen s nižším věkem.
Opice Rhesus, které byly vystaveny 40% kalorickému omezení, projevily metylační změny nalezené u starších opic pozdě [342]. Ačkoli tato studie neposkytuje přímý důkaz o delší životnosti spojené se zpožděným metylačním driftem, naznačuje, že CR by mohla být použita ke zpomalení procesu stárnutí. V souladu s tím vedlo zlepšení délky života myší pomocí resveratrolu nebo CR k pomalejšímu epigenetickému stárnutí [343]. Bylo také prokázáno, že celoživotní CR zabraňuje změnám metylace DNA v mozku souvisejícím s věkem a poskytuje neuroprotekci [344].
Několik studií vysvětluje, jak může CR ovlivnit epigenetiku. Tyto mechanismy zahrnují sníženou acetylaci histonů zprostředkovanou zvýšenou expresí SIRTI, vyšší aktivitu DNA metyltransferázy (DNMT) a hypermetylaci specifických regulačních genů, jako je Ras [340]. Podobně metformin působí na epigenetické znaky prostřednictvím aktivace SIRT1 a inhibice HDAC (345). Pokud je nám známo, neexistuje žádný výzkum, který by zkoumal účinky CR na epigenetické změny související se stárnutím, pravděpodobně kvůli omezením provádění takových dlouhodobých intervencí na lidech.
Potenciální léčby zaměřené na mikrobiotu
Protože střevní mikroflóra reguluje metabolismus hostitele, zásahy proti stárnutí zaměřené na metabolismus nevyhnutelně ovlivňují střevní mikroflóru. Jako příklad, kromě působení na metabolické dráhy, metformin moduluje střevní mikroflóru. Studie zkoumající účinky metforminu u obézních a starých myší zjistila pokles IL-1 a IL-6 v epididymálním tuku, což bylo spojeno se změnami ve střevních mikrobech [346]. Kromě toho měli pacienti s diabetem 2. typu, kteří užívali metformin, vyšší výskyt Akkermansie ve střevech [347], což korelovalo s nižší bakteriální translokací a rizikem dysbiózy [348]. zánět u myší [349].
Další léčebnou strategií k zastavení imunogenu zacílením na mikroflóru je použití pro- a prebiotik. Probiotika jsou doplňky obsahující živé mikroorganismy, zatímco prebiotika jsou substráty, které mohou mikroorganismy využít k životu [350]. Ačkoli existují protichůdné důkazy, studie naznačují, že pravidelné užívání probiotik může modulovat rozmanitost a početnost střevních mikrobů a snížit tak výskyt dysbiózy [351,352]. Probiotika jsou spojena se zlepšenými imunitními reakcemi evidentními ze zvýšeného počtu B a T buněk, zvýšené aktivity NK buněk [353] a vyšší produkce IgA proti viru chřipky u starších jedinců [354]. Kromě toho suplementace probiotiky pomohla snížit růst oportunních bakterií Clostridium dif-file u starších osob[355]. Na rozdíl od těchto zjištění metaanalýza 10 randomizovaných kontrolovaných studií neprokázala žádný příznivý účinek probiotik na snížení produkce zánětlivých cytokinů [356].
Příznivé účinky má i kombinace probiotik s prebiotiky, tedy synbiotiky, jako suplementace probiotik. Dvouměsíční léčba u starších jedinců synbiotickým přípravkem významně zlepšila parametry metabolického syndromu v oběhu a snížila zánětlivé proteiny, jako je TNF a C-reaktivní protein [357]. Dvojitě zaslepená 4-týdenní studie symbiotické léčby zaznamenala nárůst bifidobakterií, aktinobakterií, Firmicutes a metabolitu butyrátu v léčené skupině ve srovnání s placebem, zatímco proteobakterie a prozánětlivé cytokiny byly nižší [358].
Kalorická restrikce by mohla být další léčebnou strategií ke zlepšení kognitivních funkcí, metabolických parametrů a střevní mikroflóry u starších osob. CR zpomalila kognitivní pokles u myšího modelu Alzheimerovy choroby, spojený se zvýšenými bakteriemi ve střevech. Starší myši, které dostávaly o 30 procent méně kalorií po dobu 2 měsíců, vykazovaly významné posuny ve své mikrobiotě směrem k vyváženějšímu složení podobnému složení mladých myší [359]. Celoživotní CR vyvolala rozsáhlejší změny v mikrobiotě, snížila koncentraci zánětlivých peptidů a prodloužila délku života myší [360]. Nedávná studie však odhalila, že závažná CR, z více než 50 procent, narušuje diverzitu mikrobioty a vede k růstu patogenních bakterií C. difficile [361]. Proto je důležité pečlivě určit rozsah a trvání CR.
Intervence proti stárnutí mozku
Fyzické cvičení je skvělý způsob, jak podpořit zdraví mozku. Cvičení působí proti kognitivním poruchám, snižuje riziko demence, zlepšuje prostorovou paměť a zvyšuje neuroplasticitu [362]. Fyzická aktivita může zmírnit účinky rizikových alel pro poruchu paměti [363] a chránit před rozvojem Alzheimerovy choroby [364,365]. Systematický přehled 16 studií s celkovým počtem 163 797 účastníků uvádí, že pravidelné cvičení vedlo ke snížení rizika demence o 28 % a Alzheimerovy choroby o 45 % [366]. Je třeba poznamenat, že snížení rizika spojeného s cvičením bylo pozorováno ve většině jednotlivých studií bez ohledu na frekvenci a intenzitu cvičení.
Studie naznačují antioxidační a protizánětlivé účinky cvičení jako potenciální mechanismy neuroprotekce [367,368]. Mezi protizánětlivé důsledky cvičení patří snížený cirkulující IL-6, ale zvýšený IL-10 a IL-1RA, nižší počet Treg, vyšší počet zánětlivých monocytů v oběhu a inhibovaná funkce monocytů [ 369]. Kromě toho je fyzické cvičení spojeno se snížením senescentních T buněk, zvýšenou cytotoxicitou NK buněk a fagocytózou neutrofilů a delšími telomerami v leukocytech [370]. Mírné kardiovaskulární cvičení navíc zlepšilo séroprotekci po očkování proti chřipce u starších osob [371]. Zpomalení imunosenescence by omezilo stárnutí mozku a kognitivní úpadek prostřednictvím zlepšeného imunitního dozoru a opravy CNS.
Navíc i jediné cvičení zvyšuje hladinu BDNF, která se dále zvyšuje pravidelným cvičením [372]. Je zajímavé, že nárůst BDNF související s cvičením je výraznější u mužů než u žen. Ukázalo se také, že ketolátky indukují expresi BDNF [373,374], což možná přispívá k neuroprotektivnímu účinku ketogenních diet u neurologických onemocnění [375].
CR je další intervence, o které se ukázalo, že zabraňuje poškození neuronů. Vede ke zvýšené expresi BDNF a zesílené neurogenezi [376], způsobuje energetický posun od glykolýzy k použití ketolátek, chrání integritu bílé hmoty a zlepšuje dlouhodobou paměť u myší (377). U potkanů režim CR obden podporuje odolnost neuronů vůči chemicky vyvolanému poškození [378]. Jeden mechanismus neuroprotekce indukované CR je pravděpodobně způsoben supresí oxidačního stresu v mozku [379,380]. Bylo však hlášeno, že závažná CR s 50procentním snížením příjmu kalorií způsobuje u potkanů depresivní chování [381]. Na myších modelech Alzheimerovy choroby je CR schopna omezit ukládání amyloidních plaků [382, 383], pravděpodobně prostřednictvím mechanismu zahrnujícího aktivaci SIRT1 [384].
Přes všechny pozitivní výsledky u hlodavců nejsou neuroprotektivní účinky CR u subhumánních primátů příliš jasné, zatímco velké studie na lidech chybí [385]. Nicméně malá randomizovaná kontrolovaná studie s lidmi nevedla k žádnému významnému zlepšení kognitivních funkcí [386]. Další klinická studie na starších dospělých prokázala zlepšení skóre paměti po 3 měsících CR [387]. Zlepšená paměť spolu s vyšší funkční konektivitou v hipokampu byla hlášena u obézních žen, které podstoupily 3-měsíční CR dietu [388]. K pochopení rozsahu neuroprotektivních účinků jsou nutné rozsáhlejší studie na lidech s CR.
Je zajímavé, že nedávno bylo prokázáno, že BCG vakcinace snižuje riziko Alzheimerovy a Parkinsonovy choroby u pacientů s rakovinou močového měchýře léčených BCG imunoterapií ve srovnání s neléčenými pacienty [389, 390]. Při léčbě rakoviny močového měchýře se BCG aplikuje přímo do močového měchýře, spíše než obvyklým intradermálním způsobem podání. Vzrušujícími budoucími výzkumnými projekty by bylo hodnocení účinků intradermálního BCG na neurodegenerativní onemocnění a zkoumání základních mechanismů s cílem zjistit, zda trénovaná imunita hraje roli v neuroprotektivních účincích. V současné době probíhá klinická studie s použitím intradermálních BCG injekcí u pacientů s Alzheimerovou chorobou s pozdním nástupem (NCT04449926).
Závěrečné poznámky
Biologické stárnutí je komplexní proces zahrnující všechny systémy organismu. Imunitní systém je v jeho samém středu a interaguje se všemi ostatními. Stárnoucí imunitní systém je mimo jiné viníkem vysoké náchylnosti seniorů k infekcím a metabolickým a neurodegenerativním onemocněním souvisejícím s věkem. Zlepšení vrozených a adaptivních imunologických odpovědí je proto nesmírně důležité pro snížení nemocnosti a úmrtnosti související s infekcí a zvýšení schopnosti reagovat na vakcínu u starších jedinců. Zde jsme také prezentovali velké množství výzkumů naznačujících nové role imunitní paměti v metabolické regulaci a udržování zdravého centrálního nervového systému. Přistupovat ke stárnutí ze všech úhlů, s imunitou jako centrálním uzlem a navrhovat intervence proti stárnutí zaměřené na společné mechanismy všudypřítomně ovlivněné stárnutím je rozumnou cestou k dalšímu výzkumu. Behaviorální intervence, jako je omezení kalorií a fyzické cvičení, stejně jako farmakologické látky, jako je metformin a resveratrol, jsou schopny regulovat mnoho aspektů stárnutí a přinesly slibné výsledky na zvířecích modelech i na lidech. Komplexní strategie je nezbytná pro lidské bytosti, které se snaží vést dlouhý život se zdravými střevy, funkčním mozkem a bez závažných infekcí.
Prohlášení
Střet zájmů Autoři neuvádějí žádné konkurenční zájmy.
Otevřený přístup Tento článek je licencován podle Creative Commons Attribution 4.{1}} Mezinárodní licence, která umožňuje použití, sdílení, adaptaci, distribuci a reprodukci na jakémkoli médiu nebo formátu, pokud uvedete příslušné jméno původního autora (s) a zdroj, uveďte odkaz na licenci Creative Commons a uveďte, zda byly provedeny změny. Obrázky nebo jiný materiál třetích stran v tomto článku jsou zahrnuty v licenci Creative Commons k článku, pokud není uvedeno jinak v kreditní hranici k materiálu. Pokud materiál není zahrnut v licenci Creative Commons článku a vaše zamýšlené použití není povoleno zákonnými předpisy nebo překračuje povolené použití, budete muset získat povolení přímo od držitele autorských práv. Chcete-li zobrazit kopii této licence, navštivte http://creativecommons.org/licenses/by/4.0/.
Tento článek je převzat z Clinical Reviews in Allergy & Immunology https://doi.org/10.1007/s12016-021-08905-x





