Mikroglie sítnice a mozku u roztroušené sklerózy a neurodegenerace, část 1
Aug 14, 2023
Abstraktní:
Mikroglie jsou rezidentní imunitní buňky centrálního nervového systému (CNS), včetně sítnice. Stejně jako mozkové mikroglie jsou retinální mikroglie zodpovědné za sledování sítnice a rychle reagují na změny prostředí změnou morfotypů a funkcí. Mikroglie se aktivují při zánětlivých reakcích u neurodegenerativních onemocnění, včetně roztroušené sklerózy (MS).
Náš mozek je komplexní orgán obsahující širokou škálu neuronů a nervových okruhů. Vzájemná propojení mezi těmito strukturami jsou klíčem k tomu, jak paměť funguje. Když se něco nového naučíme nebo něco nového zažijeme, mozek ukládá odpovídající informace do synapsí mezi neurony. Postupem času se postupně posilují spojení mezi synapsemi, což je dlouhodobá paměť.
Pokud je náš centrální nervový systém v nerovnováze, projeví se to na naší paměti. Nejčastějším příkladem je ztráta paměti u starších lidí. Tento stav je často způsoben odumíráním neuronů a oslabením spojení mezi neurony v důsledku stárnutí. Některá neurologická onemocnění mohou navíc zasahovat i do normální funkce mozku, a tím ovlivnit naši paměť. Tyto problémy ale nejsou nevratné a vědecké metody mohou pomoci zlepšit a chránit paměť.
Můžeme podpořit zdraví centrálního nervového systému a zlepšit paměť změnou našeho životního stylu. Mezi příklady patří pravidelná fyzická aktivita, dostatečný spánek, zdravá strava a cvičení mozku. Tato opatření nejen pomáhají udržovat fyzické zdraví, ale také podporují zdraví mozku a snižují ztrátu neurotransmiterů, čímž zlepšují paměť.
Celkově vzato existuje silné spojení mezi centrálním nervovým systémem a pamětí. Měli bychom věnovat pozornost našim životním návykům, aby náš mozek fungoval co nejzdravěji, a používat to jako základ pro udržení paměti. Je vidět, že potřebujeme zlepšit paměť. Cistanche může výrazně zlepšit paměť, protože masová pasta je tradiční čínský léčivý materiál s mnoha unikátními účinky, z nichž jedním je zlepšení paměti. Účinnost mletého masa vychází z různých účinných látek, které obsahuje, včetně karboxylové kyseliny, polysacharidů, flavonoidů atd. Tyto složky mohou různými kanály podporovat zdraví mozku.

Klikněte na možnost poznat krátkodobou paměť, jak se zlepšit
Když jsou retinální mikroglie aktivovány stresovými podněty, mění svou morfologii a aktivitu s prospěšnými nebo škodlivými důsledky. V tomto přehledu popisujeme charakteristiky mikroglií CNS, včetně mikroglií v sítnici, se zaměřením na jejich morfologii, aktivační stavy a funkci ve zdraví, stárnutí, RS a dalších neurodegenerativních onemocněních, jako je Alzheimerova choroba, Parkinsonova choroba, glaukom, a retinitis pigmentosa, aby se zvýraznila jejich aktivita ve stavu. Diskutujeme také protichůdná zjištění v literatuře a možné způsoby, jak v budoucnu snížit nekonzistence pomocí standardizované metodologie, např. automatizovaných algoritmů, abychom umožnili komplexnější pochopení této vzrušující oblasti výzkumu.
klíčová slova:
Sítnice; mikroglie; neurodegenerace; roztroušená skleróza; retinální mikroglie; morfotyp mikroglie.
1. Úvod
Mikroglie jsou rezidentní imunitní gliové buňky centrálního nervového systému (CNS). Dynamicky se posouvají do různých morfologií, které jsou také spojeny se specifickými aktivačními stavy, které mohou souviset s neuroprotektivními a/nebo neurotoxickými funkcemi v reakci na podněty, poranění nebo urážku [1–6]. Tyto morfologické a funkční změny jsou nezbytné pro podporu zdravého CNS tím, že přispívají k homeostáze [2,7,8]. Objevující se důkazy však začaly ukazovat účast mikroglií na onemocnění, přičemž mikrogliální dysfunkce může být způsobena onemocněním a/nebo způsobit rozšířené patologické stavy spojené s onemocněním [2].
Přesný stupeň zapojení a mechanismy, jak mohou mikroglie ovlivnit zdraví a onemocnění, však nejsou známy a v současné době se zkoumají. Účelem tohoto přehledu bylo shromáždit informace o charakteristikách mikroglií CNS, včetně mikroglií v sítnici, se zaměřením na jejich aktivační stavy, morfologii a funkci, o zdraví a nemoci. V první části jsme sestavili rozsáhlý popis hlavních znaků mikroglie v obecném CNS a sítnici.
Vysvětlujeme také některé mikrogliální změny, ke kterým dochází během normálního vývoje a procesu stárnutí. V další části diskutujeme současné chápání roztroušené sklerózy (RS) jako autoimunitního onemocnění, překvapivě časté oční projevy RS, mikroglie u RS a konečně mikroglie u jiných neurodegenerativních onemocnění. Nakonec poskytujeme pohled na to, proč mohou existovat protichůdná zjištění o charakteristikách CNS a retinálních mikroglií. Zde navrhujeme různé metody experimentování, jako je použití automatizovaných algoritmů ve světle přesvědčivějších a konzistentnějších výsledků.
2. Mikroglie
CNS se skládá z několika různých typů buněk, z nichž 5–10 % tvoří mikroglie, rezidentní imunitní buňky [9]. Původně se předpokládalo, že mikroglie existují jako klidové nebo „odpočinkové“ buňky, které nepřetržitě sledují své mikroprostředí a hledají jakékoli podněty nebo poškození, které mohou být škodlivé [5]. Naopak novější nálezy navrhly vysvětlení jejich dynamických vlastností. Mikroglie se mohou posunout do různých morfologických stavů, označovaných jako morfotypy. Každý morfotyp byl korelován s různými aktivačními stavy, které byly také spojeny s jedinečnými funkcemi potřebnými k zachování fyziologicky „normálního“ prostředí [5].
Jakmile jsou mikroglie aktivovány z jejich klidového stavu, mohou se dále diferencovat na dva hlavní fenotypy: M1 a M2 [6]. Ačkoli chybí pochopení specifických mechanismů, které indukují tuto diferenciaci, mikroglie M1 a M2 byly také spojovány s odlišnými cytokiny, chemokiny a trofickými faktory [6]. Prozánětlivé reakce jsou spojeny s „klasicky“ aktivovanými mikrogliemi M1, které podporují neurozánět jako odpověď na urážku nebo poranění, vytvářejí neurotoxické prostředí a odstraňují dysfunkční fragmenty buněčného odpadu [6]. K tomu může dojít v důsledku zánětlivých faktorů, jako je interleukin-1ß (IL-1ß), tumor nekrotizující faktor alfa (TNFalfa) a indukovatelná syntáza oxidu dusnatého (iNOS) [6,10] .
Naopak „alternativně“ aktivované mikroglie M2 jsou notoricky zodpovědné za protizánětlivé reakce, které podporují neuroprotektivní a regenerační procesy [6,10]. Nedávno byly nalezeny alespoň tři další subfenotypy typu M2 (M2a-c) [11], přičemž konkrétně typ M2a secernuje protizánětlivé faktory, jako je IL-10 a inzulín jako růstový faktor-1 (IGF-1), který podporuje odstraňování buněčného odpadu a neuroprotekci [6,11,12].
Uvádí se, že M2b je stimulován zánětlivými faktory, jako je IL-1ß a lipopolysacharidy (LPS), které mohou také zvýšit expresi IL-10 [11]. Bylo zjištěno, že tyto M2b mikroglie mají fagocytární vlastnosti v mozcích modelovaných pro Alzheimerovu chorobu (AD) a exprimují vysoké hladiny CD64 [11]. M2c „získává deaktivaci“ IL-10 nebo glukokortikoidy, což zase zvyšuje expresi růstových faktorů, jako je TGFß [11]. Navzdory těmto rozdílům je funkčně vyžadována aktivace M1 a M2, aby bylo zaručeno odstranění dysfunkčních buněk nebo škodlivých agregátů buněčného odpadu [6]. Mikroglie M1 se obvykle podílejí na odstraňování buněčných zbytků a tato zánětlivá odpověď musí být kontrolována mikroglií M2, aby se předešlo zbytečnému prodlužování zánětu [6].

Často u patologických procesů může být ovlivněna typická rovnováha polarizace M1 a M2 pozorovaná za normálních podmínek [6]. To může mít za následek odstranění zdravých buněk v důsledku nadměrného zánětu M1 a tlumící účinek M1 s M20 může být přemožen a způsobit další poškození [6]. K tomu často dochází u neurodegenerativních onemocnění, a proto byli navrženi někteří terapeutičtí kandidáti, kteří se zaměřují na polarizaci M1 a M2 [13]. Navzdory tomu se také objevují důkazy, které naznačují, že polarizace M1/M2 může být zastaralá. Poprvé byl představen a použit pro snadnější metody interpretace dat [14].
Nedávný technologický pokrok však odhalil překrývající se morfologické a genetické charakteristiky mezi typy M1/M2, což naznačuje potřebu přehodnotit typy mikroglií [14]. V nedávné době byly jako jedinečný typ mikroglie pozorovaný u onemocnění také rozpoznány mikroglie spojené s onemocněním (DAM) [14]. DAM se vyznačují mikrogliemi, které exprimují nízké hladiny superveillantních a homeostatických genů a vysoké hladiny markerů spojených s degenerací, jako jsou spouštěcí receptory exprimované na myeloidních buňkách 2 (TREM2) [14,15].
Pokud jde o morfologii, existuje asi pět hlavních mikrogliálních morfotypů, které byly rozpoznány, včetně rozvětveného, hyper-rozvětveného, aktivovaného, améboidního a tyčinkového typu. Za neprimovaných nebo "neaktivních" podmínek se mikroglie jeví jako "rozvětvené". Jsou rozmístěny rovnoměrně jako „mozaika“, přičemž každé se skládá z malého a kulatého buněčného těla, ke kterému je připojeno několik tenkých a dlouhých výběžků, které se neustále natahují a zatahují, aby usnadnily jejich kontrolní funkce (obrázek 1) [2,5,16] .
Experimentální in vivo zobrazování mozku ukázalo, že tyto dynamické procesy se dostávají do blízkosti neuronů, glií a krevních cév, což naznačuje, že mikroglie aktivně spolupracují s ostatními částmi kůry, aby udržely fyziologicky normální prostředí CNS [17]. Někdy mohou rozvětvené mikroglie rozpoznat změny v mikroprostředí a reagovat změnou na „hyper-rozvětvené“ mikroglie typicky definované hojnějšími procesy, které jsou delší a tlustší, připojené k větším, lobulárním a nepravidelně tvarovaným buněčným tělům (obrázek 1) [16,18] ]. Většina typů primovaných „nerozvětvených“ mikroglií, včetně hyper-rozvětvených buněk, je rozptýlena v CNS v nepravidelné a „shlukované“ distribuci [2].
Hyper-rozvětvené mikroglie se mohou také posunout do aktivované formy po vystavení výrazně škodlivým stimulům, které mají také podobná buněčná těla jako hyper-rozvětvené buňky, zatímco mají mnohem méně procesů, které jsou tlustší a kratší (obrázek 1) [2,16,19]. . Když jsou škodlivé podněty značně prodlouženy, aktivovaná mikroglie se může přeměnit do „améboidního“ stavu s kulatější, větší a pravidelněji tvarovanou buňkou a velmi malým počtem nebo žádnými procesy (obrázek 1) [16,18]. Nedávno znovu objevený morfotyp je „tyčová“ mikroglie charakterizovaná dlouhým buněčným tělem ve tvaru klobásy s několika procesy, které nemusí vždy přesahovat délku rozvětvené mikroglie (obrázek 1) [20,21].
Ačkoli nové důkazy ukázaly, že tyčinkové mikroglie se lokalizují v blízkosti neuronů a zarovnají se podél nervových vláken, jejich přesná funkce je stále ještě třeba objevit [20–23]. Konečným typem je améboidní mikroglie, často označovaná jako fagocytární typ, který se přesouvá na místo poškození a fagocytuje mrtvé nebo odumírající neurony a buněčné zbytky (obrázek 1) [5,24]. Nedávno se objevující důkazy vedly k teorii, že hyper-rozvětvené, aktivované a tyčinkové morfotypy mohou být „přechodné“ formy, které existují mezi rozvětveným a améboidním stavem [5,25].

2.1. Retinální mikroglie
Sítnice je nezbytnou součástí CNS. Vzhledem k její průhlednosti pro světlo je možné k vizualizaci sítnice použít méně invazivní zobrazovací modality s vysokým rozlišením [26,27]. Je známá především svou účastí na přeměně světelné energie na elektrické signály [28]. U lidí se sítnice vyvíjí od prvního měsíce embryologicky do konce prvního roku a pochází z neuroektodermu [28,29]. Sítnice se skládá z několika odlišných vrstev, přičemž nejvnitřnější vrstvou je vrstva nervových vláken sítnice (RNFL), dále vrstva gangliových buněk (GCL), vnitřní plexiformní vrstva (IPL), vnitřní jaderná vrstva (INL), vnější plexiformní vrstva (OPL), vnější jaderná vrstva (ONL) a konečná vrstva retinálního pigmentového epitelu (RPE) (obrázek 2) (29) V těchto vrstvách existuje několik typů buněk, včetně amakrinních buněk, Mullerových buněk, astrocytů, horizontálních buněk , tyčinkové a čípkové fotoreceptory a bipolární buňky, z nichž všechny lze nalézt také ve zbytku CNS [29].
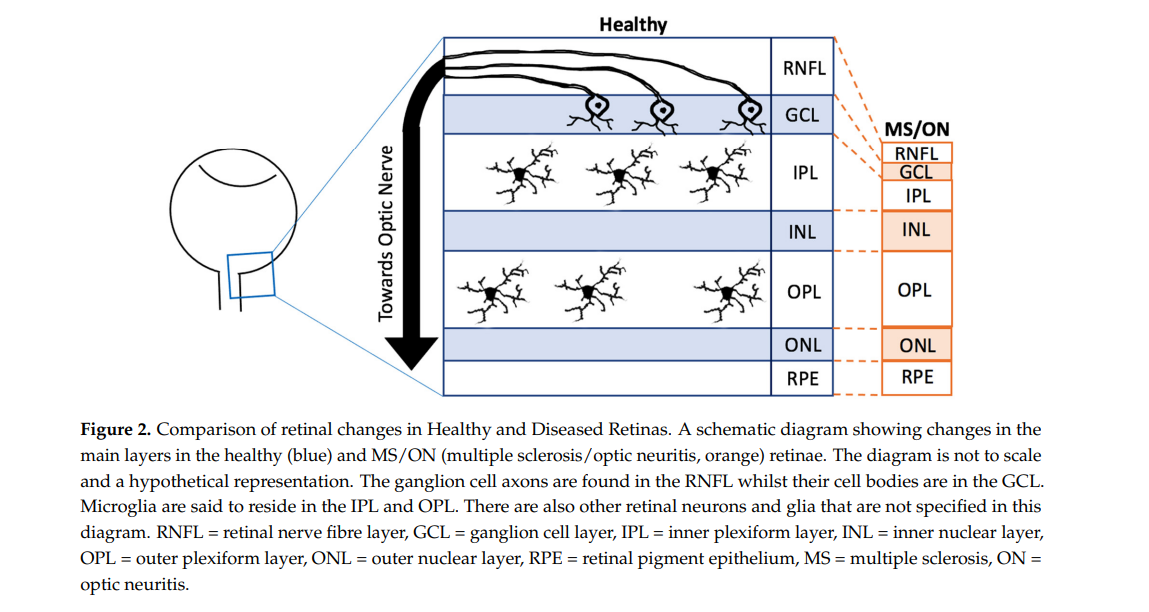
Přibližně 0,2 % z celkového počtu buněk sítnice jsou tvořeny mikrogliemi, z nichž 50 % obvykle sídlí v IPL, zatímco zbytek se nachází v OPL (obrázek 2) [2]. Prostřednictvím vývoje a homeostázy se mikroglie dynamicky pohybují různými vrstvami sítnice, i když se vyhýbají ONL [2]. Kromě toho mnoho modelů onemocnění sítnice a poranění sítnice ukázalo, že mikroglie mohou migrovat směrem k oblasti degenerace, aktivovat se a proliferovat [30,31], jak bude podrobněji popsáno později. Přestože se z primitivního žloutkového vaku vyvinuly jak retinální, tak mozkové mikroglie, vzhled každého morfotypu se může lišit v závislosti na oblasti CNS [10].
Například mikroglie ve striatu, hippocampu a frontálním kortexu mají větší buněčná těla s více procesy ve srovnání s těmi v mozečku [32]. Navíc existují důkazy, že různé vrstvy mozkové kůry obsahují mikroglie různých velikostí [32]. Vzhled morfotypu se také může lišit v závislosti na použitých metodách nebo osách disekce. Například rozvětvené mikroglie se mohou jevit jako horizontálně rozvětvené, což se při pozorování v příčném řezu jeví jako jedna vodorovně dlouhá buňka, zatímco při pozorování z celé hory se jeví jako a jako dříve zmíněný standardní morfologický popis rozvětvených mikroglií [2,33 ].
Když jsou mikroglie primovány a stávají se hyper-rozvětvenými, jejich procesy se rozšiřují radiálně a zasahují přes různé vrstvy, což je lépe zobrazitelné v řezu v řezu ve srovnání s pozorováním na celé montáži [2,33]. Navzdory těmto rozdílům bylo zjištěno, že retinální a mozkové mikroglie sdílejí expresi několika transkripčních faktorů [2]. Četné studie také dokázaly pozorovat každý morfotyp jak v mozku, tak na sítnici [2,4,5,22,33,34]. Stále však není jasné, zda každý morfotyp v obou oblastech CNS sdílí stejné rysy [2].
2.2. Molekulární markery a stimuly ovlivňující mikrogliální morfologii
Podobně jako v mozku mohou jednotlivé morfotypy mikroglií v sítnici vyplývat z mikrogliálních odpovědí na různé cytokiny, chemokiny nebo molekulární vzorce spojené s poškozením přítomné v jeho mikroprostředí, což naznačuje heterogenitu v mikrogliální genetické expresi [9]. Například se uvádí, že rozvětvené mikroglie mají vysokou expresi P2RY12, která je často spojena s funkcemi dozoru, zatímco u améboidních mikroglií bylo zjištěno, že exprimují vysoké hladiny CD68 – notoricky známého markeru fagocytózy [35,36].
Rozdílné úrovně exprese mikrogliálních iontových kanálů a povrchových receptorů mohou také interagovat s takovými molekulami (např. cytokiny) v mikrogliálním mikroprostředí, což vede k mikrogliálním změnám včetně hustoty, prostorové distribuce, aktivačního stavu a morfotypu a patogeneze onemocnění [9,37]. Například transformující růstový faktor beta (TGFß) je důležitý mikrogliální cytokin, pleiotropně zapojený do fyziologického vývoje retinálních neuronů a cév [37]. Ma et al. pozorovali pouze-1 pozitivní mikroglie z celých sítnic tamoxifenem indukované ablace TGFßR2 (TGFß receptor) u 2-měsíčních myší Cx3cr1CreER/+, Tgfbr2flox/flox [37 ].
Mikrogliální morfologie se zdála rozvětvená 1 den po ablaci TGFßR2 (PTA), která se pak po 2–5 dnech PTA méně rozvětvovala „zatuhlými“ procesy a nakonec se objevila zdlouhavými procesy, které byly zarovnány podél retinálních krevních cév za 3–10 týdnů. PTA [37]. Analýza retinálních mikroglií s ablací TGFßR2 v reálném čase (RT-PCR) odhalila sníženou expresi růstových faktorů (např. BDNF, PDGFA) a zvýšenou expresi markerů zánětlivé aktivace (např. MHCII, CD68). U zdravých mikroglií to nebylo pozorovatelné.
Kromě toho, zatímco zvířata s ablací TGFßR2 nevykazovala žádné účinky na vaskulaturu sítnice, došlo u nich k ztenčení sítnice a zvýšené míře patologické choroidální neovaskularizace v reakci na poranění [37].

2.3. Extracelulární vezikuly: Účinky na mikroglie
Retinální (a mozková) mikroglie také vylučují extracelulární vezikuly (EV), což jsou membránově vázané částice složené z mRNA, miRNA, DNA, cytokinů, lipidů a proteinů, považované za biopsii původní buňky [6,38,39]. . EV se podílejí na komunikaci mezi buňkami tím, že transportují své neuroprotektivní/toxické složky v reakci na intracelulární a extracelulární podněty, když se pohybují krevním řečištěm a mozkomíšním mokem (CSF), aby dosáhly dalších buněk v blízké i vzdálené blízkosti [6, 38,39].
EVs include exosomes and exosomes, which consist of apoptotic bodies and microvesicles [39]. Firstly, many endosomal vesicular bodies fuse to form exosomes (40–160 nm in size) which are then released for intercellular communication [39]. Secondly, microvesicles instead originate from the plasma membrane undergoing outward budding (100–1000 nm) [38]. Finally, apoptotic bodies are >1000 nm ve velikosti a formě prostřednictvím membránových bublin dezintegrujících, např. retinálních mikroglií [38]. Složky apoptotických tělísek, jako je fosfatidyl serin, modulují mikrogliální fagocytózu [38,39]. V důsledku těchto různých vlastností se mikrogliální EV nedávno začaly zkoumat pro neurodegenerativní onemocnění.
2.4. Mikroglie a stárnutí
Mikrogliální buňky v sítnici novorozených a postnatálních potkanů mají kulatou nebo améboidní formu a vykazují pseudopodální procesy zapojené do fagocytózy buněčného odpadu a vývojové remodelace synapse [2]. Jak se druhý a třetí týden postnatálního období blíží, těla mikrogliových buněk se postupně zmenšují s jemnými větvemi [2], za předpokladu vysoce rozvětveného fenotypu s pokrokem ve vývoji mozku [40]. Tato progrese se také odráží v oblastech mozku, včetně cerebellum, což naznačuje, že mikroglie jsou aktivně zapojeny prostřednictvím zrání CNS.
Studie zkoumala charakteristiky kortikálních mikroglií u starých dospělých (24 měsíců) a mladých dospělých myší (6 měsíců), aby nalezla sníženou hustotu mikroglií a nepravidelně distribuované shluky [41]. Studie retinálních mikroglií však odhalily některé protichůdné výsledky.
Nejprve byly zkoumány podobné věkové skupiny myší jako v předchozí studii (18–24 měsíců vs. 3–4 měsíce), aby se zjistilo, že starší dospělí měli významně zvýšenou hustotu retinálních mikroglií ve srovnání s mladšími dospělými myšmi [42]. To naznačuje, že mikrogliální reakce na stárnutí mohou být regionálně specifické. Další inspekce zobrazování sítnice v reálném čase ukázala, že většina starých dospělých mikroglií má méně a kratších procesů, což naznačuje aktivované nebo améboidní mikroglie, než ty u mladých myší [42].
Bylo zjištěno, že jsou uspořádány v mozaikovém rozložení. Novější studie se zabývala morfologickými rozdíly a rozdíly v expresi markerů celoplošných retinálních mikroglií u starých (15 měsíců) a mladých (věk neuveden) myší [43]. Na rozdíl od výsledků Damaniho et al. tato studie nezjistila žádné významné rozdíly v hustotě pouze-1 pozitivních buněk retinální mikroglie a ploše pokryté procesy mezi těmito dvěma věkovými skupinami, zatímco oblast buněčného soma v OPL, IPL, NFL a GCL a počet vertikálních procesů se významně zvýšil [42,43].
Kromě toho mladé mikroglie většinou exprimovaly P2RY12 a žádný CD68, zatímco staré mikroglie byly CD68+ a vypadaly jako améboidní [43]. Tyto výsledky místo toho naznačují, že se stárnutím mohou mikroglie posunout svou morfologii a genetický profil, aby se přizpůsobily procesu stárnutí [43]. FernándezAlbarral et al. však neuvádějí přesný věk, druhy myší ani použité metody kvantifikace. Takové rozdíly mezi studiemi mohou ovlivnit výsledky.
Starší mikroglie se stávají méně dynamickými a vykazují výrazně pomalejší motilitu procesů ve srovnání s těmi u jejich mladších protějšků, což pravděpodobně ohrožuje jejich schopnost nepřetržitě zkoumat a interagovat s prostředím [42]. Postmortální hipokampální a kortikální vyšetření u dospělých „mladých“, „středních“ nebo „starých“ (20–69 vs. 70+ vs. 90+ let) dospělých odhalilo více regionálně specifických mikrogliálních odpovědí na stárnutí [4]. Bylo zjištěno, že tyčinkovité mikroglie jsou výrazně četnější u „uprostřed“ ve srovnání s „mladými“ dospělými, ačkoli to bylo pozorováno pouze v hipokampu, zatímco „staří“ dospělí měli významné zvýšení tyčinek pouze v hippocampu [4]. Jiné kortikální a hipokampální studie nalezly podobné mikrogliální trendy s věkem, což naznačuje, že stárnoucí mikroglie mohou mít snížené schopnosti dozoru potřebné pro udržení zdravého CNS, což zase může zvýšit riziko rozvoje neurodegenerativních onemocnění [44–46].
Myelinizované axony neuronů jsou základním znakem CNS, který umožňuje účinnou vodivost akčního potenciálu [47]. Zatímco myelin je produkován mnoha buňkami oligodendrocytů, prochází neustálou obnovou, přičemž myelinové zbytky jsou přímo odstraňovány a nepřímo nahrazeny mikrogliemi [47,48]. Bylo však navrženo, že změny v tvorbě myelinových trosek se stárnutím mohou také vést k dysfunkci imunitních buněk CNS, jako jsou mikroglie, související s věkem [49]. S věkem je tedy více narušených molekul spojených s myelinem a je vyžadována vyšší rychlost obratu myelinového proteinu [49].
To vede ke zvýšené rychlosti rozpadu myelinu, což způsobuje zatěžující akumulaci myelinu, který pak tvoří nerozpustné lysozomální agregáty v mikrogliových buňkách [49]. TREM2 je exprimován na mikrogliálních buněčných povrchových membránách; jeho nedostatek nebo mutace však může vyústit v onemocnění způsobené nadměrnou demyelinizací [50]. Poliani a kol. zjistili, že „staré“ mozky s deficitem TREM2 měly demyelinizaci s dystrofickými a améboidně vyhlížejícími mikrogliemi [50]. Také se říká, že TREM2-pozitivní améboidní mikroglie se pak mohou transformovat do různých tvarů, když začnou produkovat faktory jako TNF a IL-1, které jsou považovány za „proregenerační“ faktory [48 ].
Extracelulární matrice je tedy modifikována tak, aby spustila modifikaci extracelulární matrice, aby přitahovala a aktivovala oligodendrocytové prekurzorové buňky (OPC), které pak remyelinizují axon [48]. Dále bylo zjištěno, že zdravé mikrogliální odpovědi na demyelinizaci zvyšují expresi genů spojených s aktivací, fagocytózou a metabolismem lipidů, zatímco u TREM2 deficitních mikroglií tomu tak není [50]. Jiné studie ukázaly, že i když je odstraňování trosek mikrogliální fagocytózou významnější se zvyšujícím se věkem, fagocytóza „mladších“ myelinu byla výkonnější než u „staršího“ myelinu [51]. Tyto změny související s věkem také korelovaly s častějším výskytem „dystrofických“ nerozvětvených mikroglií [51]. Dosud není mnoho výzkumů myelinových úlomků související s retinální mikrogliální fagocytózou, pravděpodobně kvůli nedostatku myelinu v samotné sítnici.
Se stárnutím se mikrogliální populace stávají dystrofickými a podléhají strukturálním a morfologickým změnám. Cytoplazma se začíná fragmentovat a jejich buněčné procesy postupně ztrácejí jemné větvení a vykazují sféroidní otoky [52]. Navíc jejich konstitutivní mikrogliální funkce začíná klesat a vykazuje abnormální reakce na poškození mikroglií. Tyto změny v kombinaci se změnami stárnutí molekulární a genové exprese v mikrogliích mají za následek jejich sníženou schopnost udržovat homeostázu v imunitním prostředí, což může přispívat k neuronálním poruchám, kognitivnímu poklesu a onemocněním souvisejícím s věkem [5,27,53– 55].
2.5. Genetické faktory: Účinky na stárnoucí mikroglie
Věk je dobře známým rizikovým faktorem neurodegenerativních onemocnění [56–58]. Proto se změna genové exprese ve stárnoucí sítnici stala významným předmětem zájmu. Například Chen a kol. zkoumali celkovou retinální RNA 3-měsíců a 20-měsíců starých myší C57BL/6 [57]. S přibývajícím věkem bylo 298 genů, včetně genů souvisejících se stresovou reakcí a syntézou glykoproteinů, upregulováno více než dvojnásobně, zatímco 137 genů, včetně genů souvisejících s imunitními a obrannými reakcemi, bylo také více než dvojnásobně sníženo [57]. ].
Kromě toho analýzy RT-PCR ukázaly zvýšení zánětlivých genů spojených s aktivací cytokinů, chemokinů nebo komplementu, např. chemokinový (CC motiv) ligand 2 (CCL2), CCL12 nebo komplementová složka 3 (C3) [57]. Autoři poté předpokládali, že by to mohlo odrážet mikrogliální aktivaci, což bylo podpořeno imunohistologickým pozorováním améboidních mikroglií isolectinu B4+ v IPL pouze u starých myší [57]. Další studie dokázala konkrétně prozkoumat transkripční změny ve stárnoucích retinálních mikrogliích porovnáním RNA extrahované z izolovaných retinálních mikroglií 3-, 12-, 18- a 24-měsíc- staré myši C57BL/6 [58].
Bylo identifikováno celkem 719 odlišně exprimovaných genů, které byly funkčně spojeny s mikrogliální imunitní regulací, např. IL3 a IL7, angiogenezí, např. vaskulárními endoteliálními růstovými faktory, a trofickými růstovými faktory, např. neurotrofinem [58]. Je zajímavé, že podobně jako Chen et al. se exprese C3, genu spojeného s věkem podmíněnou makulární degenerací (AMD), zvyšovala s věkem, což naznačuje, že transkripční změny retinální mikroglie související se stárnutím mohou přispívat k patogenezi AMD [58].
3. Roztroušená skleróza
3.1. Roztroušená skleróza
Roztroušená skleróza (RS) je chronické zánětlivé onemocnění CNS postihující přibližně 100000 pacientů ve Spojeném království a 2500000 pacientů na celém světě [59]. Je zajímavé, že může postihnout až třikrát více žen než mužů, s průměrným věkem nástupu v rané dospělosti [60]. Zatímco první záznamy o patofyziologických rysech souvisejících s RS pocházejí z roku 1838, jejich patologické a klinické projevy byly poprvé identifikovány jako „RS“ v roce 1863 Jean-Martinem Charcotem [61].
Od té doby byly odhaleny složité patologie RS. Často se vyskytující příznaky RS zahrnují oční dráhu, jako je ztenčení RNFL, optická neuritida (ON) charakterizovaná zánětlivým poškozením zrakového nervu a uveitida charakterizovaná nitroočním zánětem sklivce, sítnice a uveálního traktu [62–66]. Bylo také popsáno, že k takovým změnám sítnice může dojít před změnami ve zbytku CNS u mnoha neurodegenerativních onemocnění, včetně RS [26].
Tyto nedávné poznatky vedly k velkému zájmu o výzkum sítnice. Navzdory komplexním procesům, které se účastní rozvoje RS, jde o onemocnění definované autoimunitními odpověďmi prostřednictvím aktivace imunitních buněk, jako jsou T-lymfocyty, B-lymfocyty, mikrogliové buňky a makrofágy, demyelinizace, remyelinizace a neurodegenerace [12,67–69].
Dobře uznávaná hypotéza RS je, že se vyvíjí ve dvou hlavních fázích. Za prvé, T-buňky a B-buňky zprostředkovávají zánětlivé reakce uvolňováním cytokinů, které indukují aktivaci zánětlivých buněk, jako jsou mikroglie, za „uzavřenou“ hematoencefalickou bariérou (BBB) [68,70–72]. Chronický zánět pak může vyústit v mitochondriální dysfunkci, způsobující nedostatek energie. Za druhé, neuroprotektivní signály jsou potlačeny, což zhoršuje schopnost opravit demyelinizaci, poškozené axony a neurodegeneraci [68,70]. V důsledku toho dochází k významným blokádám axonální vodivosti, přičemž nakonec u pacienta zůstanou ireverzibilní léze CNS, jako je BBB, což způsobí, že se stane „propustným“ [68]. Toto však zůstává teorií kvůli nedávným objevům, které ukazují, že někteří pacienti reagují lépe na terapeutika, která cílí na B-buňky, než na ty, která cílí na T-buňky [70]. Přestože bylo provedeno několik výzkumů využívajících stále se vyvíjející metody, neexistuje konsenzus kvůli protichůdným vědeckým výsledkům [73].

3.2. Podtypy roztroušené sklerózy
Existuje spektrum závažnosti symptomů a rychlosti progrese, což odráží heterogenitu RS [70]. Nejčasnější projevy pacientů s RS lze rozpoznat jako klinicky izolovaný syndrom (CIS) [67]. Pacienti s CIS mají monofázické a monofokální symptomatické epizody, prožívající např. ataxii, fotofobii nebo areflexii, která trvá 24 hodin po 3 týdnech [67]. Primárně progresivní RS (PPMS) postihuje přibližně 15 % pacientů s RS, u kterých obvykle dochází k trvalému a progresivnímu poklesu zdraví [74]. Progresivní relabující RS (PRMS) je nejméně častou formou RS, která postihuje pouze přibližně 5 % pacientů, u nichž dochází k trvalému zhoršování zdravotního stavu s neočekávanými skoky zhoršení a zotavení [74]. Relaps-remitující RS (RRMS) je častější formou, která postihuje 80–90 % pacientů, u nichž dojde k nepředvídanému nárůstu invalidity [70].
Obvykle jsou tyto nárůsty následovány úplnými zotaveními, ale jak pacienti stárnou a postupují do pozdějších stadií, tato zotavení se stávají více částečnými [70,74]. To může být odůvodněno tím, že u mnoha pacientů s RRMS se rozvine sekundárně progresivní RS (SPMS), kdy pacienti mohou zaznamenat méně vrcholů poškození a začít napodobovat trajektorii onemocnění PPMS [70,74]. V poslední době širší zájem o genetické studie umožnil rozpoznání alel a genových variant specifických pro MS, zejména prostřednictvím celogenomové asociační studie [70,75]. Velké množství dat umožnilo sofistikovanější analýzy, které odhalily, že specifické genové varianty korelovaly s různými typy RS [76]. Tyto genové varianty byly nalezeny převážně fyzicky a funkčně blízko imunomodulačních genů asociovaných s patogenezí RS [70,75].
Navzdory tomu jsou profily těchto podtypů pouze popisné, protože chybí dostatečné důkazy pro přesné patofyziologické rozlišení [77]. Velká část pacientů s RS například zažívá asymptomatické fáze, kdy se léze spojené s RS a další patofyziologické změny mohou objevit tiše [78]. Některé postmortální studie mozku dokonce ukázaly, že u jedinců, kteří byli během svého života považováni za „zdravé“, byly pozorovány výrazné patologické stavy spojené s RS [78]. V poslední době se proto vyvinuly odkazy na tyto podtypy, které rozlišují mezi aktivitou onemocnění nebo žádnou aktivitou onemocnění s podrobnostmi o „nárůstech“ nebo stabilní progresi a pozorování nových lézí CNS [77].
For more information:1950477648nn@gmail.com
