Nové perspektivy pro Fisetin, část 1
May 26, 2022
Prosím kontaktujteoscar.xiao@wecistanche.comPro více informací
Fisetin je flavonol, který sdílí výrazné antioxidační vlastnosti s množstvím jiných rostlinných polyfenolů.flavonoidyNavíc vykazují specifickou biologickou aktivitu značného zájmu, pokud jde o ochranu funkčních makromolekul proti stresu, což vede k udržení cytoprotekce normálních buněk. Navíc vykazuje potenciál jako protizánětlivé, chemopreventivní, chemoterapeutikum a nově i chemoterapeutikum. Vzhledem k jeho perspektivním aplikacím ve zdravotnictví a pravděpodobné poptávce po fisetinu jsou zde diskutovány způsoby jeho přípravy a jejich vhodnost pro farmaceutické použití.
klíčová slova:fisetin, flavon-3-oly, syntéza flflavonolů, biologická aktivita flflavonolů, protirakovinné, proti stárnutí
ÚVOD
První záznam o fisetinu jako izolátu ze škumpy benátské (Rhus Cotinus L.) pochází z roku 1833. Základní chemické vlastnosti sloučeniny poskytl o několik desetiletí později Schmidt (1886), přičemž její struktura byla objasněna a nakonec potvrzena syntézou. S. Kostanecki, který v 90. letech 19. století zahájil masivní výzkum žlutých rostlinných pigmentů a vytvořil nové názvy skupin pro jejich podkategorie, v současnosti známé jako „flavony“, chromony, „chalkony“ atd. (Kostanecki a kol., 1904). Flavonol fisetin (č. CAS [528-48-3]), běžně popisovaný jako:2-(3,4-dihydroxyfenyl)-3,7-dihydroxy{{ 11}}H-1-benzopyran-4-on;3,3',4',7-tetrahydroxy flavon; nebo 5-deoxykvercetin, reprezentovaný strukturním vzorcem 1, byl dosud identifikován jako sekundární metabolit mnoha rostlin, vyskytující se v jejich zelených částech, plodech, stejně jako v kůře a tvrdém dřevě (Panche et al. , 2016; Hostetler a kol., 2017; Verma, 2017; Wang a kol., 2018). Byl to Roux, kdo v sérii pečlivých studií provedených před příchodem moderních spektrálních nástrojů strukturní analýzy vysvětlil původ a stereochemii oligomerních taninů, které obsahují flavon{24}}olické struktury úzce související s fustinem, fisetidinolem, fisetinem, a podobné struktury přítomné v různých afrických stromech (Roux a Paulus, 1961, 1962; Roux a kol., 1961; Drewes a Roux, 1965) (obrázek 1).používá hesperidinI když si kondenzované taniny používané v kožedělném průmyslu zachovaly část svého technického významu, dnes je více pozornosti věnováno přítomnosti fisetinu v rostlinných složkách lidské stravy a jejich roli jako důležitých epigenetických faktorů při modulaci stavu lidského zdraví. Fisetin je přítomen v jahodách. jablka, tomel, hroznové víno, cibule, kiwi, kapusta atd., byť v nízké koncentraci, až stovky mikrogramů na 1 gram čerstvé biomasy. Důvod tohoto zájmu pramení z relativně nedávných pozorování, že sloučenina 1 je nejen zvláště účinná jako antioxidační činidlo, ale také vykazuje pozoruhodnou selektivitu, pokud jde o ovlivnění mnoha biologických procesů považovaných za klíčové pro biologickou homeostázu.

Tato zjištění přirozeně vyvolávají některé otázky týkající se obecné dostupnosti fisetinu.používá hesperidinPřírodní látka vysoké chemické čistoty – vysoce tající žluté jehlice, rozpustná v polárních organických rozpouštědlech a prakticky nerozpustná ve vodě – byla dosud k dispozici pro výzkumné účely jako izolát z rostlin a jako biochemické činidlo, které se již stalo důležitá molekulární sonda v lidské fyziologii. Otázka dostupnosti fisetinu přirozeně vyvstává s nárůstem počtu farmakologických studií.ztracená říše cistanchePři přípravě dokumentu CTD (Common Technical Document), který je nezbytný před schválením látky pro klinické zkoušky, je nutné zajistit jednotnou kvalitu zkoumané účinné látky. Tato otázka je dále diskutována podrobněji.

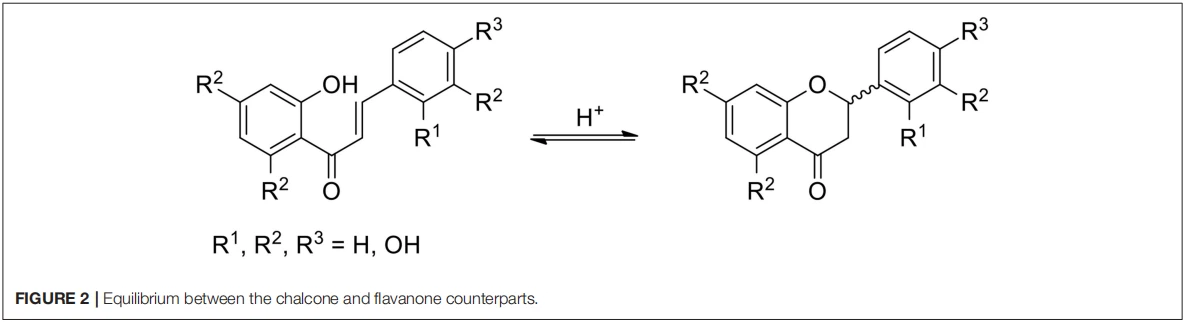
Téměř všechny přírodní fenylpropanoidy mají tendenci se vyskytovat v glykosylovaných formách, ale glykosidy 1 jsou zřídka zmíněny ve fytochemické literatuře, na rozdíl od cukerných derivátů jejich analogů uvedených na obrázku 1. Sloučeniny 2-8 jsou blízce příbuzné fisetinu: během biogeneze rostlin chalkony a jejich izomerní flavanony podléhají dvěma různým druhům hydroxylací (aromatické v kruhu B 4 a alicyklické v kruhu Cof 6), obě prováděné enzymy typu CYP450. Nakonec je flavanol-3-na-4(8) oxidován, přičemž ztrácí obě centra chirality a poskytuje 1.mikronizovaná purifikovaná flavonoidní frakce 1000 mg používáVývoj proteinového záhybu pro chalkonsyntázu (CHS, EC2.3.1.74; a její izomeráza CHI, EC5.5.1.6) představoval velký evoluční úspěch, který rostlinám umožnil zvládnout stereoselektivní syntézu fenylpropanoidů a dosáhnout mnoha nových funkcí jako pokud jde o signalizaci, obranu a alelopatii (Austin a Noel, 2003; Dao et al., 2011; Ngaki et al., 2012; Yin et al., 2018). V abiotickém světě chemické syntézy však může být poloha izomerní rovnováhy mezi chalkony a jejich racemickými flavanonovými protějšky řízena pouhou změnou hodnoty pH (Obrázek 2) (Pramod et al, 2012; Bhattacharyya a Hatua, 2014 ; Masesane, 2015). Interakce dietárního rostlinného metabolomu s lidskou fyziologií tedy může vyžadovat zvláštní péči při interpretaci nutričních jevů, tradičně založených na vybraných markerových sloučeninách.
CHEMICKÝ ZÁKLAD PRO SELEKTIVNÍ BIOLOGICKOU AKTIVITU FISETINU
Existovalo množství experimentálních důkazů na podporu jednoduchého zobecnění, že prakticky všechny rostlinné fenolické látky vykazují výrazné antioxidační vlastnosti (Halliwell, 2006; Galleano et al, 2010; Prior a Wu, 2013). Velmi složitá chemie jednoduchých fenolických látek, zahrnující reaktivitu volných radikálů, iontových radikálů a organických iontových struktur vzniklých přenosem protonů, se do značné míry odráží v jejich biologické aktivitě a farmakologii (Cicerale et al, 2008; Pereira et al, 2009 Baruah, 201l; Adeboye a kol., 2014). Polyfenolické struktury rozšířené inkluzí katecholového kruhu jsou zvláště

náchylné ke specifické delokalizaci aromatických elektronů, která může v důsledku kontaktu s akceptory vodíku zahrnovat chinonové a vicinální diketonové struktury, jak je doloženo pro 1 na obrázku 3 (Awad et al., 2001). Takové meziprodukty jsou zjevně méně náchylné k oligomerizaci flavonoidů, ale mohou být aktivní jako akceptory řady buněčných nukleofilů.
BUNĚČNÁ SENESCENCE A FISETIN
Téměř před šesti desetiletími byl objeven fenomén omezené proliferační kapacity lidských fibroblastů (Hayflick, 1965, 1974), což zahájilo období rozsáhlých studií mechanismů zastavení růstu buněk, zejména v souvislosti s příčinami procesu stárnutí. Podle nedávných zjištění se zdá, že buněčné stárnutí, které je v podstatě trvalé, hraje odlišné role jak v normální fyziologii, tak v různých patologiích. Senescentní buněčné fenotypy, které normálně vylučují zánětlivé proteiny (SASP) a směřují k apoptóze, mohou podstoupit určité způsoby farmakologicky indukované intervence vedoucí ke zvratu buněčného osudu (Kuilman et al, 2010, str. 92). Senescence a kancerogeneze (onkogeneze) v podstatě nasměrují buněčný osud opačným směrem, což má zásadní význam, pokud jde o pochopení mechanismů chemoterapie, během níž může být výsledkem indukované senescence regrese nádoru (Campisi, 2013; van Deursen, 2014; Mendelsohn a kol., 2015). Navzdory skutečnosti, že senescentní buňky mohou také podléhat podpoře a progresi rakoviny, zůstane vliv farmakologických činidel na oba reverzní procesy důležitou oblastí výzkumu po dlouhou dobu. V současnosti obojí: myšlenka senescence vyvolávající stimuly za různých stresových podmínek a schopnost působit proti a/nebo zvrátit sekreční fenotyp spojený se stárnutím jsou silně propojeny. To je založeno na teoriích stárnutí, které poukazují na škodlivé účinky reaktivních forem kyslíku (ROS), buď mitochondriálního původu, nebo generované vlivem životního prostředí (Gil del Valle, 201l, s. 102; Liochev, 2013). Zatímco pojem přírodních produktů, zejména těch, které jsou přijímány s potravou, jako ochránců před ROS, je již dobře zaveden na buněčné úrovni, zdá se příliš obecný na to, abychom podrobně vysvětlili konkrétní selektivní aktivity velkého množství rostlinných sekundárních metabolitů, pro něž jsou tvrzení o příznivé léčivé účinky již byly formulovány.oteflavonoidKromě antibiotické aktivity (Manjolin et al., 2013; Borsari et al., 2016) sdílí fisetin výraznou antioxidační aktivitu s mnoha dalšími polyfenolickými sloučeninami, což bylo potvrzeno


různými modely in vitro i in vivo (Khan et al., 2013; Lall et al., 2016; Jiang et al., 2018; Kashyap et al., 2018). Kromě toho jsou antioxidační účinky 1 a zejména indukce syntézy glutathionu považovány za důležité, pokud jde o neuroprotekci. Velká pozornost byla také věnována protirakovinné aktivitě 1. Byly provedeny studie in vitro, které nabízejí panoramatický pohled na selektivitu cílových orgánů a také přehled makromolekulárních cílů. Posledně jmenované zahrnují: AMP-aktivovaná proteinkináza (AMPK); cyklooxygenáza (COX); receptor epidermálního růstového faktoru (EGFR); extracelulární signálem regulovaná kináza (ERKI1/2); matrix metaloproteináza (MMP);nukleární faktor-kappa B(NF-kB); prostatický specifický antigen (PSA) transkripční faktor T-buněčný faktor (TCF); ligand indukující apoptózu související s TNF (TRAIL); Wnt inhibiční faktor (WIF-1); X-vázaný inhibitor apoptózy (XIAP), mimo jiné (Lall et al., 2016; Hostetler et al., 2017; Kashyap et al., 2018; Wang et al., 2018). Protirakovinnou aktivitu fisetinu lze zvýšit některými pomocnými látkami. Například fisetin významně narušuje růst rakovinných buněk v přítomnosti kyseliny askorbové, což vede k 61% inhibici buněčného růstu za 72 hodin; léčba samotnou kyselinou askorbovou neměla žádný účinek na buněčnou proliferaci (Kandaswami et al, 1993). Bylo také prokázáno, že flavonoly typu fisetin extrahované z Allium Vegetables mohou hrát roli takové pomocné látky v kombinaci s dobře definovanými

protirakovinná léčiva a zvyšují antiproliferativní aktivitu cis-diammindichloroplatiny(II), dusíkatého yperitu a busulfanu v kultivačních systémech lidských nádorových buněk. Analýza chemického složení flavonolových extraktů z různých druhů Allium Vegetables a jejich účinků na neoplastickou transformaci buněk NIH/3T3 již byla prezentována (Leighton et al., 1992).
Mezi další aktivity v tomto směru patří zlepšení dlouhodobé paměti, antidepresivní účinky, inhibice ischemicko-reperfuzního poškození a zlepšení behaviorálních deficitů po mrtvici (Khan et al., 2013; Maher, 2015; Currais et al., 2018 Kashyap a kol., 2018).
Snad nejslibnější z dokumentovaných biologických aktivit fisetinu spočívá v předpokládané možnosti zacílení na základní mechanismy stárnutí. Ačkoli senescentní buňky odolávají apoptóze prostřednictvím upregulace antiapoptotických drah senescentních buněk (SCAP), bylo prokázáno, že některá kombinace farmakologických činidel (nazývaných politika nebo chemoterapeutika; např. Dasatinib s kvercetinem) může překonat tuto rezistenci. Následný screening flavonoidů odhalil, že 1 byl ještě účinnější než kvercetin a mohl splnit úkol snížení markerů stárnutí jako jediný prostředek (Yousefzadeh et al., 2018). Modelové experimenty, které začaly se S. cerevisiae a pokračovaly přes D.melanogaster až k obratlovcům, jasně ukazují, že fisetin je schopen prodloužit životnost zkoumaných organismů obou pohlaví (Wood et al, 2004; Si et al, 2011; Wagner et al, 2015). V důsledku těchto zjištění tým JL Kirkland na Mayo Clinic nedávno navrhl a zahájil klinickou studii zaměřenou na „zmírnění křehkosti, zánětu a souvisejících opatření u starších dospělých pomocí fisetinu“ (AFFIRM-LITE) s fisetinem podávaným perorálně. v dávkách do 20 mg na kilogram tělesné hmotnosti pacienta¹. S ohledem na špatnou rozpustnost (10,45 ug/ml), relativně nízkou orální biologickou dostupnost (44 procent) a rychlý metabolismus, takový vývoj zaručuje zájem o potenciální zdroje fisetinu pro vhodné farmaceutické formulace. Nedávné studie in vitro poskytly mechanický pohled na to, jak fisetin inhibuje cíl rapamycinové dráhy v různých buněčných modelech, a proto ovlivňuje buněčné dráhy, o kterých je známo, že ovlivňují stárnutí (Syed et al., 2013; Pallauf et al 2016). Bylo také zjištěno, že fisetin v kombinaci s jinými epigeneticky aktivními molekulami, které jsou schopné překročit bariéru krev-voda a krev-sítnice, vykazuje synergické příznivé účinky. To platí pro nízkou dávku polyfenolů z červeného vína, stejně jako pro vitamín D3 a některé další sloučeniny s nízkou molekulovou hmotností, synergicky zlepšující zrakovou ostrost u pacientů s pokročilou atrofickou věkem podmíněnou svalovou degenerací, včetně starších pacientů s pokročilým stadiem nemoc, pro kterou zbývalo jen velmi málo možností (Ivanova et al.2017).

Cistanche může proti stárnutí
Vezmeme-li v úvahu střední dostupnost přírodního fisetinu na mezinárodním trhu na jedné straně a jeho vysokou biologickou aktivitu na straně druhé, potravinové doplňky této sloučeniny jsou stále vzácné. Na trhu existuje několik doplňků stravy obsahujících fisetin, které mají podle výrobců „zdánlivý přínos pro zdraví mozku“. Jsou inzerovány jako senoterapeutické (Yousefzadeh et al., 2018), antikarcinogenní, dietní antioxidanty pro podporu zdraví (Khan et al, 2013), protože neurotrofické, protizánětlivé látky vyžadují kritické zhodnocení již popsaných syntéz, zejména s ohledem na současné požadavky na farmaceutickou SVP a zajištění kvality.
První syntéza 1, dokončená v roce 1904 (Kostanecki et al, 1904), zahrnovala přípravu částečně chráněného chalkonu, který by mohl být cyklizován na flavanon za kyselých podmínek. Další krok v pokroku oxidace meziproduktu fenylpropanoidu byl dosažen pomocí amylnitrátu, který sloužil jako oxidační činidlo. Postupná hydrolýza oximu a deprotekce alkylovaných fenolových skupin pomocí HI poskytly fisetin identický s autentickým vzorkem izolovaným z rostlinného zdroje (obrázek 4). Tato metoda má několik nedávných modifikací, které se většinou věnují krokům oxidace a demethylace (Hasan et al, 2010; Borsari et al., 2016).
Další pokus o přípravu 1 učinil Robinson v roce 1926 (Allan a Robinson, 1926). Zpracování o-methoxyreacetofenonu anhydridem kyseliny veratrilové v přítomnosti veratanu draselného v ethanolu v utěsněné skleněné zkumavce při 180 stupních poskytlo požadovaný chrom{5}}on, který byl převeden na 1 pomocí jodovodíku (obrázek 5).
V poslední době byly vyvinuty šetrnější metody pro flavonoidy obecně a flavonoly zvláště. Je třeba zdůraznit, že v současné době, jak je znázorněno na obrázku 6, existuje široký výběr syntetických metod používaných k přípravě chalkonů, které zůstávají hlavními meziprodukty pro cyklizaci na chromanony (Zhuang et al., 2017). Zejména s pomocí U moderních katalyzátorů na bázi přechodných kovů může tvorba vazeb uhlík-uhlík mezi dvěma aromatickými synthony probíhat různými způsoby, jak objevili Heck, Suzuki a Negishi (Johansson-Seechurn et al., 2012).
Zvláště zajímavé jsou zde chalkony hydroxylované v ortho-poloze ke ketonové skupině, protože mohou snadno podléhat cyklizaci vedoucí k flavonovým prekurzorům a flavonům (obrázek 7), mnohem vzácněji k auronům (nezobrazeno) (Krohn et al., 2009; Megens a Roelfes, 2012; Nising a Bräse, 2012; Zhang a kol., 2013; Masesane, 2015).

Vzhledem k snadné dostupnosti chalkonů (snadno transformovatelných na flavony, např. jodem podporovanou cyklizací prováděnou v DMSO) lze jejich epoxidaci s následným intramolekulárním otevřením oxiranového kruhu považovat za metodu volby pro přípravu flavonolu. Ve skutečnosti byla taková cesta vyvinuta v praktickou syntetickou metodu postupným úsilím irských a japonských výzkumníků a jejich následovníků. V současné době známá jako reakce Algar-Flynn-Oyamada (AFO), používá zásaditý roztok peroxidu vodíku jako klíčové činidlo (Oyamada, 1935; Gunduz et al, 2012; Bhattacharyya a Hatua, 2014; Shen et al, 2017). Jeho obecné schéma, které ukazuje typické substituční vzory, je uvedeno níže (obrázek 8). Tato reakce nabízí možnost tvorby produktu auronu otevřením -oxiranového kruhu, přičemž obvykle jsou uváděny pouze mírné výtěžky flavonolů. Je třeba zmínit, že flavony, které jsou snadněji dostupné než flavonoly různými preparativními postupy, lze snadno halogenovat v poloze 3 pomocí činidel, která generují kladně nabité atomy halogenu, jako je NCS(N-chlorsukcinimid), NBS (N-bromsukcinimidy) nebo jód v přítomnosti CAN (dusitan ceru-amonný). Zdá se, že toto zdánlivě


zřejmá cesta nebyla využita jako praktická metoda pro přípravu flavonolů.
V novějším pokusu o přípravu flavanolů byla organokovová chemie aplikována na arylační krok katalyzovaný 2-bromochromanonem Pd, jak je znázorněno níže (obrázek 9). V případě fisetinu byly dokončeny dva zásadní kroky syntézy v 75 procentech celkového výtěžku (Rao a Kumar, 2014). V zásadě mohou být při takové reakci arylovány tři ekvivalenty bromchromonového substrátu jedním ekvivalentem vhodného fenylbismutového činidla.
Zdá se, že původní myšlenka Kostanecki, kde byly flavanony vybrány jako hlavní substráty pro transformaci, nebyla dosud plně využita, ačkoli již bylo prokázáno, že prekurzory, jako jsou flavony, mohou být přímo oxidovány na flavanoly, například 3 ,3-dimethyldioxiran (Maloney a Hecht, 2005). V této souvislosti je třeba zmínit polosyntézu jako více než teoretickou možnost. Příklad transformace hesperidinu (hojný citrusový flavanon snadno získatelný z pomerančové kůry) na methoxylovaný 3-flavonol v 5 syntetických krocích jasně ukazuje, že některé přírodní produkty mohou být zpracovány jako vhodné substráty pro požadovaný flavonoidní materiál (Garg et al, 2001; Lewin a kol., 2010).
I když se zdá, že výše uvedený seznam reakcí vyčerpává chemické syntetické prostředky pro potenciální dostupnost fisetin API (Molga et al, 2019), současné průmyslové trendy naznačují, že biotransformace je třeba považovat za konečný zdroj chemických entit pro lidské použití v potravinových a léčivých doplňcích. . Za tímto účelem existují značné poznatky o biosyntéze fisetinu: chalkon isoliquiritigenin je cyklizován na flavanon liquiritigenin, hydroxylován na katechin garbanzo, flavon resoka kaempferol a oxidován na 1. Všechny biokatalyzátory pro tento řetězec transformací jsou navíc úspěšně známy. exprimován v mikroorganismech pro přípravu kvercetinu i fisetinu (Jendresen et al., 2015; Stahlhut et al., 2015; Jones et al., 2016; Pandey et al., 2016; Rodriguez et al., 2017).

ZÁVĚRY A VÝHLEDY
Průměrný denní příjem fisetinu z různých rostlinných zdrojů se odhaduje na úrovni 0,4 mg (Kashyap et al., 2018). S ohledem na nedávná zjištění týkající se jeho prospěšných antioxidačních, protizánětlivých, protinádorových, neuroprotektivních biologických aktivit a účinků proti stárnutí lze předpokládat rostoucí potřebu vysoce čisté látky vhodné pro farmaceutický vývoj. Hledání léčivého stavu 1 může být pomalé a obtížné, jak ukazuje historie stažení flavonoidů z vitaminového stavu. Současná poptávka po přírodních produktech, jako je fisetin, však může pocházet z méně regulovaných trhů, jako je tomu v případě funkčních potravin nebo doplňků stravy. Pro funkční potravinu a její současnou definici neexistuje jednotný právní pojem: „přírodní nebo zpracované potraviny, které obsahují biologicky aktivní sloučeniny; které v definovaných, účinných, netoxických množstvích poskytují klinicky ověřený a zdokumentovaný zdravotní přínos s využitím specifických biomarkerů, pro prevenci, řízení nebo léčbu chronické nemoci nebo jejích příznaků“ (Danik a Jaishree, 2015; Martirosyan, 2015) nemusí znít ideálně. Nicméně plní účel, pokud jde o používání zdravotních tvrzení, a může jistě podpořit nové vstupy na trh za předpokladu, že se na podporu přítomnosti nových složek v potravinářských výrobcích použije dobrá věda. Chemická syntéza se zdá být zřejmým řešením první pomoci s návrhem procesu založeným na chalkonových meziproduktech, podél cesty AFO. Tato jednoduchá chemie však vyžaduje značné optimalizační úsilí zaměřené na minimalizaci nebo dokonce eliminaci chemického vstupu ochranných skupin. Případně je třeba pečlivě prozkoumat dostupnost vhodných (tj. 5-deoxy) meziproduktů, protože flavon{11}}oly lze získat chemickou transformací z jejich strukturních příbuzných, jako je flavan{{12} }jedničky a flavony, katechiny a chalkony. V každém případě je třeba dbát na zvýšení špatné rozpustnosti a biologické dostupnosti 1. Některá technická řešení již byla navržena (DeCorte, 2016; Chadha et al., 2019). Problém nízké rozpustnosti fisetinu by mohl být překonán jeho komplexací s dimerem cyklosoforoázy a cyklodextriny, což také významně zlepšuje cytotoxicitu fisetinu proti buňkám HeLa (Jeong et al, 2013; Zhang et al, 2015). Takové studie mohou dobře posloužit k rozšíření medicínské chemické kapacity sloučeniny 1, stejně jako jejích analogů a derivátů, po četných příkladech sekundárních metabolitů využívaných jako hlavní léčiva. Konečně je pravděpodobné, že budoucnost výroby fisetinu jako API (nebo jeho prekurzoru) by mohla ležet v oblasti biotechnologií (Wu et al., 2018; Huccetogullari et al., 2019; Market al., 2019). V tomto případě je třeba poukázat na to, že suplementace jediným činidlem (jako je 1) může vyvolat jiné celkové farmakologické účinky než rostlinná strava bohatá na stejnou látku, protože v druhém případě celý 5-deoxyflavonoidní segment rostlinný metabolom (který obsahuje mnoho příbuzných jednotlivých chemikálií) se střetává s biologií lidského systému, což vede k podstatně složitější síti vzájemných interakcí.
Tento článek je extrahován z Frontiers in Chemistry|www.frontiersin.org 1. října 2019|Svazek 7|Článek 697
