Je neurofilament užitečným biomarkerem pro ženy s Fabryho chorobou?
Mar 04, 2022
Lehký řetězec neurofilamentu séra není užitečným biomarkerem postižení centrálního nervového systému u žen s Fabryho chorobou
Kontakt: emily.li@wecistanche.com
Tomasz Hołub, Kamila Kędzierska, Katarzyna Muras-Szwedziak, Michał Nowicki*
Klinika nefrologie, hypertenze a transplantace ledvin Lékařské univerzity v Lodži, Polsko.
SOUHRN
NeurofilamentSérová koncentrace lehkého řetězce (NfL) je novým neinvazivním markerem neurodegenerativních poruch. Fabryho choroba (FD) vede k akumulaci glykosfingolipidů ve tkáních, což vede k progresivnímu poškození kritických tělesných systémů a orgánů, včetně periferního a centrálního nervového systému. Neexistují žádné zavedené sérové markery neurodegenerace u FD. Naše průřezová jednocentrická studie byla navržena tak, aby prokázala koncept, že hladiny NfL v séru mohou odrážet závažnost kognitivní poruchy a nepřímo i hladinucentrální nervový systémzapojení u žen v časnějších stádiích FD. Bylo zahrnuto 12 žen s diagnózou FD potvrzenou genetickými testy a 12 odpovídajících zdravých subjektů. Sérové koncentrace NfL byly měřeny u všech subjektů společně s neuropsychologickými testy, které zahrnovaly Mini Mental State Examination (MMSE) a Montrealskou kognitivní škálu hodnocení (MoCA). Kvalita života byla hodnocena pomocí Short Form Survey (SF-36). Pacienti s FD a zdraví jedinci se nelišili s ohledem na koncentraci NfL v séru, výsledky neuropsychologických testů a kvalitu života. U žen s FD byla signifikantně pozitivní korelace mezi NfL a koncentrací globotriaosylosfingosinu (lyso-Gb3) (R=0,69, p=0,01). Byla zde také korelace mezi koncentrací NfL a skóre MoCA, ale nikoli skóre MMSE. Analýza provozních charakteristik přijímače (ROC) ukázala, že nejlepším prediktorem mírné kognitivní poruchy v obou skupinách byla eGFR. Zdá se, že koncentrace NfL v séru nepředpovídá stupeň postižení nervového systému u žen s FD.
klíčová slova:biomarker, neurodegenerace, kvalita života

Cistanche vám pomůže mít dobrou kvalitu života
1. Úvod
Fabryho nemoc (FD), je ultravzácné lysozomální střádavé onemocnění, které se dědí jako X-vázaná porucha. FD je způsobena deficitem lysozomálního enzymu alfagalaktosidázy A (-Gal A; EC 3.2.1.22). Gen GLA, umístěný na X chromozomu na Xq22, kóduje 429 aminokyselinový prekurzor, který je zpracován na 398 aminokyselinový glykoprotein fungující jako homodimer. Mutace GLA vede k nedostatku nebo absenci enzymu -galaktosidázy A ( -Gal A), který katalyzuje hydrolýzu globotriaosylceramidu.
Nedostatek alfa-Gal A vede k progresivní akumulaci glykolipidů a globotriaosylosfingosinu (lyso-Gb3) v různých buňkách těla, což vede k poškození a dysfunkci postižených orgánů. Mezi nejvíce postižené buňky a tkáně u FD patří glomerulární podocyty, kardiomyocyty, endoteliální buňky, vaskulární svaly a periferní a centrální nervy. To vše vede k dysfunkci a selhání životně důležitých orgánů včetně srdce, ledvin a nervového systému. Závažnost onemocnění závisí na pohlaví, věku a typu mutace. Muži s klasickým fenotypem mají nejvyšší riziko komplikací a časných příznaků, zatímco mladší ženy jsou většinou postiženy FD později v životě (1).
Neurofilamentajsou hlavní složkou neuronového cytoskeletu. Lehké (NfL), střední (NfM) a těžké (NfH) řetězce byly rozlišeny na základě jejich molekulové hmotnosti. Sérové koncentrace NfL a jejich význam jako markeru onemocnění centrálního nervového systému byly prokázány v několika nedávných studiích (2,3). Poškození neuronů a fyziologické změnycentrální nervový systém(CNS) způsobují uvolnění neurofilament. To se promítá do zvýšených hladin NfL v mozkomíšním moku a nakonec v krvi, kde jeho koncentrace odráží rychlost, jakou se NfL uvolňuje z neuronů (3). Několik studií prokázalo silnou pozitivní korelaci mezi NfL v krvi a v mozkomíšním moku (4). Koncentrace NfL v séru pozitivně korelovala se závažností různých onemocnění centrálního nervového systému včetně roztroušené sklerózy, amyotrofické laterální sklerózy, frontotemporální demence, Alzheimerovy choroby, traumatických poranění mozku a degenerace nervového systému spojené s infekcí HIV (2).

Je neurofilament užitečným biomarkerem pro ženy s Fabryho chorobou?
Hlavním fyziologickým faktorem ovlivňujícím koncentraci NfL je věk pacientů. Se stárnutím se koncentrace NfL u zdravých jedinců zvyšovala o 2,2 procenta ročně. Po 60. roce věku je pozorován další významný vzestup koncentrace NfL (5). Tyto změny lze přičíst jak samotnému stárnutí, tak agregaci komorbidit. Bylo dobře prokázáno, že pacienti s FD se vyznačují mnohem rychlejším stárnutím mozku ve srovnání se zdravou populací (6). Pacienti s FD mají zvýšené riziko rozvoje kognitivní dysfunkce a většina z nich má také příznaky deprese (7). Pacienti s diagnózou těžké deprese mají více kognitivní poruchy ve srovnání s běžnou populací (8). Bylo také prokázáno, že u velké depresivní poruchy byly pozorovány vyšší hladiny NfL (9). U FD však nebylo potvrzeno, že by kognitivní porucha byla způsobena symptomy deprese, ale mezi její rizikové faktory patří mužské pohlaví, pacienti s klasickým fenotypem onemocnění, nižší inteligenční kvocient (IQ) a anamnéza cévní mozkové příhody (10,11).
Pro hodnocení kognitivních funkcí bylo vyvinuto mnoho klinických testů, z nichž každý hodnotí specifické domény kognitivního fungování, ale v jiném aspektu. Screeningové testy hrají klíčovou roli v tom, že umožňují každému lékaři provést počáteční posouzení kognitivní poruchy. Mezi nejlépe validované testy používané pro screening kognitivních poruch patří Mini Mental State Examination (MMSE) a Montreal Cognitive Assessment Scale (MoCA) (12,13). MMSE a MoCA byly použity a dobře ověřeny v nedávných studiích hodnotících kognitivní poruchu u pacientů s FD (11,14). Cílem studie bylo posoudit, zda sérová koncentrace NfL může být markerem časnéhocentrální nervový systémpostižení a kognitivní poruchy u žen s FD.
Tabulka 1. Klinické charakteristiky studované populace

eGFR: odhadovaná rychlost glomerulární filtrace; MMSE: Mini Mental State Examination; MoCA: Montreal Cognitive Assessment Scale; SF-36: The Short Form 36 Health Survey
2. Materiály a metody
Studie byla schválena Místní etickou komisí a byla provedena v souladu s Helsinskou deklarací. Všichni pacienti dali informovaný písemný souhlas s účastí ve studii.
Bylo zařazeno 24 subjektů, včetně 12 žen s potvrzenou FD a 12 odpovídajících zdravých kontrol. Studie byla provedena mezi březnem a říjnem 2020. Charakteristiky studované populace jsou uvedeny v tabulce 1. Diagnóza FD byla založena na koncentraci -Gal A, lyso-Gb3 v krvi a na genetických testech. Testy byly provedeny metodou Dry Blood Spot (DBS). Jednotlivé výsledky jsou uvedeny v tabulce 2. Pouze jedna žena ze studijní skupiny byla kvalifikována pro enzymovou substituční terapii.
Pacienti s FD zařazení do naší studie pocházeli ze tří různých rodin. Míra laskavosti a rodokmeny pacientů jsou uvedeny na obrázku 1.
Kontrolní skupinu tvořilo 12 zdravých žen, odpovídajících ženám s FD podle věku, úrovně vzdělání a funkce ledvin. Vylučovacími kritérii byla diagnóza jakéhokoli onemocněnícentrální nervový systémjiné než spojené s FD, postižení, které by bránilo jakémukoli ze studijních postupů, jako je ztráta sluchu nebo zraku, chronické onemocnění ledvin s eGFR < 30 ml/min, demence, akutní funkční psychiatrická porucha a nekontrolovaná hypertenze (systolický TK > 130 mmHg nebo diastolický TK > 80 mmHg).
Každý pacient vyplnil dotazník kvality života The Short Form 36 Health Survey (SF-36) a dva screeningové testy hodnotící kognitivní funkce, MoCA a MMSE.
MoCA a MMSE se běžně používají jako screeningové neuropsychologické škály. U MMSE je nejčastěji používaným hraničním bodem pro diagnózu demence skóre 24 bodů nebo méně. Maximální skóre za test MoCA je 30 bodů; výsledek 26 nebo více bodů je definován jako normální. Skóre od 19 do 25 je považováno za mírnou kognitivní poruchu (MCI) (13).
Během stejné návštěvy byla všem účastníkům odebrána krev nalačno po nočním odpočinku, aby se stanovila sérová koncentrace NfL, kreatininu, močoviny, vápníku, fosfátu, parathormonu (PTH) a krevního hemoglobinu. Koncentrace NfL byla hodnocena pomocí aNeurofilamentLight Polypeptide (NEFL) ELISA Kit (antibodies-online GmbH, Aachen, Německo). Ostatní parametry byly měřeny pomocí rutinních automatizovaných laboratorních metod v místní laboratoři.
Pro každou normálně rozdělenou proměnnou byla vypočtena střední hodnota a standardní odchylka. Pro nenormálně rozdělené proměnné byla vypočtena střední hodnota s interkvartilním rozsahem (IQR). Analýza normality rozdělení byla provedena Shapiro-Wilkovým testem a na základě jeho výsledků byl použit parametrický t-test nebo neparametrický Mann-Whitney U test. Křivky operačních charakteristik přijímače (ROC) byly nakresleny pro posouzení hodnoty sérové koncentrace NfL, eGFR, lyso-Gb3 a -Gal A indikující přítomnost mírné kognitivní poruchy v testu MoCA. K provedení statistické analýzy byl použit software Statistica 13.1.
Tabulka 2. Typ genetické varianty, koncentrace globotriaosylosfingosinu a -galaktosidázy A v krvi u žen sFabryho nemoc
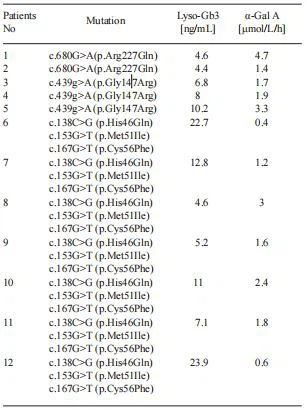
Lyso-Gb3: globotriaosylosfingosin; -Gal A - -galaktosidáza A.

Obrázek 1. Rodokmeny tří rodin sFabryho nemoczahrnuty do naší studie
3. Výsledky a diskuse
Koncentrace NfL v séru se mezi skupinami významně nelišila ({{0}},053 ± 0,1 vs. 0,048 ± 0 ,09 ng/ml; p=0,9). Ženy s FD měly také podobný krevní hemoglobin, sérový fosfát a PTH. Koncentrace vápníku v séru byla vyšší ve skupině FD než u zdravých žen (2,38 ± 0,08 vs. 2,28 ± 0,11 mmol/l, v tomto pořadí; p=0,03). Skóre MMSE, MoCA a SF{20}} byla také podobná v každé skupině.
U žen s FD byla signifikantně pozitivní korelace mezi věkem a koncentrací PTH v séru (R=0,62, p=0,03). Stejná korelace nebyla pozorována v kontrolní skupině.
Ve skupině FD byla také signifikantně pozitivní korelace mezi koncentrací NfL a lyso-Gb3 (R=0,69, p=0,01).
V kontrolní skupině byla nalezena signifikantně negativní korelace mezi sérovým NfL a hemoglobinem (R= -0,8, p=0,001) MoCA skóre (R=-0,6, p {{6 }}.04) a pozitivní korelaci mezi NfL a koncentrací PTH v séru (R=0.8, p=0.0009). Tyto korelace nebyly u žen s FD přítomny.
V kontrolní skupině byla silná negativní korelace mezi věkem a skóre MoCA (R=-0,83, p=0,0009) a pozitivní korelace mezi věkem a skóre SF-36 (R=0.6, p=0.04). Ve skupině FD byla pozorována pouze významná korelace mezi věkem a skóre MoCA (R=-0,85, p=0,0004).
ROC analýza ukázala, že nejlepším prediktorem MCI v obou skupinách byl eGFR. Plocha pod křivkou (AUC) u žen s FD byla {{0}},938 (95 procent CI: 0.792 - 1.083) a v kontrolní skupina 0,857 (95 procent CI: 0.{10}},086). Podrobné informace o výsledcích analýzy ROC jsou uvedeny na obrázku 2.

Obrázek 2. Prediktory mírné kognitivní poruchy a provozní charakteristiky přijímače.
Naše průřezová jednocentrická studie byla navržena tak, aby prokázala koncept, že hladiny NfL v séru by mohly odrážet závažnost kognitivní poruchy a nepřímo míru postižení CNS u žen v časnějších stádiích FD bez předchozích klinických příznaků postižení nervového systému. Hypotézou studie bylo, že poškození neuronů u pacientů s FD povede ke zvýšení koncentrace NfL v mozkomíšním moku a jeho pronikání do periferního oběhu, což lze hodnotit měřením jejich sérových hladin. Loeffler T, a kol. na myším modelu ukázal, že koncentrace NfL může být cenným biomarkerem nejen u typických neurodegenerativních onemocnění, ale také u jiných onemocnění, která mají další neuronální složku, jako jsou lysozomální střádavá onemocnění, např. Gaucherova choroba (15). Erante D, a kol. potvrdili, že NfL je dobrým biomarkerem neurodegenerace u Niemann-Pickovy choroby (16). Ru Y, a kol. popsali NfL jako biomarker neurodegenerace u neuronální ceroidní lipofuscinózy typu 2 (onemocnění CLN2), další lysozomální střádavou chorobu. Tito autoři prokázali na psím modelu významnou korelaci mezi koncentrací NfL v séru a progresí onemocnění. Na rozdíl od toho v lidské části své studie nebyli schopni prokázat korelace mezi koncentrací NfL a závažností CLN2 nebo věkem pacientů. Ukázali však, že koncentrace NfL se po zahájení enzymatické substituční terapie snížila o 50 procent (17).

Je neurofilament užitečným biomarkerem pro ženy s Fabryho chorobou?
Výše citované studie hodnotily užitečnost NfL jako abiomarkerpro zapojení nervového systému do některých lysozomálních střádavých onemocnění. Pokud je nám známo, žádné podobné studie u pacientů s FD neproběhly. U FD mají ženy obvykle mírnější průběh onemocnění než muži, což je způsobeno náhodnou inaktivací X chromozomu. Závažné postižení takových cílových orgánů, jako je srdce nebo ledviny, je však zcela běžné (18). Navzdory reziduální enzymatické aktivitě se u žen s FD s věkem rozvíjejí charakteristické symptomy, včetněcentrálnínervovýSystémpříznaky. Klinická manifestace je však pestřejší a příznaky se objevují zhruba o 10 let později ve srovnání s muži. Medián intervalu mezi nástupem časných příznaků FD a správnou diagnózou je u žen ještě opožděnější, v průměru o 19 let [19]. Identifikace markeru časného postižení nervového systému u žen s FD by mohla být zvláště klinicky relevantní, protože u žen s tímto onemocněním se symptomy rozvinou mnohem později než u mužů, ale nejčastěji je postižen nervový systém. Symptomy FD významně zasahují do každodenního fungování pacientů, což přispívá k výrazně zkrácené délce života. Studie ukazují, že délka života mužů s Fabryho chorobou je o 15 až 20 let kratší a žen o 6 až 10 let kratší ve srovnání s průměrnou délkou života v populaci (20). V naší studii jsme nebyli schopni potvrdit, že koncentrace NfL je klinicky užitečným biomarkerem pro hodnocení stupně postižení nervového systému u žen s FD. Důvodem může být nízký věk pacientů zařazených do studie a skutečnost, že většina z nich neměla žádné nebo středně závažné typické příznaky onemocnění z jiných orgánů než z nervového systému. U většiny našich sledovaných subjektů byly provedeny genetické testy z důvodu diagnózy FD u jejich příbuzných.
Aktivity -Gal a koncentrace lyso-Gb3 jsou sérové markery běžně používané při diagnostice a monitorování FD. Měření aktivity -Gal v plazmě nebo leukocytech, které je referenční metodou pro laboratorní potvrzení diagnózy u mužů, je často neprůkazné u pacientek, jejichž enzymatická aktivita se může pohybovat od nízkých po normální hodnoty. V naší studii mělo 25 procent žen s FD normální aktivitu -Gal a koncentrace lyso-Gb3 byla ve všech případech nadnormální. Základ variability fenotypu u žen je stále nedostatečně objasněn, ale úloha inaktivace chromozomu X se zdá být nejdůležitější (21). U FD jsou hladiny lyso-Gb3 vždy zvýšené u mužů, ale pouze mezi 40 a 60 procenty u žen. Hladiny lyso-Gb3 se u žen zvyšují s věkem a v dětství jsou v normálním rozmezí. Při podezření na symptomatickou FD u dospělých žen však jak měření -Gal A, tak plazmatické lyso-Gb3 aktivity zlepšuje diagnostickou hodnotu (18).
V naší studii koncentrace lyso-Gb3 nekorelovala s výsledky testů validovaných pro diagnostiku kognitivní dysfunkce a s výsledky SF-36. Přes žádný rozdíl v koncentraci NfL mezi studovanou a kontrolní skupinou byla pozorována pozitivní významná korelace mezi koncentrací lyso-Gb3 a NfL v populacích žen s FD. Akumulace depozit lyso-Gb3 v důsledku nedostatku -Gal A způsobuje poškození nervových buněk s následnou prozánětlivou aktivitou (22,23). Je možné, že vzhledem k časné diagnóze onemocnění a absenci předchozích neurologických příznaků v naší studijní skupině bylo riziko neurodegenerace nízké, a proto nebyl pozorován žádný rozdíl v sérové koncentraci NfL mezi těmito dvěma skupinami.
Dosud provedené studie ukázaly, že pacienti s FD mají významné kognitivní deficity (24). Většina studií připisovala změny kognitivních funkcí v průběhu FD akumulaci glykosfingolipidů v cerebrální cirkulaci (25). V naší studii však nebyl nalezen žádný vztah mezi koncentrací lyso-Gb3 a kognitivní poruchou. Pro screening kognitivní poruchy v klinické praxi bylo vyvinuto mnoho psychologických testů. Liší se svou citlivostí a specificitou. Nejčastěji používaným screeningovým testem v diagnostice kognitivní poruchy je MMSE. Körver S, a kol. ukázal, že MMSE neumožnil screening na MCI u pacientů s FD a může ztratit svou prediktivní hodnotu, když je kognitivní porucha mírnější, méně rozšířená a vyskytuje se převážně v exekutivní doméně, jak se zdá být v případě FD (14). Naše výsledky jsou v souladu se zjištěním, že MMSE nedokáže přesně odlišit pacienty s jemným kognitivním postižením od pacientů bez klinicky detekovatelné kognitivní poruchy. Proto by měla být MoCA upřednostňována před MMSE v populacích s rizikem MCI nebo s demencí v časném stadiu. Ve studii provedené Körver S, et al. Dotazník MoCA klasifikoval 21 procent pacientů s FD jako s MCI, ve srovnání s 11 procenty v referenční skupině [14]. Tyto údaje jsou v souladu s našimi výsledky. V naší studii bylo pomocí testu MoCA identifikováno více pacientů s MCI ve srovnání s MMSE.
V naší studii bylo průměrné skóre v testu MMSE a MoCA podobné u žen s FD a kontrolních subjektů. Löhle M, a kol. také nenalezli žádný významný rozdíl v testech zpřístupňujících kognitivní funkce mezi pacienty s FD a zdravými subjekty. Jejich studijní skupina byla větší, zahrnovala ženy i muže v různých stadiích FD a s klasickým i pozdním typem (11). Naproti tomu naše studie zahrnovala pouze ženy bez jakýchkoli příznakůcentrálnínervovýSystémúčast.
Výsledky naší studie naznačují, že ani deprese, ani závažnost onemocnění, doba od příznaků FD a aktivita enzymů nepředpovídaly kognitivní dysfunkci. Analýza nezjistila žádnou souvislost mezi kognitivní poruchou a výsledky testů
Onemocnění ledvin je jednou z hlavních komplikací FD a je spojeno s kontinuální akumulací glykosfingolipidů v celém nefronu. To vede k progresivní ztrátě GFR a nakonec k selhání ledvin. Ledviny a mozek sdílejí podobné hemodynamické schopnosti, jako je vazoregulace mikrocirkulace. Studie ukázaly, že nižší eGFR byl spojen se zvyšující se závažností chronické hyperintenzity bílé hmoty (CWMH) a pacienti se stabilnější eGFR měli méně cévních mozkových příhod než pacienti s rychle progredujícím onemocněním ledvin (26). Naše studie také naznačuje důležitost hladin eGFR jako prediktoru MCI u této skupiny pacientů. Proto je nutný další výzkum vztahu mezi hladinami eGFR a MCI u pacientů s FD (9).

Je neurofilament užitečným biomarkerem pro ženy s Fabryho chorobou?
V naší studii jsme neprokázali souvislost mezi zvýšenými hladinami sérového vápníku u žen s FD a sérovým PTH. V jedné předchozí studii se autoři pokusili objasnit patomechanismus kalcium-fosfátových poruch u pacientů s FD pomocí myšího modelu GlatmTg (CAG-A4GALT). Výsledky studie ukázaly vztah mezi hyperkalcémií a hyperkalciurií a sekundární hypertyreózou (27). To může naznačovat, že pacienti s FD mají zvýšené riziko zrychlené kostní resorpce a osteomalacie (28).
Naše studie má omezení, protože jsme hodnotili koncentraci NfL pouze v periferní cirkulaci. Předchozí studie však ukázaly, že koncentrace NfL v krvi silně koreluje s jeho koncentrací v mozkomíšním moku (29,30). Dalším omezením je malý studijní soubor, který je důsledkem ultra nízkého výskytu onemocnění v populaci a selekce pouze pacientek bez předchozích známekcentrální nervový systémzapojení typické pro FD.
4. závěr
Výsledky naší studie nepotvrdily vztah mezi mírou postižení nervového systému u žen s FD a hladinou NfL v séru. Proto nelze sérový NfL považovat za užitečný marker kognitivní poruchy u tohoto onemocnění. Naše studie také ukázala, že MoCA je preferovaným testem pro detekci mírné kognitivní poruchy u FD.
Financování: Studie byla podpořena grantem Lékařské univerzity v Lodži č. 503/1-151-02/503-01.
Střet zájmů: Autoři nemají žádné střety zájmů, které by mohli zveřejnit.
Reference
1. Sodré LSS, Huaira RMNH, Bastos MG, Colugnati FAB, Coutinho MP, Fernandes NMDS. Screening Fabryho choroby u onemocnění ledvin: průřezová studie u mužů a žen. Kidney Blood Press Res. 2017; 42:1258- 1265.
2. Weydt P, Oeckl P, Huss A, Muller K, Volk AE, Kuhle J, Knehr A, Andersen PM, Prudlo J, Steinacker P, Weishaupt JH, Ludolph AC, Otto M. Hladiny neurofilamentů jako biomarkery u asymptomatických a symptomatických familiárních Amyotrofní laterální skleróza. Ann Neurol. 2016; 79:152- 158.
3. Khalil M, Teunissen CE, Otto M, Piehl F, Sormani MP, Gattringer T, Barro C, Kappos L, Comabella M, Fazekas F, Petzold A, Blennow K, Zetterberg H, Kuhle J. Neurofilamenta jako biomarkery u neurologických poruch . Nat Rev Neurol. 2018; 14:577-589.
4. Thebault S, D RT, Lee H, Bowman M, Bar-Or A, Arnold DL, H LA, Tabard-Cossa V, Freedman MS. Vysoký sérový lehký řetězec neurofilament se normalizuje po transplantaci hematopoetických kmenových buněk pro RS. Neurol Neuroimmunol Neuroinflamm. 2019; 6:e598.
5. Khalil M, Pirpamer L, Hofer E, Voortman MM, Barro C, Leppert D, Benkert P, Ropele S, Enzinger C, Fazekas F, Schmidt R, Kuhle J. Hladiny lehkého řetězce neurofilamentu v séru při normálním stárnutí a jejich souvislost s morfologické změny mozku. Nat Commun. 2020; 11:812.
6. Wadley VG, McClure LA, Warnock DG, Lassen-Greene CL, Hopkin RJ, Laney DA, Clarke VM, Kurella Tamura M, Howard G, Sims K. Kognitivní funkce u dospělých stárnoucích s Fabryho chorobou: případová studie proveditelnosti pomocí telefonického hodnocení. JIMD rep. 2015; 18:41-50.
7. Cole AL, Lee PJ, Hughes DA, Deegan PB, Waldek S, Lachmann RH. Deprese u dospělých s Fabryho chorobou: běžný a nedostatečně diagnostikovaný problém. J Zdědit Metab Dis. 2007; 30:943-951.
8. Rock PL, Roiser JP, Riedel WJ, Blackwell AD. Kognitivní porucha u deprese: systematický přehled a metaanalýza. Psychol Med. 2014; 44:2029-2040.
9. Tapia D, Kimonis V. Cévní mozková příhoda a chronické onemocnění ledvin u Fabryho choroby. J Stroke Cerebrovasc Dis. 2021; 30:105423.
10. Loeb J, Feldt-Rasmussen U, Madsen CV, Vogel A. Kognitivní poruchy a subjektivní kognitivní potíže u Fabryho choroby: celostátní studie a přehled literatury. JIMD rep. 2018; 41:73-80.
11. Lohle M, Hughes D, Milligan A, Richfield L, Reichmann H, Mehta A, Schapira AH. Klinické prodromy neurodegenerace u Anderson-Fabryho choroby. Neurologie. 2015; 84:1454-1464.
12. Tombaugh TN, McIntyre NJ. Státní mini-mentální zkouška: komplexní přehled. J Am Geriatr Soc. 1992; 40:{4}}.
13. Zhuang L, Yang Y, Gao J. Nástroje kognitivního hodnocení pro screening mírné kognitivní poruchy. J Neurol. 2021; 268:1615-1622.
14. Körver S, van de Schraaf SAJ, Geurtsen GJ, Hollak CEM, van Schaik IN, Langeveld M. Mini vyšetření duševního stavu přesně nevyšetřuje objektivní kognitivní poruchu u Fabryho choroby. JIMD rep. 2019; 48:53-59.
15. Loeffler T, Schilcher I, Flunkert S, Hutter-Paier B. Neurofilament-lehký řetězec jako biomarker neurodegenerativních a vzácných onemocnění s vysokou translační hodnotou. Přední Neurosci. 2020; 14:579.
16. Eratne D, Loi SM, Li QX, Varghese S, McGlade A, Collins S, Masters CL, Velakoulis D, Walterfang M. Lehký řetězec neurofilament mozkomíšního moku je zvýšený u Niemann-Pick typu C ve srovnání s psychiatrickými poruchami a zdravými kontrolami a může být markerem léčebné odpovědi. Psychiatrie Aust NZJ. 2020; 54:648-649.
17. Ru Y, Corado C, Soon RK, Jr, Melton AC, Harris A, Yu GK, Pryer N, Sinclair JR, Katz ML, Ajayi T, Jacoby D, Russell CB, Chandriani S. Lehký řetězec neurofilamentů je léčeb- responzivní biomarker u onemocnění CLN2. Ann Clin Transl Neurol. 2019; 6:2437-2447.
18. Michaud M, Mauhin W, Belmatoug N, Garnotel R, Bedreddine N, Catros F, Ancellin S, Lidové O, Gaches F. Kdy a jak diagnostikovat Fabryho chorobu v klinické praxi. Am J Med Sci. 2020; 360:641-649.
19. Godel T, Köhn A, Muschol N, Kronlage M, Schwarz D, Kollmer J, Heiland S, Bendszus M, Mautner VF, Baumer P. Morfometrie a perfuze dorzálních kořenových ganglií in vivo u pacientek s Fabryho chorobou. J Neurol. 2018; 265:2723-2729.
20. Nowicki M, Bazan-Socha S, Blazejewska-Hyzorek B, Gellert R, Imiela J, Kazmierczak J, Klopotowski M, OkoSarnowska Z, Pawlaczyk K, Ponikowski P, Slawek J, Sykut-Cegielska J, Witkowski A, Zwolinska D. Enzymová substituční terapie u Fabryho choroby v Polsku: stanovisko. Pol Arch Intern Med. 2020; 130:91-97.
21. Echevarria L, Benistan K, Toussaint A, Dubourg O, Hagege AA, Eladari D, Jabbour F, Beldjord C, De Mazancourt P, Germain DP. Inaktivace X-chromozomu u pacientek s Fabryho chorobou. Clin Genet. 2016; 89:44-54.
22. De Francesco PN, Mucci JM, Ceci R, Fossati CA, Rozenfeld PA. Vyšší apoptotický stav u mononukleárních buněk periferní krve Fabryho choroby.: účinek globotriaosylceramidu. Mol Genet Metab. 2011; 104:319- 324.
23. De Francesco PN, Mucci JM, Ceci R, Fossati CA, Rozenfeld PA. Imunitní buňky periferní krve Fabryho choroby uvolňují zánětlivé cytokiny: role globotriaosylceramidu. Mol Genet Metab. 2013; 109:93- 99.
24. Elstein D, Doniger GM, Altarescu G. Kognitivní testování u Fabryho choroby: pilotní projekt využívající krátký počítačový hodnotící nástroj. Isr Med Assoc J. 2012; 14:624-628.
25. Ferraz MJ, Kallemeijn WW, Mirzaian M, Herrera Moro D, Marques A, Wisse P, Boot RG, Willems LI, Overkleeft HS, Aerts JM. Gaucherova choroba a Fabryho choroba: nové markery a poznatky v patofyziologii dvou odlišných glykosfingolipidóz. Biochim Biophys Acta. 2014; 1841:811-825.
26. Oksala NK, Salonen T, Strandberg T, Oksala A, Pohjasvaara T, Kaste M, Karhunen PJ, Erkinjuntti T. Onemocnění malých cév mozku a funkce ledvin predikují dlouhodobé přežití u pacientů s akutní cévní mozkovou příhodou. Mrtvice. 2010; 41:1914-1920.
27. Maruyama H, Taguchi A, Mikame M, Lu H, Tada N, Ishijima M, Kaneko H, Kawai M, Goto S, Saito A, Ohashi R, Nishikawa Y, Ishii S. Nízká hustota kostních minerálů v důsledku sekundární hyperparatyreózy v Gla(tm)Tg(CAG A4GALT) myší model Fabryho choroby. FASEB Bioadv. 2020; 2:365-381.
28. Germain DP, Benistan K, Boutouyrie P, Mutschler C. Osteopenie a osteoporóza: dříve nerozpoznané projevy Fabryho choroby. Clin Genet. 2005; 68:93- 95.
29. Novakova L, Zetterberg H, Sundström P, Axelsson M, Khademi M, Gunnarsson M, Malmeström C, Svenningsson A, Olsson T, Piehl F, Blennow K, Lycke J. Sledování aktivity onemocnění u roztroušené sklerózy pomocí sérového neurofilamentního proteinu lehkého řetězce . Neurologie. 2017; 89:2230-2237.
30. Bavato F, Cathomas F, Klaus F, Gütter K, Barro C, Maceski A, Seifritz E, Kuhle J, Kaiser S, Quednow BB. Změněná neuroaxonální integrita u schizofrenie a velké depresivní poruchy hodnocená pomocí lehkého řetězce neurofilamentů v séru. J Psychiatr Res. 2021; 140:141-148.
